
【题目】(1)写出NaHSO4在熔融状态下的电离方程式 _______。
(2)写出NaHCO3在水溶液中的电离方程式 ________。
(3)1mol乙烷气体(C2H6)在氧气中完全燃烧生成二氧化碳和液态水,放出热量1558.3 kJ,写出乙烷燃烧热的热化学方程式________。
(4)含NaOH 20.0g的稀溶液与足量的稀盐酸反应,放出28.7KJ的热量,表示该反应的热化学方程式是___。
【答案】NaHSO4= Na++HSO4- NaHCO3= Na++ HCO3- C2H6(g)+![]() O2(g)=2CO2(g)+3H2O(g) △H=-1558.3 kJ /mol NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.4kJ /mol
O2(g)=2CO2(g)+3H2O(g) △H=-1558.3 kJ /mol NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.4kJ /mol
【解析】
根据题意可知,本题考查电离方程式和热化学方程式的书写,运用电离方程式和热化学方程式的书写步骤分析。
(1)NaHSO4在熔融状态下电离成钠离子和硫酸氢根离子,NaHSO4= Na++HSO4-。
故答案为:NaHSO4= Na++HSO4-;
(2) NaHCO3在水中全部电离成钠离子和碳酸氢根离子,NaHCO3= Na++ HCO3-。
故答案为:NaHCO3= Na++ HCO3-;
(3) 燃烧热是指1mol纯物质完全燃烧生成稳定的氧化物所放出的热量,1mol乙烷气体(C2H6)在氧气中完全燃烧生成二氧化碳和液态水,放出热量1558.3 kJ,则乙烷燃烧热的热化学方程式为:C2H6(g)+ ![]() O2(g)=2CO2(g)+3H2O(g) △H=-1558.3 kJ /mol。
O2(g)=2CO2(g)+3H2O(g) △H=-1558.3 kJ /mol。
故答案为:C2H6(g)+ ![]() O2(g)=2CO2(g)+3H2O(g) △H=-1558.3 kJ /mol;
O2(g)=2CO2(g)+3H2O(g) △H=-1558.3 kJ /mol;
(4)20.0g NaOH的物质的量为0.5mol, 则表示该反应的热化学方程式为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.4kJ /mol。
故答案为:NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.4kJ /mol。


科目:高中化学 来源: 题型:
【题目】NiSO4·xH2O是一种绿色易溶于水的晶体,广泛用于镀镍、电池等,可由电镀废渣(除镍外,还含有铜、锌、铁等元素)为原料获得.操作步骤如图:

(1)在待镀件上镀镍时,待镀件应作____极,电镀过程中电解质溶液浓度___ (填“增大”、“减小”、“不变”)
(2)向滤液Ⅰ中加入FeS是为了除去Cu2+、Zn2+等杂质,则除去Cu2+的离子方程式为_____________.当Zn2+恰好沉淀完全时,在CuS、ZnS共存的混合液中c(Zn2+)=10﹣5mol/L,则c(Cu2+)=______mol/L(已知Ksp(CuS)=1.3×10﹣36,Ksp(ZnS)=1.6×10﹣24).
(3)对滤液Ⅱ中先加H2O2再调pH,调pH的目的是______________________________________________________________________.
(4)为测定NiSO4·xH2O晶体x的值,称取26.3g晶体加热至充全失去结晶水,剩余固体15.5g,则x的值等于__________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在3种不同条件下,分别向容积为2L的恒容密闭容器中充入2molA和1molB,发生反应:![]()
![]() 。相关条件和数据见下表:
。相关条件和数据见下表:
实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
反应温度/℃ | 700 | 700 | 750 |
达平衡时间/min | 40 | 5 | 30 |
n(D)平衡/mol | 1.5 | 1.5 | 1 |
化学平衡常数 | K1 | K2 | K3 |
下列说法正确的是( )
A. 实验Ⅲ达平衡后,恒温下再向容器中通入1molA和1molD,平衡不移动
B. 升高温度能加快反应速率的原理是降低了活化能,使活化分子百分数提高
C. 实验Ⅲ达平衡后容器内的压强是实验Ⅰ的0.9倍
D. K3>K2>K1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷(As)与氮同一主族,As原子比N原子多两个电子层。可以形成As2S3、As2O5、H3AsO3、H3AsO4,等化合物,有着广泛的用途。回答下列问题:
(1)As的原子序数为______________________。
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式____________。该反应需要在加压下进行,原因是___________。
(3)己知:As(s)+![]() H2(g)+2O2(g)=H3AsO4(s)
H2(g)+2O2(g)=H3AsO4(s) ![]()
H2(g)+![]() O2(g)=H2O(l)
O2(g)=H2O(l) ![]()
2As(s)+![]() O2(g)=As2O5(s)
O2(g)=As2O5(s) ![]()
则反应As2O5(s)+3 H2O(l)=2 H3AsO4(s)的![]() =______________________。
=______________________。
(4)298K肘,将2OmL 3xmol·L-1 Na3AsO3、20m L3xmol·L-1 I2和20 mL NaOH溶液混合,发生反应:AsO33-(aq)+I2(aq)+2OH-![]() AsO43-(aq) +2I-(aq)+H2O(l)。溶液中c(AsO43-)与反应时间(t)的关系如图所示。
AsO43-(aq) +2I-(aq)+H2O(l)。溶液中c(AsO43-)与反应时间(t)的关系如图所示。

①下列可判断反应达到平衡的是_____(填标号)。
a.v(I-)=2v(AsO33-) b.溶液的pH不再变化
c.c(I-)=ymol·L-1 d.c(AsO43-)/c(AsO33-)不再变化
②tm时,v正____v逆(填“大于”、“小于”或“等于”)。
③) tm时v逆____tn时v逆(填“大于”、“小于”或“等于”),理由是___________。
④若平衡时溶液的pH=14,则该反应的平衡常数为_____(用x、y表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机反应属于加成反应的是 ( )
A. CH4 + Cl2![]() CH3Cl + HCl
CH3Cl + HCl
B. 2CH3CH3+5O2![]() 2CO2+6H2O
2CO2+6H2O
C. ![]()
D. 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化合物2苯基丙烯(![]() ),下列说法正确的是
),下列说法正确的是
A. 不能使稀高锰酸钾溶液褪色
B. 可以发生加成聚合反应
C. 分子中所有原子共平面
D. 易溶于水及甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M、N、Q的转化关系为:
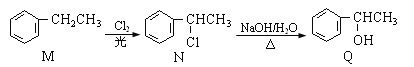
下列说法正确的是( )
A.M分子中的所有原子均在同一平面
B.上述两步反应依次属于加成反应和取代反应
C.M的同分异构体中属于芳香烃的还有3种
D.Q与乙醇互为同系物,且均能使酸性KMnO4溶液褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com