
| ||
| ||



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
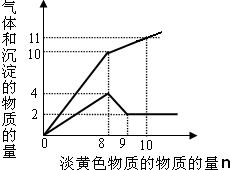 ij��Һ��ֻ���ܺ���Fe2+��Mg2+��Cu2+��NH4+��Al3+��Cl-��OH-��CO32-��������һ�ֵ���ɫ���岢����ʱ���д̼�������ų��Ͱ�ɫ�������������뵭��ɫ��������ʵ����������꣩�������ij����Ͳ�����������ʵ����������꣩�Ĺ�ϵ��ͼ��ʾ���õ���ɫ��������ɫ��Ӧʵ���Ի�ɫ����֪��Һ�к��е�������
ij��Һ��ֻ���ܺ���Fe2+��Mg2+��Cu2+��NH4+��Al3+��Cl-��OH-��CO32-��������һ�ֵ���ɫ���岢����ʱ���д̼�������ų��Ͱ�ɫ�������������뵭��ɫ��������ʵ����������꣩�������ij����Ͳ�����������ʵ����������꣩�Ĺ�ϵ��ͼ��ʾ���õ���ɫ��������ɫ��Ӧʵ���Ի�ɫ����֪��Һ�к��е��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ϩʹ��ˮ��ɫ |
| B����֬��������Ӧ |
| C��±������ˮ�ⷴӦ |
| D��������Ҵ�����������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������Na2CO3��NaHCO3�ֱ���������ϡ���ᷴӦ��NaHCO3������CO2�� |
| B����������Na2CO3��NaHCO3�ֱ���������ͬ�����ᷴӦ��NaHCO3��Ӧ�������ĵ������ |
| C����NaHCO3��Һ�е���Ba��OH��2��Һ��������Na2CO3��Һ�м���Ba��OH��2��Һ���ְ�ɫ���� |
| D��Na2CO3��NaHCO3����������������NaOH��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
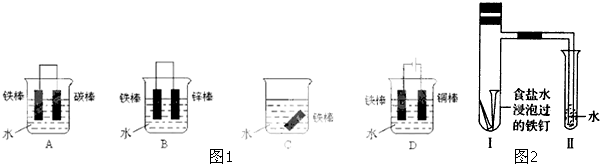
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ba2+��Na+��I-��ClO- |
| B��Mg2+��Cl-��Al3+��SO42- |
| C��K+��Cl-��HCO3-��NO3- |
| D��Ca2+��Na+��Fe3+��AlO2- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����2H2��g��+O2��g��=2H2O��g����H=-483.6kJ?mol-1����H2ȼ����Ϊ241.8kJ?mol-1 |
| B����ϡ��Һ�У�H+��aq��+OH-��aq���TH2O��l����H=-57.3kJ/mol��������0.6molH2SO4��ϡ�����뺬1molNaOH����Һ��ϣ��ų�����������57.3kJ |
| C����֪C��ʯī��s���TC�����ʯ��s����H��0������ʯ��ʯī�ȶ� |
| D����BaSO4��s��+4C��s��=4CO��g��+BaS��s����H1=+571.2kJ?mol-1�� BaSO4��s��+2C��s��=2CO2��g��+BaS��s����H2=+226.2kJ?mol-1�ڿɵ÷�ӦC��s��+CO2��g��=2CO��g�� �ġ�H=+172.5kJ?mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��12 g���ʯ������ϩ��C60���Ļ�����к���NA��̼ԭ�� |
| B��2 molCH4��Ħ��������32 g?mol-1 |
| C����״����2.24 L H2O�к���0.1 NA����ԭ�� |
| D��4 g NaOH�ܽ���100 mLˮ�����1 mol?L-1NaOH��Һ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com