
【题目】要使溶液中的Ag+、Mg2+、Ba2+三种离子逐一形成沉淀析出,选择的试剂及加入的顺序正确的是( )
A. NaOH―→NaCl―→Na2CO3
B. NaCl―→Na2CO3―→NaOH
C. HCl―→Na2CO3―→NaOH
D. NaCl―→NaOH―→Na2CO3
科目:高中化学 来源: 题型:
【题目】下列无色溶液中,能大量共存的离子组是( )
A. SO42-、Cl-、Na+、Cu2+ B. CO32-、Na +、Ba2+、H+
C. CO32-、Na +、Cl-、HCO3- D. HCO3-、Na+、CO32-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为V(甲)∶V(乙)=1∶2,则加入铝粉质量为( )
A.5.4 g B.3.6 g C.2.7 g D.1.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分离物质的方法中,不正确的是( )
A. 利用分馏的方法从石油中分离出汽油和煤油
B. 利用分液的方法将水和酒精分离
C. 利用结晶的方法除去硝酸钾中混有的少量氯化钠
D. 利用过滤的方法除去水中的泥沙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年中美专家研制出可在一分钟内完成充电的超常性能铝离子电池,分别以金属铝和石墨为电极,用A1C14-、A12C17-和有机阳离子组成电解质溶液,其放电工作原理如下图所示。下列说法不正确的是( )
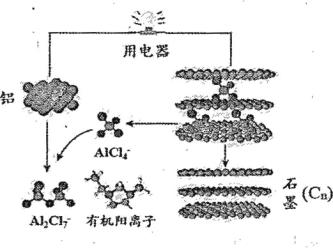
A.放电时,铝为负极、石墨为正极
B.充电时的阳极反应为:Cn+ A1C14- - e-= Cn A1C14
C.放电时的负极反应为:Al-3e- +7 A1C14-=4A12C17-
D.放电时,有机阳离子向铝电极方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将氯化钠、氯化铝、氯化亚铁、氯化铁、氯化镁五种溶液.只用一种试剂就能加以区别,这种试剂是
A.KSCN B.BaCl2 C.NaOH D.HCI
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)被称为21世纪的新型能源,它清洁、高效、具有优良的环保性能。
I.Ⅰ.工业制备二甲醚的生产流程如下:

催化反应室中(压力2.0~10.0Mpa,温度230~280℃)发生如下反应:
CO(g)+2H2(g)![]() CH3OH(g)△H=-90.7kJ/mol ①
CH3OH(g)△H=-90.7kJ/mol ①
2CH3OH(g)![]() CH3OCH3(g)+H2O(g)△H=-23.5kJ/mol ②
CH3OCH3(g)+H2O(g)△H=-23.5kJ/mol ②
CO(g)+H2O(g)![]() CO2(g)+H2(g)△H=-41.2kJ/mol ③
CO2(g)+H2(g)△H=-41.2kJ/mol ③
(1)甲烷氧化可制得合成气,反应如下:CH4(g)+![]() O2
O2![]() CO(g)+2H2(g) △H=-35.6kJ/mol。该反应是_______反应(填“自发”或“非自发”)
CO(g)+2H2(g) △H=-35.6kJ/mol。该反应是_______反应(填“自发”或“非自发”)
(2)催化反应室中总反应3CO(g)+3H2(g)![]() CH3OCH3(g)+CO2(g)的△H=______,830℃时反应③的K=1.0,则在催化反应室中反应③的K______1.0(填“>”、“<”或“=”)。
CH3OCH3(g)+CO2(g)的△H=______,830℃时反应③的K=1.0,则在催化反应室中反应③的K______1.0(填“>”、“<”或“=”)。
(3)上述反应中,可以循环使用的物质有________。
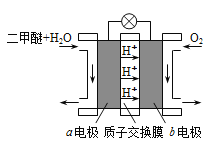
II.如图为绿色电源“二甲醚燃料电池”的工作原理示意图。b 电极是______极。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题:
(1)N2H4中N原子核外最外层达到8电子稳定结构.写出N2H4的结构式:___________.
(2)实验室用两种固体制取NH3的反应化学方程式为_____________.
(3)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为_____________.
(4)肼一空气燃料电池是一种碱性环保电池,该电池放电时,负极的反应式为_____________.
(5)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2]反应的化学方程式为2NH3(g)+CO2(g)CO(NH2)2(l)+H2O(l),该反应的平衡常数和温度关系如下:
T/℃ | 165 | 175 | 185 | 195 |
K | 111.9 | 74.1 | 50.6 | 34.8 |
①焓变△H_________0(填“>”、“<”或“=”).
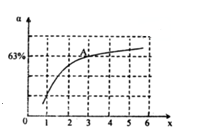
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)\frac{n(NH_{3})}{n(CO_{2})}=x,如图是氨碳比(x)与CO2平衡转化率(α)的关系.α随着x增大而增大的原因是_____________.图中A点处,NH3的平衡转化率为___________.
(6)在恒温恒容密闭容器中按照甲、乙、丙三种方式分别投料,发生反应:N2(g)+3H2(g)2NH3(g),测得甲容器中H2的平衡转化率为40%.
n(N2) | n(H2) | n(NH3) | |
甲 | 1mol | 3mol | 0mol |
乙 | 0.5mol | 1.5mol | 1mol |
丙 | 0mol | 0mol | 4mol |
①判断乙容器中反应进行的方向是_____________(填“正向或“逆向”)移动.
②达平衡时,甲、乙、丙三容器中NH3的体积分数大小顺序为_____________。
(6)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式: ,科学家利用此原理,设计成氨气一氧气燃料电池,则通入氨气的电极是
(7)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是 (填字母代号)。
4NO(g)+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是 (填字母代号)。
a.增大压强 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
(8)如果某氨水的电离程度为1%,浓度为0.01 mol/LMgCl2溶液滴加氨水至开始产生沉淀时(不考虑溶液体积变化),溶液中的NH3·H2O的浓度为 {已知Ksp[Mg(OH)2]=4.0×10-12]}
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种元素均位于周期表的前四周期,且原子序数依次增大。元素A是原子半径最小的元素;B元素基态原子的核外电子分占四个原子轨道(能级);D元素原子的已成对电子总数是未成对电子总数的3倍;E与D处于同一主族;F位于ds区,且原子的最外层只有1个电子。
(1)E+离子的电子排布式是 。
(2)B、C、D元素的第一电离能由大到小的顺序是 。
(3)B、C元素的某些氢化物的分子中均含有18个电子,则B的这种氢化物的化学式是 ;B、C的这些氢化物的沸点相差较大的主要原因是 。
(4)A、B、D可形成分子式为A2BD的某化合物,则该化合物分子中B原子的轨道杂化类型是 ;1 mol该分子中含有π键的数目是 。
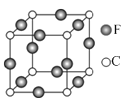
(5)C、E两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是 ,C原子的配位数是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com