
【题目】海洋是一个巨大的化学资源宝库,从海水中可制取氯、溴、碘及其化工产品。
(1)氯的原子结构示意图是___。
(2)碘在元素周期表中的位置是___。
(3)向浓缩的海水中通入Cl2,可将Br﹣转化为Br2.该反应的离子方程式是___。
(4)用热空气将上述过程中产生的Br2吹出,并用浓Na2CO3溶液吸收,生成NaBr、NaBrO3等;再将混合溶液用稀硫酸酸化得到Br2,得到Br2的离子方程式是___。
【答案】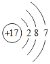 第五周期ⅦA族 2Br﹣+Cl2=Br2+2Cl- 5Br﹣+BrO3﹣+6H+=3Br2+3H2O
第五周期ⅦA族 2Br﹣+Cl2=Br2+2Cl- 5Br﹣+BrO3﹣+6H+=3Br2+3H2O
【解析】
(1)Cl原子核外电子数为17,有3个电子层,各层电子数为2、8、7,原子结构示意图为: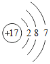 ,故答案为:
,故答案为: ;
;
(2)I原子核外有5个电子层、最外层电子数为7,处于周期表中第五周期ⅦA族,故答案为:第五周期ⅦA族;
(3)Cl2将Br﹣氧化为Br2,自身被还原为Cl﹣,反应离子方程式为:2Br﹣+Cl2=Br2+2Cl﹣,故答案为:2Br﹣+Cl2=Br2+2Cl﹣;
(4)Br﹣、BrO3﹣在酸性条件下发生反应生成Br2,根据元素守恒可知还生成H2O,反应离子方程式为:5Br﹣+BrO3﹣+6H+=3Br2+3H2O,故答案为:5Br﹣+BrO3﹣+6H+=3Br2+3H2O。


科目:高中化学 来源: 题型:
【题目】下列说法合理的是
①根据纯净物中是否含氧元素,来判断是否属于氧化物
②根据电泳现象可证明胶体带电荷
③直径介于lnm~l00nm之间的微粒称为胶体
④金属氧化物都是碱性氧化物
⑤根据分散系的稳定性将分散系分为胶体、溶液和浊液
⑥同一钢笔使用不同牌号的墨水容易堵塞,是由于胶体的聚沉
A. 只有⑥ B. 只有②⑥ C. 只有③④⑤ D. 只有①②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B的结构简式如下:

(1)A分子中含有的官能团的名称是____________________________________。
(2)A、B能否与NaOH溶液反应:A________(填“能”或“不能”,下同),B________。
(3)A在浓硫酸作用下加热可得到B,其反应类型是____________________。
(4)A、B各1 mol分别加入足量溴水,完全反应后消耗单质溴的物质的量分别是________mol、________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过卤素间的反应实验,可以比较出卤素单质氧化性的强弱。实验如下:

下列说法不正确的是
A. CCl4起到萃取、富集I2的作用
B. a中下层变无色,说明I2 转化为I-
C. Ⅲ中发生反应的离子方程式为:Br2 + 2I-=== I2 + 2Br-
D. 依据a、b中现象,可以证明Cl2的氧化性比 Br2强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三个密闭容器中分别充入N2、H2、O2三种气体,以下各种情况下排序正确的是( )
A. 当它们的温度和压强均相同时,三种气体的密度:ρ(H2)>ρ(N2)>ρ(O2)
B. 当它们的温度和密度都相同时,三种气体的压强:p(H2)>p(N2)>p(O2)
C. 当它们的质量和温度、压强均相同时,三种气体的体积:V(O2)>V(N2)>V(H2)
D. 当它们的压强和体积、温度均相同时,三种气体的质量:m(H2)>m(N2)>m(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某工业废水中含有大量FeSO4,较多的CuSO4, 以及部分污泥,通过下列流程可从该废水中回收FeSO4·7H2O晶体及金属Cu。
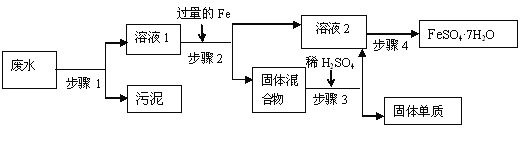
(1)步骤1的主要操作是______,(填操作名称)需用到的玻璃仪器除烧杯外还有_______。
(2)步骤2中发生反应的化学方程式为___________
(3)步骤3中发生反应的化学方程式为_______
(4)步骤4中涉及的操作是:蒸发浓缩、________、过滤、洗涤、烘干。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有25 mL 2 mol·L-1Na2CO3和75 mL 1 mol·L-1的稀盐酸:①将Na2CO3溶液缓缓滴到稀盐酸中 ②将稀盐酸缓缓滴到Na2CO3溶液中,在标准状况下产生气体的体积情况( )
A.均为0.84 L
B.均为0.56 L
C.①>②
D.②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中,反应aA(g)![]() bB(g)达平衡后,保持温度不变,将容器体积增加一倍,将达到新的平衡时,B的浓度是原来的60%,则
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,将达到新的平衡时,B的浓度是原来的60%,则
A.平衡向逆反应方向移动了
B.物质A的转化率减小了
C.物质B的质量分数增加了
D.a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲用18.4mol·L-1的浓硫酸配制250 mL 0.2 mol·L-1的硫酸溶液,完成下列问题:
(1)所需的主要仪器有__________________________________________________。
(2)根据计算,所取18.4mol·L-1的浓硫酸的体积为________mL,稀释浓硫酸的正确操作方法是____________________________________________________________。
(3)下列操作会使所配制硫酸浓度偏低的是________。
A.转移溶液时未洗涤烧杯与玻璃棒
B.容量瓶水洗后未干燥
C.定容时加水越过刻度线
D.定容时仰视刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com