
选考【化学-选修有机化学基础】(15分)
H是一种新型香料的主要成分之一,其结构中含有三个六元环。H的合成路线如下(部分产物和部分反应条件略去):

已知:
①B中核磁共振氢谱图显示分子中有6种不同环境的氢原子。
②
③D和G是同系物
请回答下列问题:
(1)用系统命名法命名(CH3)2C=CH2 : 。
(2)A→B反应过程中涉及的反应类型有 。
(3)写出D分子中含有的官能团名称: 。
(4)写出生成F与足量氢氧化钠溶液在加热条件下反应的化学方程式: 。
(5)写出E在铜催化下与O2反应生成物的结构简式: 。
(6)同时满足下列条件:①与FeCl3溶液发生显色反应;②能发生水解反应;③苯环上有两个取代基的G的同分异构体有 种(不包括立体异构),其中核磁共振氢谱为5组峰的为 (写结构简式)。
(1)2—甲基—1—丙烯(1分,甲基丙烯,2—甲基丙烯也可,异丁烯不给分。)
(2)取代反应,加成反应。(各1分,共2分。只写取代、加成不给分。)
(3)羟基,羧基。(各1分,共2分,错别字不给分。)
(4)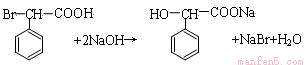 (3分)
(3分)
(5)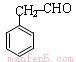 (3分)(6)9,(2分)
(3分)(6)9,(2分) 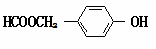 (2分)
(2分)
【解析】
试题分析:根据已知信息②可知苯乙烯与2—甲基—1—丙烯反应生成A,A在高温下与氯气发生取代反应生成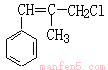 ,则A的结构简式为
,则A的结构简式为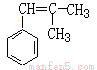 。
。 与氯化氢发生加成反应生成B,由于B中核磁共振氢谱图显示分子中有6种不同环境的氢原子,则B的结构简式为
与氯化氢发生加成反应生成B,由于B中核磁共振氢谱图显示分子中有6种不同环境的氢原子,则B的结构简式为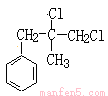 。B在氢氧化钠溶液中水解生成C,则C的结构简式为
。B在氢氧化钠溶液中水解生成C,则C的结构简式为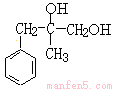 。C发生氧化反应生成D,则D的结构简式为
。C发生氧化反应生成D,则D的结构简式为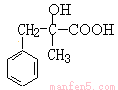 。苯乙烯与水发生加成反应生成E,E氧化生成C8H8O2,这说明羟基被氧化为羧基,则E的结构简式为
。苯乙烯与水发生加成反应生成E,E氧化生成C8H8O2,这说明羟基被氧化为羧基,则E的结构简式为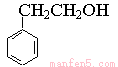 。苯乙酸与溴发生取代反应生成F,F水解生成G,D和G是同系物,所以F和G的结构简式分别是
。苯乙酸与溴发生取代反应生成F,F水解生成G,D和G是同系物,所以F和G的结构简式分别是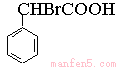 、
、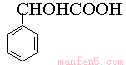 。H结构中含有三个六元环,这说明D和G通过酯化反应生成H。
。H结构中含有三个六元环,这说明D和G通过酯化反应生成H。
(1)用系统命名法命名(CH3)2C=CH2的名称为2—甲基—1—丙烯。
(2)根据以上分析可知A→B反应过程中涉及的反应类型有取代反应和加成反应。
(3)根据D的结构简式可知D分子中含有的官能团名称羟基,羧基。
(4)F与足量氢氧化钠溶液在加热条件下反应的化学方程式为 。
。
(5)苯乙醇在铜催化下与O2反应生成苯乙醛,则生成物的结构简式为 。
。
(6)①与FeCl3溶液发生显色反应,说明含有酚羟基;②能发生水解反应,说明含有酯基;③苯环上有两个取代基,则两个取代基可以是—OH与—OOCCH3、—OH与—CH3OOCH、—OH与—COOCH3,在苯环上的位置均有邻间对三种,共计是9种。其中核磁共振氢谱为5组峰的为 。
。
考点:考查有机物推断、反应类型、官能团、同分异构体判断以及方程式书写等
考点分析: 考点1:有机化学知识综合应用 试题属性

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源:2014-2015学年山东省烟台市高三下学期一模诊断测试理科综合化学试卷(解析版) 题型:实验题
(19分)过氧化钙是一种重要的化工原料,温度在350℃以上容易分解。
(1)利用反应Ca(s)+O2 CaO2(s),在纯氧条件下,制取CaO2的装置示意图如下:
CaO2(s),在纯氧条件下,制取CaO2的装置示意图如下:

请回答下列问题:
①装置A中反应的化学方程式为____________;仪器a的名称为__________;装置D中盛有的液体是浓硫酸,其作用一是观察氧气的流速,判断氧气通入是否过快及氧气与钙反应进行的程度;二是_______________。仪器安装后应进行的实验操作:
a.通入氧气
b.检查装置气密性
c.加入药品
d.停止通氧气
e.点燃酒精灯
f.熄灭酒精灯
g.冷却至室温,
正确的操作顺序为________。
②完全反应后,有关数据记录如下:
空瓷舟质量m0/g | 瓷舟与钙的质量m1/g | 瓷舟与产物的质量m2/g |
14.80 | 15.08 | 15.25 |
据此可判断m2与理论值不符,则产物中的杂质可能是_________________________。
(2)利用反应Ca2++H2O2+2NH3·H2O+6H2O=CaO2·8H2O+2NH4+,在碱性环境中,制取CaO2的流程示意图如下:

请回答下列问题:
①主反应中,NH3·H2O在Ca2+和H2O2的反应历程中所起的作用是_______________;该反应所需的条件及操作为_______(填字母)。
a.把氯化钙溶液逐滴加入过氧化氢—氨水溶液中
b.把过氧化氢—氨水溶液逐滴加入氯化钙溶液中
c.滴加时先搅拌后静置,观察晶体析出
d.滴加时不停搅拌,直至晶体完全析出
e.反应体系热水浴加热 f.反应体系冰水浴冷却
洗涤CaO2·8H2O晶体时,判断晶体是否完全洗净的试剂为_____;滤液循环使用时需在反应器中加入一种物质,该物质的化学式为_____。
②利用反应2CaO2 2CaO+O2↑测量产品中CaO2含量时,停止反应且冷却至25℃后的装置示意图如下:若直接读数确定25℃、1大气压下气体的体积,则测量结果______(填“偏大”、“偏小”或“无影响”)。
2CaO+O2↑测量产品中CaO2含量时,停止反应且冷却至25℃后的装置示意图如下:若直接读数确定25℃、1大气压下气体的体积,则测量结果______(填“偏大”、“偏小”或“无影响”)。

查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省中山市高三下学期第二次模拟考试理科综合化学试卷(解析版) 题型:选择题
用0.1mol·L—1的盐酸滴定0.1mol·L—1的氨水,在滴定过程中不可能出现的结果是
A.c(NH4+)>c(Cl-),c(OH-)>c(H+)
B.c(NH4+)=c(Cl-),c(OH-)=c(H+)
C.c(Cl-)>c(NH4+),c(OH-)>c(H+)
D.c(Cl-)>c(NH4+),c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省江门市高三3月模拟考试理科综合化学试卷(解析版) 题型:选择题
有机物在生活中的应用非常广泛。下列有关说法正确的是
A.食用植物油均可水解生成氨基酸
B.铺路用的沥青主要含有C、H、O等元素
C.做衣服的棉、麻的主要成分是纤维素
D.煤经过汽化、液化等物理变化可转化为清洁燃料
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高三下学期3月月考理综化学试卷(解析版) 题型:选择题
在恒容密闭容器中通入X并发生反应:2X(g) Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是
Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是
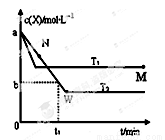
A.该反应进行到M点放出的热量大于进行到W点放出的热量
B.T2下,在0~t1时间内,v(Y)= mol/(L·min)
mol/(L·min)
C.M点的正反应速率v正大于N点的逆反应速率v逆
D.M点时再加入一定量的X,平衡后X的转化率减小
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省六校高三3月联考化学试卷(解析版) 题型:实验题
(16分)某研究性学习小组将一定浓度的Na2CO3溶液滴入MgSO4溶液中得到白色沉淀。甲同学认为两者反应只生成MgCO3一种沉淀;乙同学认为这两者相互促进水解,只生成Mg(OH)2一种沉淀;丙同学认为生成MgCO3和Mg(OH)2两种沉淀。(查阅资料知:MgCO3和Mg(OH)2均不带结晶水)
(1)按照乙同学的理解Na2CO3溶液和MgSO4溶液反应的化学反应方程式为__ _____;
在探究沉淀物成分前,须将沉淀从溶液中分离并净化。具体操作为①过滤②洗涤③干燥。
(2)请用下图所示装置,选择合适的实验装置和必要的试剂,证明沉淀物中只有碳酸镁。

各装置连接顺序为__________________(用装置编号表示);
②装置C中装有试剂的名称是______________;
③能证明生成物中只有MgCO3的实验现象是 _______。
(3)若Mg(OH)2和MgCO3两者都有,可通过下列所示装置的连接,进行定量分析来测定其组成。

实验结束时通入过量的空气的作用________________ 。
A装置和E装置的共同作用是__________________________。
实验过程中测定的数据有:W1:样品的质量,W2:反应后装置B中残渣的质量,W3:反应生成水的质量,W4:反应生成二氧化碳的质量,为了测定其组成,至少需要其中 个数据,请将可能的组合填入下表中(每个空格中填一种组合,至少填5个)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省六校高三3月联考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.电解法精炼铜,当阴极质量增加32 g时,一定有6.02×1023个电子转移
B.含10.6 g Na2CO3的溶液中,所含阴离子总数等于6.02×1022
C.28 g由乙烯和氮气组成的混合气体中,含有6.02×1023个原子
D.含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为6.02×1022
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省七市教科研协作体高三3月联考化学试卷(解析版) 题型:实验题
二氧化氯(ClO2)为一种黄绿色气体,是一种高效、广谱、安全的杀菌、消毒剂。制备ClO2的方法有多种。
(1)纤维素还原法制ClO2。其原理是:纤维素水解得到的最终产物A与NaClO3反应生成ClO2。完成反应的化学方程式:其流程如下:□ (A) +□NaClO3+□H2SO4=□ClO2↑+□CO2↑+□H2O+□______
(2)电解食盐水制取ClO2 ,其流程如下:

①粗盐中含有Ca2+、Mg2+、SO42-等杂质。除杂操作时,往粗盐水中加入试剂的顺序依次为__________(填化学式),充分反应后将沉淀一并滤去,再加入盐酸。
②食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸在发生器中反应生成ClO2 ,写出发生器中生成ClO2的化学方程式____________________。
③上述流程中,可循环利用的物质有__________;按照绿色化学原则,电解槽阴极产生的气体与方框中物质的物质的量之比为________时,原子的利用率为100%。
(3)实验室以NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料制备ClO2的流程下如下:

已知:(I)A气体在标准状况下的密度为0.089g/L;
(Ⅱ)气体B能使湿润的红色石蕊试纸变蓝。
①电解时,发生反应的化学方程式为 。
②NCl3与NaClO2(亚氯酸钠)按物质的量之比为1∶6混合,在溶液中恰好反应生成ClO2,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省漳州市高三3月质量检查化学试卷(解析版) 题型:选择题
下列相关工业制法的描述不正确的是
A.电解熔融氯化钠制取金属钠
B.电解熔融的Al(OH) 3制取金属铝
C.用石英、纯碱、石灰石为原料制玻璃
D.用焦炭在电炉中还原二氧化硅得到含杂质的粗硅
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com