
【题目】用 NA表示阿伏加德罗常数的值。下列说法正确的是( )
A. 1 L 1 mol/L 的 CH3COOH 溶液中 CH3COO-为 NA个
B. 标况下 22.4 L NO 和 11.2 L O2 反应后,气体分子总数为 NA个
C. 1 L 0.1 mol/L 的 Na2SO3 溶液中离子总数大于 0.3NA
D. H2和 O2反应生成 NA个 H2O(l)和 NA个 H2O(g)放出热量相等
【答案】C
【解析】
A. CH3COOH属于弱电解质,在水中部分发生电离,因此1 L 1 mol/L 的 CH3COOH 溶液中 CH3COO-个数小于NA个,A错误;
B. 标准状况下,22.4 L NO是1mol,11.2 L O2是0.5mol,二者混合生成1molNO2,但由于存在2NO2![]() N2O4,所以所得气体的分子数目小于NA,B错误;
N2O4,所以所得气体的分子数目小于NA,B错误;
C. Na2SO3溶液中存在水解平衡:SO32-+H2O![]() HSO3-+OH-,HSO3-+ H2O=
HSO3-+OH-,HSO3-+ H2O=![]() H2SO3+ OH-,从水解的原理可知,1个SO32-水解后生成1个HSO3-和1个OH-,溶液中阴离子数目增加,所以1 L 0.1 mol/L 的 Na2SO3 溶液中离子总数大于 0.3NA,C正确;
H2SO3+ OH-,从水解的原理可知,1个SO32-水解后生成1个HSO3-和1个OH-,溶液中阴离子数目增加,所以1 L 0.1 mol/L 的 Na2SO3 溶液中离子总数大于 0.3NA,C正确;
D. 由于H2O(l)= H2O(g) H>0,所以H2 和 O2 反应生成 NA 个 H2O(l)和 NA 个 H2O(g)放出热量不相等,生成NA 个 H2O(l) 放出的热量多,D错误;
综上所述,本题选C。


科目:高中化学 来源: 题型:
【题目】CH4超干重整CO2技术可得到富含CO的化工原料。回答下列问题:
(1)CH4超干重整CO2的催化转化如图所示:
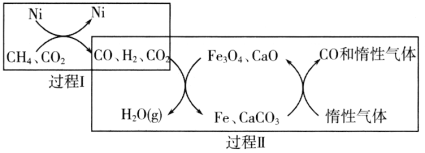
①已知相关反应的能量变化如图所示:

过程Ⅰ的热化学方程式为________。
②关于上述过程Ⅱ的说法不正确的是________(填序号)。
a.实现了含碳物质与含氢物质的分离
b.可表示为CO2+H2=H2O(g)+CO
c.CO未参与反应
d.Fe3O4、CaO为催化剂,降低了反应的ΔH
③其他条件不变,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,反应CH4(g)+CO2(g)=2CO(g)+2H2(g)进行相同时间后,CH4的转化率随反应温度的变化如图所示。a点所代表的状态________(填“是”或“不是”)平衡状态;b点CH4的转化率高于c点,原因是________。
(2)在一刚性密闭容器中,CH4和CO2的分压分别为20kPa、25kPa,加入Ni/α-Al2O3催化剂并加热至1123K使其发生反应CH4(g)+CO2(g)=2CO(g)+2H2(g)。

①研究表明CO的生成速率υ(CO)=1.3×10-2·p(CH4)·p(CO2)mol·g-1·s-1,某时刻测得p(CO)=20kPa,则p(CO2)=________kPa,υ(CO)=________mol·g-1·s-1。
②达到平衡后测得体系压强是起始时的1.8倍,则该反应的平衡常数的计算式为Kp=________(kPa)2。(用各物质的分压代替物质的量浓度计算)
(3)CH4超干重整CO2得到的CO经偶联反应可制得草酸(H2C2O4)。常温下,向某浓度的草酸溶液中加入一定浓度的NaOH溶液,所得溶液中![]() ,则此时溶液的pH=________。(已知常温下H2C2O4的Ka1=6×10-2,Ka2=6×10-5,lg6=0.8)
,则此时溶液的pH=________。(已知常温下H2C2O4的Ka1=6×10-2,Ka2=6×10-5,lg6=0.8)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下述装置制取氯气,并用氯气进行下列实验。看图回答下列问题:
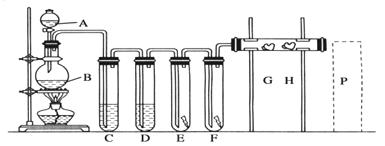
![]() 仪器的名称: ________。B中发生反应的化学方程式为____________。
仪器的名称: ________。B中发生反应的化学方程式为____________。
![]() 为了获得纯净干燥的氯气, C、D中应分别放入的试剂C为_________,作用是________________________;D中为___________。
为了获得纯净干燥的氯气, C、D中应分别放入的试剂C为_________,作用是________________________;D中为___________。
![]() 中为红色干布条,F中为红色湿布条,可观察到有色布条褪色的是______
中为红色干布条,F中为红色湿布条,可观察到有色布条褪色的是______![]() 填E或
填E或![]()
![]() 是浸有淀粉KI溶液的棉花球,G处现象是棉花球表面变成__________,H是浸有NaBr溶液的棉花球,H处发生的离子方程式为_________________。
是浸有淀粉KI溶液的棉花球,G处现象是棉花球表面变成__________,H是浸有NaBr溶液的棉花球,H处发生的离子方程式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知五种短周期元素aX、bY、cZ、dR、eW存在如下关系:① X、Y同主族,R、W同主族 ②![]() ;a+b=
;a+b=![]() (d+e);
(d+e);![]() =c-d,下列有关说法不正确的是
=c-d,下列有关说法不正确的是
A.原子半径比较:r(W)>r(Z)>r(Y) >r(R)
B.X和Y形成的化合物中,阴阳离子的电子层相差1层
C.W的最低价单核阴离子的失电子能力比R的强
D.Z、Y最高价氧化物对应的水化物之间可以相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚是一种绿色、可再生的新能源。如图是绿色电源“二甲醚燃料电池”的工作原理示意图(a、b均为多孔性Pt电极)。该电池工作时,下列说法正确的是( )

A. a电极为该电池正极
B. O2在b电极上得电子,被氧化
C. 电池工作时,a电极反应式:CH3OCH3-12e-+3H2O===2CO2↑+12H+
D. 电池工作时,燃料电池内部H+从b电极移向a电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CO2(g) + 3H2(g)![]() CH3OH(g) + H2O(g) ΔH =-49.0 kJmol-1。一定条件下,向体积为1 L的密闭容器中充入1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如右图所示。下列叙述中,正确的是 ( )
CH3OH(g) + H2O(g) ΔH =-49.0 kJmol-1。一定条件下,向体积为1 L的密闭容器中充入1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如右图所示。下列叙述中,正确的是 ( )

A. 升高温度能使![]() 增大
增大
B. 反应达到平衡状态时,CO2的平衡转化率为75%
C. 3 min时,用CO2的浓度表示的正反应速率等于用CH3OH的浓度表示的逆反应速率
D. 从反应开始到平衡,H2的平均反应速率υ(H2)=0.075 molL-1min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知断裂1molH2(g)中的H—H键需吸收436kJ 能量,断裂1molO2中的共价键需吸收496kJ能量,且氢气在氧气中燃烧的能量变化如图所示。下列说法正确的是
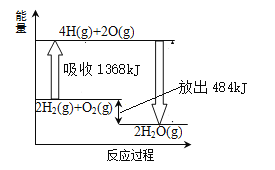
A.H2O(g)=H2(g)+1/2O2(l) △H=+242kJ/mol
B.H2(g)+1/2O2(g)= H2O(l) △H<-242kJ/mol
C.形成1molH2O(g)中的化学键需吸收926kJ
D.2H2(g)+ O2 (g)= 2H2O (g) △H=-1852kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A是石油裂解气的主要产物之一,其产量常用于衡量一个国家石油化工发展水平的标志。下列是有机物 A~G之间的转化关系:
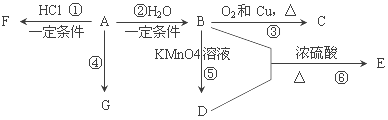
请回答下列问题:
(1)A的官能团的名称是_________;C的结构简式是_____;
(2)B是一种具有特殊香味的液体,由A→B的反应方程式为_____,该反应类型是_____;
(3)G 是一种高分子化合物,其结构简式是_____;
(4)比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射物质F(沸点12.27°C)进行应急处理。写出由A制F的化学反应方程式_____。
(5)D的结构简式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com