
【题目】正己烷是优良的有机溶剂,其球棍模型为![]() ,下列有关说法正确的是( )
,下列有关说法正确的是( )
A.正己烷的分子式为![]()
B.正己烷的一氯代物有3种
C.正己烷能与溴发生取代反应而使溴水褪色
D.主链上含有4个碳原子的正己烷的同分异构体只有1种
 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:
【题目】短周期元素D、E、X、Y、Z原子序数逐渐增大。它们的最简氢化物分子的空间构型依次是正四面体、三角锥形、正四面体、角形(V形)、直线形。回答下列问题:
(1)Y的最高价氧化物的化学式为________;Z的核外电子排布式是________;
(2)D的最高价氧化物与E的一种氧化物为等电子体,写出E的氧化物的化学式________;
(3)D和Y形成的化合物,其分子的空间构型为________;D原子的轨道杂化方式是________;
(4)金属镁和E的单质在高温下反应得到的产物与水反应生成两种碱性物质,该反应的化学方程式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯腈(CH2=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2=CHCHO)和乙腈(CH3CN)等,回答下列问题:
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的热化学方程式如下:
①C3H6(g)+NH3(g)+![]() O2(g)=C3H3N(g)+3H2O(g) ΔH=-515kJ/mol
O2(g)=C3H3N(g)+3H2O(g) ΔH=-515kJ/mol
①C3H6(g)+O2(g)=C3H4O(g)+H2O(g) ΔH=-353kJ/mol
两个反应在热力学上趋势均很大,其原因是________;有利于提高丙烯腈平衡产率的反应条件是________;提高丙烯腈反应选择性的关键因素是________。
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应温度为460℃。低于460℃时,丙烯腈的产率________(填“是”或者“不是”)对应温度下的平衡产率,判断理由是________;高于460℃时,丙烯腈产率降低的可能原因是________(双选,填标号)
A.催化剂活性降低B.平衡常数变大C.副反应增多D.反应活化能增大
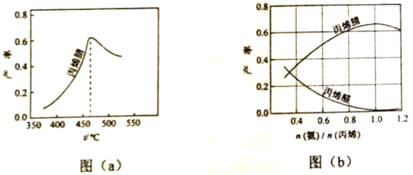
(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示。由图可知,最佳n(氨)/n(丙烯)约为1理由是_______________。进料氨、空气、丙烯的理论体积约为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三元电池成为2018年我国电动汽车的新能源,其电极材料可表示为![]() ,且x+y+z=1.充电时电池总反应为LiNixCoyMnzO2+6C(石墨)=Li1-aNixCoyMnzO2+LiaC6,其电池工作原理如图所示,两极之间有一个允许特定的离子X通过的隔膜。下列说法正确的是
,且x+y+z=1.充电时电池总反应为LiNixCoyMnzO2+6C(石墨)=Li1-aNixCoyMnzO2+LiaC6,其电池工作原理如图所示,两极之间有一个允许特定的离子X通过的隔膜。下列说法正确的是
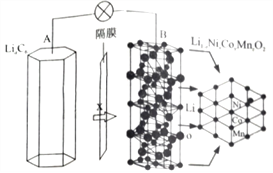
A. 允许离子X通过的隔膜属于阴离子交换膜
B. 充电时,A 为阴极,Li+被氧化
C. 可从无法充电的废旧电池的石墨电极中回收金属锂
D. 放电时,正极反应式为 Li1-aNixCoyMnzO2+aLi ++ae-= LiNixCoyMnzO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四苯基乙烯(TPE)及其衍生物具有诱导发光特性,在光电材料等领域应用前景广泛。以下是TPE的两条合成路线(部分试剂及反应条件省略):
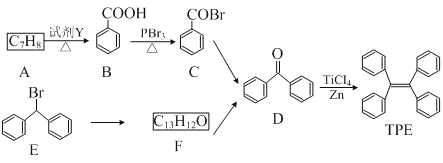
(1)A的名称是__________________;试剂Y为____________________。
(2)B→C的反应类型为_______________;B中官能团的名称是_________________,D中官能团的名称是_______________。
(3)E→F的化学方程式是______________________________________。
(4)W是D的同分异构体,具有下列结构特征:①属于萘(![]() )的一元取代物;②存在羟甲基(-CH2OH)。写出W所有可能的结构简式:______________________。
)的一元取代物;②存在羟甲基(-CH2OH)。写出W所有可能的结构简式:______________________。
(5)下列叙述正确的是______。
a. B的酸性比苯酚强
b. D不能发生还原反应
c. E含有3种不同化学环境的氢
d. TPE既属于芳香烃也属于烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三种物质均含有同一种中学常见元素X,其转化关系如下,下列说法不正确的是
![]()
A.若A为硝酸,X为金属元素,则甲与丙反应可生成乙
B.若乙为NaHCO3,则丙一定是CO2
C.若A为NaOH溶液,X为短周期的金属元素,则乙一定为白色沉淀
D.若A为金属单质,乙的水溶液遇KSCN溶液变红,则甲可能为非金属单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)实验室用图甲装置制备SO3并测定SO2催化氧化为SO3的转化率。
已知:SO3熔点为16.8℃,沸点为44.8℃,假设气体进入装置可以被完全吸收,不考虑空气的影响。

(1)A中使用浓硫酸的质量分数为70%的原因是___,B中浓H2SO4的作用是___。
(2)当实验停止通入SO2,熄灭酒精灯后,还需要继续通一段时间的氧气,其目的是___。
(3)实验结束后测得装置D增加了ag,装置E中的沉淀洗涤烘干后其质量为bg。则E中的沉淀的化学成分是___(填写化学式),本实验中SO2转化率为___(用代数式表示,不用化简)。
(二)SO3溶于浓硫酸后可得到发烟硫酸,工业上把干燥的氯化氢气体通入到发烟硫酸中可以得到HSO3Cl。HSO3Cl是一种无色液体,沸点为152℃,有强腐蚀性,遇湿空气产生强烈的白雾。现用图乙所示的装置制取HSO3Cl(夹持及加热装置略去)。

(1)HSO3Cl遇湿空气产生强烈的白雾,请结合用化学方程式解释其原因___。
(2)分液漏斗下方接的毛细管,其作用是___;若不用毛细管而直接用分液漏斗注入浓盐酸,可能发生的现象是___。
(3)装置F的作用是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl3、FeCl2和CuCl2的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法中,不正确的是
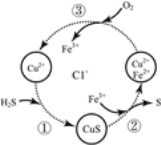
A.过程①中,没有化合价的变化
B.过程②中,发生反应为S2-+Fe3+=S+Fe2+
C.过程③中,Fe2+作还原剂
D.整个转化过程中Fe3+可以循环使用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,在500℃时发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H<0。CH3OH的浓度随时间变化如图所示,下列说法不正确的是
CH3OH(g)+H2O(g) △H<0。CH3OH的浓度随时间变化如图所示,下列说法不正确的是

A.从反应开始到10min时,H2的平均反应速率v(H2)=0.15 mol/(L·min)
B.从20min到25min达到新的平衡,可能是增大压强
C.其他条件不变,将温度升到700℃,再次达平衡时平衡常数减小
D.从开始到25min,CO2的转化率是70%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com