
【题目】I.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学们分别设计了如图甲、乙所示的实验装置。请回答相关问题:

(1)定性甲所示装置可通过观察___,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是___。
(2)定量如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为___,实验中需要测量的数据是___。
Ⅱ.以下是某研究小组探究影响反应速率部分因素的相关实验数据。
实验序号 | H2O2溶液浓度/% | H2O2溶液体积/mL | 温度/℃ | MnO2的用量/g | 收集O2的体积/mL | 反应所需时间/s |
① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
③ | 30 | 5 | 35 | 2 | 49.21 | |
④ | 30 | 5 | 55 | 2 | 10.76 |
(1)写出实验①中H2O2分解的化学方程式___。
(2)通过实验①和②对比可知,化学反应速率与____有关;从实验③和④对比可知,化学反应速率与温度的关系是___。
【答案】反应产生气泡的快慢 控制阴离子相同,消除阴离子不同对实验的干扰 分液漏斗 产生40mL气体所需的时间 2H2O2![]() 2H2O+O2↑ 反应物浓度(或浓度) 温度越高,化学反应速率越快
2H2O+O2↑ 反应物浓度(或浓度) 温度越高,化学反应速率越快
【解析】
I.(1)双氧水分解生成水和氧气,可以根据反应生成气体的快慢来比较催化剂的催化效果;探究Fe3+和Cu2+对H2O2分解的催化效果时,必须保持其他的条件相同,据此分析解答;
(2)定量比较Fe3+和Cu2+对H2O2分解的催化效果,可以通过测定产生40mL的气体所需的时间来比较;
Ⅱ.双氧水分解得到水和氧气;根据表格中的①、②数据和③、④数据的不同点分析解答。
I.(1)双氧水分解生成水和氧气,可以根据反应生成气体的快慢来分析比较Fe3+和Cu2+对H2O2分解的催化效果;在探究Fe3+和Cu2+对H2O2分解的催化效果时,必须保持其他的条件相同,所以将FeCl3改为Fe2(SO4)3更为合理,可以避免由于阴离子不同造成的干扰,故答案为:反应产生气泡的快慢;控制阴离子相同,消除阴离子不同对实验的干扰;
(2)由图可知,A为分液漏斗;定量比较Fe3+和Cu2+对H2O2分解的催化效果,可以通过测定产生40mL的气体所需的时间来比较,产生40mL的气体所需的时间越短,则催化效果越好,故答案为:分液漏斗;收集40 mL气体所需要的时间;
Ⅱ.(1)双氧水分解得到水和氧气,反应为:2H2O2![]() 2H2O+O2↑,故答案为:2H2O2
2H2O+O2↑,故答案为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(2)从表中分析可知:①②是过氧化氢浓度不同而其他的反应条件均相同,可知这一过程是探究反应物的浓度与反应速率的关系,反应物浓度越大,反应速率越快;实验③④则是温度不同,其他条件相同,探究的是温度对化学反应速率的影响,从结果可知,温度高时反应所用的时间较短,即反应的速率较快,温度低时反应的速率较慢;故答案为:反应物浓度(或浓度);温度越高,化学反应速率越快。


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】将0.2 mol·L-1的KI溶液和0.05 mol·L-1Fe2(SO4)3溶液等体积混合后,取混合液分别完成下列实验,能说明溶液中存在化学平衡“2Fe3++2I-![]() 2Fe2++I2”的是( )
2Fe2++I2”的是( )
实验编号 | 实验操作 | 实验现象 |
① | 滴入KSCN溶液 | 溶液变红色 |
② | 滴入AgNO3溶液 | 有黄色沉淀生成 |
③ | 滴入K3[Fe(CN)6]溶液 | 有蓝色沉淀生成 |
④ | 滴入淀粉溶液 | 溶液变蓝色 |
已知:离子方程式:3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓(蓝色沉淀)
A.①B.②和④C.③和④D.①和②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R为五种短周期元素,其原子半径和最外层电子数之间的关系如下图所示。下列说法错误的是
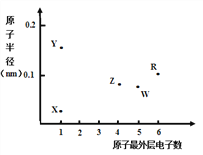
A. 简单离子半径:Y < W
B. 最高价氧化物对应水化物的酸性:Z < W
C. R为氧元素
D. X与Z可以形成正四面体结构的分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A. 向0.1mol/LCH3COOH溶液中加入少量水,溶液中c(H+)/c(CH3COOH)减小
B. 将CH3COONa溶液从20℃升温至30℃,溶液中c(CH3COO-)/c(CH3COOH)·c(OH-)增大
C. 向盐酸中加入氨水至中性,溶液中c(NH4+)/c(Cl-)>1
D. 向AgCl、AgBr的饱和溶液中加入少量硝酸银,溶液中c(Cl-)/c(Br-)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将稀HCl溶液滴加到等浓度的弱碱AOH溶液中,测得混合液的pH和![]() 的关系如图所示,其中a点表示未加盐酸时的数据,e点表示HCl和AOH恰好完全反应时的数据。下列说法错误的是( )
的关系如图所示,其中a点表示未加盐酸时的数据,e点表示HCl和AOH恰好完全反应时的数据。下列说法错误的是( )
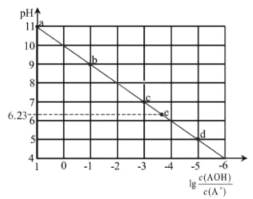
A.常温下,A+的水解平衡常数为1.0×10-10
B.点d溶液中:c(Cl-)> c(AOH)>c(A+)
C.点c 溶液中的n(A+)+n(AOH)等于点e溶液中的n(Cl-)
D.点e溶液中水电离出的H+浓度为10-6.23 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的过程是目前直接利用太阳能的研究热点。人们把通过人工光化学手段合成燃料的过程叫做人工光合作用。
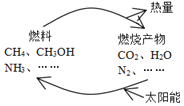
(1)在图构想的物质和能量循环中太阳能最终转化为___能;
(2)人工光合作用的途径之一就是在催化剂和光照条件下,将CO2和H2O转化为CH3OH(甲醇),该反应的化学方程式为:2CO2(g)+4H2O(g) ![]() 2CH3OH(g)+3O2(g)。
2CH3OH(g)+3O2(g)。
一定条件下,在2L密闭容器中进行上述反应,测得n(CH3OH)随时间的变化如表所示:
时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
n(CH3OH)/mol | 0.000 | 0.040 | 0.070 | 0.090 | 0.100 | 0.100 | 0.100 |
用CH3OH、H2O分别表示0~3min内该反应的平均反应速率为___mol/(L·min)-1、____mol/(L·min)-1;
②能说明该反应已达到平衡状态的是___(填序号);
A.v正(H2O)=2v逆(CO2) B.n(CH3OH)∶n(O2)=2∶3
C.容器内压强保持不变 D.容器内混合气体密度保持不变
(3)用人工光合作用得到的甲醇、氧气和稀硫酸制作燃料电池,则甲醇应通入该燃料电池的____极(填“正”或“负”),完成并配平通入氧气一极的电极反应式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设 NA 为阿伏加德罗常数的值,下列说法不正确的是
A.1mol CH4 与 Cl2 在光照下反应生成的CH3Cl分子数等于NA
B.100 g CaCO3 和 KHCO3 的固体混合物中含有的阳离子数为 NA
C.一定浓度的硫酸和镁反应,生成 11.2L(标准状况)气体,转移电子数为 NA
D.6.4g SO2 溶于水形成的酸雨中,SO2、H2SO3、HSO![]() 和 SO
和 SO![]() 的微粒数之和为 0.1NA
的微粒数之和为 0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物PH4I是一种白色晶体,受热不稳定,易分解产生PH3。PH3是无色剧毒气体, 广泛用于半导体器件和集成电路生产的外延、离子注入和掺杂。
(1)在2L真空密闭容器中加入一定量PH4I固体,T1℃ 时发生如下反应: PH4I(s) PH3(g) + HI(g)
①下列可以作为反应达到平衡的判据是_____。
A.容器内气体的压强不变
B.容器内 HI 的气体体积分数不变
C.容器内 PH4I 质量不变
D.容器内气体的密度不变
E.容器内气体的平均相对分子质量不变
②t1时刻反应达到平衡后,在t2时刻维持温度不变瞬间缩小容器体积至1L,t3时刻反应重新达到 平衡。在下图中画出t2~t4 时段的υ正、υ逆随时间变化图______。
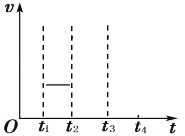
(2)PH4I固体分解产生的PH3和HI均不稳定,在一定温度下也开始分解。在2L真空密闭容器中加 入一定量PH4I固体,已知在T2℃ 时存在如下反应:
Ⅰ PH4I(s) PH3(g) + HI(g) ΔH1
Ⅱ 4 PH3(g) P4(g) + 6 H2(g) ΔH2
Ⅲ 2 HI(g) H2 (g) + I2(g) ΔH3
①已知:298K,101kPa,H-P键、P-P键、H-H键的键能分别为322 kJ·mol-1、200 kJ·mol-1、436 kJ·mol-1试计算ΔH2 =______________。
②各反应均达平衡时,测得体系中 n(PH3)=a mol ,n(P4)=b mol ,n(H2)=c mol ,则 T2℃时 反应I的平衡常数K值为___________________。(用a、b、c表示)
③维持温度不变,缩小体积增大压强,达到新的平衡后,发现其它各成分的物质的量均发生变化,而n(I2)基本不变,试解释可能原因_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2 L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。

(1)当反应进行到第_______min,该反应达到平衡。
(2)计算X的转化率______。
(3)计算反应从开始至2分钟末,Z物质的化学反应速率______。
(4)由图中所给数据进行分析,该反应的化学方程式为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com