
����Ŀ���ۺ����ú�ˮ�����Ʊ�ʳ�Ρ��������þ��������ʣ���������ͼ��ʾ�� 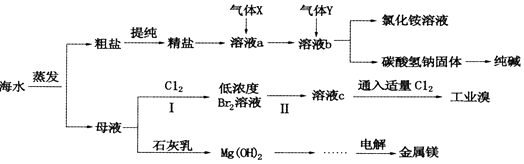
��1�����ú�ˮ���Ʊ�C12 �� Ϊ���ڴ��棬�ɽ�C12Һ����Ӧ��ȡ�Ĵ�ʩ֮һ�� ��
��2�������к��������ơ��Ȼ�þ���Ȼ��Ƶȿ��������ʣ�Ϊ��ȥ��Щ���ʶ��þ��Σ��������²��������ܽ� �ڼӹ�����BaCl2��Һ �ۼӹ�����NaOH��Һ �ܼӹ�����Na2CO3��Һ ������������ƣ���ͬ�� ������������ ��
��3������XΪ �� ��Һb�з�����Ӧ�Ļ�ѧ����ʽ�� ��
��4������I���ѻ��Br2 �� ��������ֽ�Br2��ԭΪBr�� �� ��Ŀ��Ϊ �� �������ͨ���������Br2 �� ��SO2ˮ��Һ�������գ��õ���Һc����Ӧ�����ӷ���ʽΪ �� ��ʵ�����У��ӹ�ҵ������ȡ�嵥�ʵ�ʵ����������� ��
��5����ҵ����ȡ����þ�Ļ�ѧ����ʽΪ ��
���𰸡�
��1������ �����ѹ��
��2�����ˣ������ᾧ
��3��NH3��NaCl+NH3+CO2+H2O=NaHCO3��+NH4Cl
��4��������Ԫ�أ�Br2+SO2+2H2O�T4H++SO42��+2Br������ȡ
��5��MgCl2�����ڣ� ![]() Cl2��+Mg
Cl2��+Mg
���������⣺��1�������£�����Ϊ���壬���� �����ѹ����Һ����ת��ΪҺ���������ʹ��棬���Դ��ǣ����� �����ѹ������2�������ɵ����ᱵ��̼�ᱵ��̼��ơ�������þ��������Һ�г�ȥ�ù��˵ķ������Ȼ��ƺ�����Ļ����Һ�õ��Ȼ��ƾ��壬�����������ᾧ�ķ�������ȥ��Һ�е��Ȼ����ˮ�����Դ��ǣ����ˣ������ᾧ����3����ͬ�����£��������ܽ�ȴ��ڶ�����̼��Ϊ����߶�����̼���ܽ�ȣ�����ʳ��ˮ��ͨ�백����������Һb��Ϊ�Ȼ��ƺͰ�ˮ�Ļ��Һ������XΪ������YΪ������̼��NaCl��NH3��CO2�ȷ�����Ӧ����NaHCO3��NH4Cl����ӦΪ��NaCl+NH3+CO2+H2O=NaHCO3��+NH4Cl��
���Դ��ǣ�NH3��NaCl+NH3+CO2+H2O=NaHCO3��+NH4Cl����4����������ѻ������̬����Ũ�Ⱥܵͣ����ֱ�����������ɱ��ϸߣ������ڹ�ҵ��������������ѻ������̬���壬������ֽ�֮ת��ɻ���̬���壬��Ŀ���Ǹ�����Ԫ�أ����ͳɱ����������������嵥�ʷ�����Ӧ������ǿ��HBr��H2SO4 �� ���ӷ�ӦΪ��Br2+SO2+2H2O�T4H++SO42��+2Br�� �� �����л��ܼ��е��ܽ�ȴ�����ˮ�е��ܽ�ȣ����л��ܼ���ˮ�����ܣ����Կ��Բ�����ȡ�ķ�����ȡ�壬
���Դ��ǣ�������Ԫ�أ�Br2+SO2+2H2O�T4H++SO42��+2Br������ȡ����5��������״̬�µ���Ȼ�þұ��þ����ⷴӦ����ʽΪ��MgCl2�����ڣ� ![]() Cl2��+Mg��
Cl2��+Mg��
���Դ��ǣ�MgCl2�����ڣ� ![]() Cl2��+Mg��
Cl2��+Mg��


 ����ȫ���ִʾ��ƪ��ϵ�д�
����ȫ���ִʾ��ƪ��ϵ�д� �����߿����ϵ�д�
�����߿����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ�������
�ٱ�״���£�0.2 mol�κ����ʵ������Ϊ4.48 L������1 mol��������Ϊ22.4 L������һ�����ڱ�״���¡��۱�״���£�1 L HCl��1 L H2O�����ʵ�����ͬ���ܱ�״���£�1 g H2��14 g N2�������ͬ����28 g CO�����Ϊ22.4 L�����������ʵ����ʵ�����ͬ���������ڱ�״���µ����Ҳ��ͬ������ͬ��ͬ���ʱ���������ʵ����ʵ���Խ����ѹǿԽ��ͬ��ͬѹ�£�������ܶ����������Է�������������
A. �٢ڢۢ� B. �ڢۢޢߢ� C. �ݢޢߢ� D. �ܢߢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������̬����1L������壬��ȫȼ������1.4LCO2��2.0Lˮ���������������ͬ״���²�ã����û��������ǣ� ��
A.���顢��ϩ
B.���顢��ϩ
C.���顢��ϩ
D.���顢��ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeCl3���ִ���ҵ������Ӧ�ù㷺��ij��ѧ�о���ѧϰС��ģ�ҵ�����Ʊ���ˮFeCl3�����ø���ƷFeCl3��Һ�����ж���H2S���塣
��.���������ϵ�֪����ˮFeCl3�ڿ������׳��⣬������������������Ϊ���ᡣ����������Ʊ���ˮFeCl3��ʵ�鷽����װ��ʾ��ͼ(���ȼ��г�װ����ȥ)�������������£�

�ټ���װ�õ������ԣ�
��ͨ������Cl2���Ͼ�װ���еĿ�����
���þƾ�������м�·���������Ӧ��ɣ�
�ܡ���
����ϵ��ȴ��ֹͣͨ��Cl2�����ø����N2�Ͼ�Cl2�����ռ����ܷ⡣
��ش��������⣺
��1��װ��A�з�Ӧ�Ļ�ѧ����ʽΪ_______________________________________��
��2���ڢ۲����Ⱥ����ɵ���״FeCl3�ֽ����ռ��������������ڷ�Ӧ��A�Ҷˡ�Ҫʹ������FeCl3�����ռ������ڢܲ�����Ӧ����__________________________________��
��3�����������У�Ϊ��ֹFeCl3��������ȡ�Ĵ�ʩ��(������)____________��
��4��װ��B����ˮԡ������Ϊ_______________________________________________��װ��C������Ϊ________��װ��D��FeCl2ȫ����Ӧ����ʧȥ����Cl2�����ö�ʧЧ��д������FeCl2�Ƿ�ʧЧ���Լ�_______________________________________________��
��5�������߿��л���β������װ��E��ע���Լ������ڴ���ϻ���____________
��6��FeCl3��Һ��H2S���巴Ӧ�����ӷ���ʽΪ____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���鷨�벻���ķ��ı����ʡ�ī��ֽ���⣩�������õ��Ǻ�����ī�õ�ī���Լ���ֽ������ֽ��������̨�õ���ʯ����Ҫ�ɷ������ǣ� ��
A.�����ʡ�̿�ڡ����ǡ�����
B.���ϡ�ú̿�����ǡ�����
C.���ǡ�̿�ڡ������ʡ�����
D.�����ʡ�ú̿�����ǡ��л�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС�����ʵ�飬�ⶨNa2CO3��NaHCO3�������Na2CO3������������
������
ʵ�鲽��Ϊ���ٳ���������������ΪA g �ڳ���װ����������������ΪB g �ۼ��Ȣ���ȴ�ݳ��������Ͳ����������ΪC g���ظ������ݲ�����ֱ�����أ�����ΪD g��
��1�������з�����Ӧ�Ļ�ѧ����ʽΪ ��
��2������Na2CO3�������������õ��IJⶨ����Ϊ���A������B������C����D������
�ҷ�����
����ƽ��ȷ��ȡ0.3000g��Ʒ��������ƿ�У���������ˮ�ܽ⣬����2�η�̪��Һ����0.1000mo1L��1 �� �ı�����ζ�����Һ�ɷۺ�ɫ�պñ�Ϊ��ɫ���ﵽ�ζ��յ�ʱ����ΪNaHCO3 �� �ظ������������Σ�������������Ϊ20.00mL��
��3�����������������Һ100mL������2.0molL��1HCl�������ƣ����õζ�����ȡ��HCl��ҺmL������ʱ���ӿ̶��ߣ����������Ƶ���ҺŨ�����ƫ�ߡ�����ƫ�͡���û��Ӱ�족����
��4����Ʒ��Na2CO3����������Ϊ���ðٷ�����ʾ����ȷ��0.1%����
����������ȡm g��Ʒ��ѡ����ͼ����װ�òⶨ��Ʒ�����ᷴӦ���ɵ����������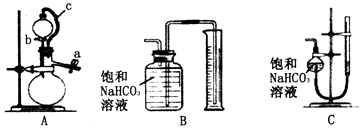
��5��ijͬѧ�����·������װ��A�������ԣ��ڷ�Һ©���м�������ˮ����ͼ���Ӻ�װ�ã��ر�ֹˮ��a����ֹˮ�м�ס��Ƥ��c������b����װ�ò�©������۲쵽������Ϊ �� ʵ��ʱ��װ��A��c�������� ��
��6��Ϊ����߲ⶨ��ȷ�ԣ�Ӧѡ��װ��A������д��ĸ��ţ�����ʵ�飮
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ij��ȤС����ݿα�ʵ����Ƶ�һ����˵��̼������̼���������ȶ��Ե���ʵ������ΪС�մ���Ϊ��������۲���ͼ��ʵ��װ�á�����ʵ��ԭ��������˵����������� ��

A. ���ձ��е�ʯ��ˮ�ȱ���ǣ�����ʯ��ˮ���������
B. Ҫ֤��̼�����������ܲ���ˮ������С�Թ�������մ����ˮ����ͭ��ĩ������
C. ����ʵ������п��Կ������ձ��ij���ʯ��ˮû�����
D. ͨ����ʵ��ɶԱ�С�մ�ʹ�������ȶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������һ�ֹ�ҵ��������Ҫ�ɷ�ΪMgCO3��MgSO4������Fe��Al�������Ϊԭ���Ʊ�MgCO33H2O��ʵ�������ͼ1 
��1����������ȵ�Ŀ����������ʱ�õ��IJ���������
��2������H2O2����ʱ������Ӧ�����ӷ���ʽΪ ��
��3������ͼ2��ʾ��ʵ��װ�ý�����ȡ�ͷ�Һ���Գ�ȥ��Һ�е�Fe3+ �� 
��ʵ��װ��ͼ2������A������Ϊ ��
��ΪʹFe3+�����ܶ�ش�ˮ��ת�����л��࣬��ȡ�IJ�������װ����Һ������A�м���һ�������л���ȡ���������á���Һ�����ظ���Σ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����pH=1������ƽ���ֳ�2�ݣ�1�ݼ�������ˮ����һ�ݼ�������������ʵ���Ũ����ͬ������NaOH��Һ��pH��������1��������ˮ��NaOH��Һ�������Ϊ�� ��
A.9��1
B.10��1
C.11��1
D.12��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com