
【题目】有机物W~H 有如下的转化关系。已知W、B为芳香族化合物,X为卤素原子,W、A、B均能与NaHCO3溶液反应,A分子中有2个甲基,H分子中含有醛基且苯环上的取代基处于对位。
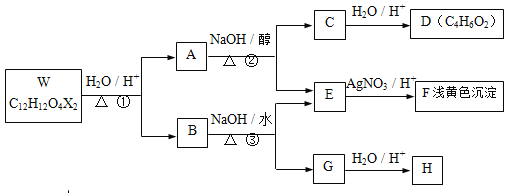
已知:
请回答下列有关问题:
(1)反应①、②分别属于 反应、 反应(填有机反应类型),A、B中均含有的含氧官能团的名称是 。
(2)F的化学式 ,B的结构简式 。
(3)反应②的化学方程式是 。
(4)若![]()
则反应④的化学方程式是 。
(5)H有多种同分异构体,且满足下列3个条件
(i) 遇FeCl3显紫色 (ii)苯环上一取代物有两种 (ⅲ)除苯环外无其它环状结构
试写出三种符合条件的同分异构体的结构简式 。
【答案】(1)水解(或取代)(1分) 消去(1分) 羧基 (1分)
(2)AgBr (1分) 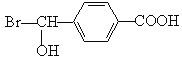 (2分)
(2分)
(3)(CH3)2CBrCOOH+2NaOH![]() CH2=C(CH3)COONa+NaBr+2H2O(3分)
CH2=C(CH3)COONa+NaBr+2H2O(3分)
(4)CH2=C(CH3)COOH+CH3OH![]() CH2=C(CH3)COOCH3+H2O(3分)
CH2=C(CH3)COOCH3+H2O(3分)
(5)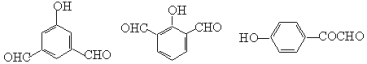 (3分)
(3分)
【解析】
试题分析:根据转化可知,反应①是W在酸性条件下发生水解反应生成A和B,因此反应类型是取代反应。W、A、B均能与NaHCO3溶液反应,这说明分子中均含有羧基。B与氢氧化钠的反应生成E与G,E能和硝酸银反应生成浅黄色沉淀,所以X是溴元素。G酸化后生成H,H分子中含有醛基且苯环上的取代基处于对位,这说明H、G、B分子中含有苯环。A在氢氧化钠的醇溶液中发生消去反应生成C与E,这说明A分子中含有1个溴原子。C酸化得到D,由于A分子中有2个甲基,则根据D的分子式C4H6O2可知,A的结构简式为(CH3)2CBrCOOH,因此D的结构简式为CH2=C(CH3)COOH。W分子中含有12个碳原子,则根据A的结构简式可知,B分子中含有8个碳原子。W水解应该产生羧基与羟基,但根据H可知B水解后产生醛基。所以根据已知信息可知B分子同一个碳原子上连接了溴原子与羟基,因此B的结构简式为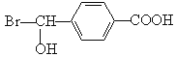 ,所以G的结构简式为
,所以G的结构简式为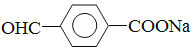 ,H的结构简式为
,H的结构简式为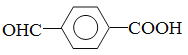 ,W的结构简式为
,W的结构简式为 。
。
(1)根据以上分析可知,反应①是取代反应,A、B中均含有的含氧官能团的名称是羧基。
(2)F是溴化银,化学式为AgBr;B的结构简式 。
。
(3)反应②是羧基与氢氧化钠中和以及溴原子的消去反应,则反应的化学方程式是(CH3)2CBrCOOH+2NaOH![]() CH2=C(CH3)COONa+NaBr+2H2O。
CH2=C(CH3)COONa+NaBr+2H2O。
(4)根据有机玻璃的结构简式可知,该醇应该是甲醇,则反应④的化学方程式为CH2=C(CH3)COOH+CH3OH![]() CH2=C(CH3)COOCH3+H2O。
CH2=C(CH3)COOCH3+H2O。
(5)遇FeCl3显紫色,说明含有酚羟基。苯环上一取代物有两种,说明苯环应该是对称的。除苯环外无其它环状结构,所以符合条件的结构简式有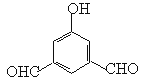 、
、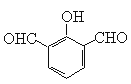 、
、![]() 。
。


科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:2A+3B![]() 2C。开始时C的浓度为amol·L-1,2min后C的浓度变为2amol·L-1,A和B的物质的量浓度均变为原来的1/2,则下列说法中不正确的是( )
2C。开始时C的浓度为amol·L-1,2min后C的浓度变为2amol·L-1,A和B的物质的量浓度均变为原来的1/2,则下列说法中不正确的是( )
A.用B表示的反应速率是0.75a mol/(L·min)
B.反应开始时,c(B)=3amol·L-1
C.反应2min后,c(A)=0.5amol·L-1
D.反应2min后,c(B)=1.5amol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂一空气电池是高能量密度的新型电池,结构如图所示。下列说法正确的是( )

A.固体电解质只有Li+可通过
B.电池反应为![]()
C.充电时,水性电解液的pH将升高
D.放电时,若外电路有0. 1mol e -通过时,理论上将消耗1.12 LO2(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①~⑩十种元素,在元素周期表中的位置如图所示。回答下列问题:

(1)在上述十种元素中,置换酸中氢的能力最强的元素为 (填化学符号,下同);最高价氧化物的水化物的酸性最强的化合物的化学式是 ,碱性最强的化合物的化学式是 ,显两性的氢氧化物的化学式是 ;原子半径最大的元素是 ,半径最小的离子是 。
(2)上述十种元素中,金属性最强的元素在周期表中的位置是第 周期 族,该元素的单质在空气中燃烧的化学方程式为 。
(3)试用电子式表示元素①和③形成分子的过程 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列给出了四种烃A、B、C、D的相关信息:
①烃A在所有的烃中含碳的质量分数最低;
②烃B是一种植物生长调节剂,可用于催熟果实;
③烃C在氧气中燃烧产生的氧炔焰常用来切割或焊接金属;
④烃D的分子比例模型如图所示。
据此回答下列问题:
(1)写出A与氯气光照下反应的化学方程式(只写第一步)为 ;
(2)将1mol A和适量的Cl2混合后光照,测得所得所有有机取代产物物质的量相等,则消耗的氯气物质的量是____________。
(3)写出B与水在催化剂作用下反应的化学方程式: 。
(4)写出C与足量溴的四氯化碳溶液反应的化学方程式: 。
(5)D分子中不存在一般的碳碳单键和碳碳双键交替的结构,以下能证实这一事实的是 。
a.D的邻位二氯取代物不存在同分异构体
b.D的间位二氯取代物不存在同分异构体
c.D 不能使溴的四氯化碳溶液褪色
d.D不能被酸性高锰酸钾溶液氧化
e.D在催化剂作用下能与氢气发生加成反应
(6)写出D与浓硝酸、浓硫酸混合后加热至50℃~60℃反应的化学方程式:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Mg-AgCl电池是一种以海水为电解质溶液的水激活电池,下列叙述错误的是
A.负极反应式为Mg-2e-=Mg2+
B.正极反应式为Ag++e-=Ag
C.电池放电时Cl-由正极向负极迁移
D.负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液加入金属铝能放出氢气。下列各组离子在该溶液中一定可以大量共存的是
A.Al3+、NH4+、Cl-、SO42-
B.Na+、Cl-、SO42-、HCO3-
C.Na+、CH3COO-、NO3- 、K+
D.K+、Na+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大;A是周期表中原子半径最小的元素;B元素的最高价氧化物的水化物与其简单氢化物能相互反应生成盐;C元素原子的最外层电子数是内层电子数的3倍;D元素的主族序数等于其周期数;E元素原子的最外层电子数是其电子层数的2倍。G单质是日常生活中用量最大的金属,易被腐蚀。
试回答下列问题:
(1)A元素的同位素有___________(写原子符号)
(2)实验室制取B的简单氢化物的化学反应方程式为_________________________
(3)C、D、E、F的简单离子半径由大到小的顺序是_________________(用离子符号表示)
(4)用化学事实说名E与F这两种元素非金属性的强弱_____________________(举一例)
(5)下列有关G的说法不正确的是_______
A、铁位于第四周期ⅧB族,在人体内的血红蛋白中含有铁元素
B、过量的铁分别与氯气和稀盐酸反应所得氯化物相同
C、FeCl3、FeCl2、Fe(OH)3都可以通过化合反应制取
D、氢氧化铁与HI溶液仅发生中和反应
(6)向NaOH溶液中通入一定量的F单质,两者恰好完全反应,生成物中有三种含F的离子,其中两种离子的物质的量与反应时间的曲线如图所示。请写出t2时反应的总的化学方程式 _____________________ 。
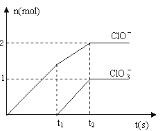
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com