
����Ŀ��ijѧ��Ϊ�ⶨδ֪Ũ�ȵ�������Һ��ʵ�����£���1��00mL������������100 mLϡH2SO4��Һ����0��14mol��L��NaOH��Һ�ζ�����ϡH2SO425mL���ζ���ֹʱ����NaOH��Һ15mL��
��1����ѧ���ñ�0��14 mol��L NaOH��Һ�ζ������ʵ��������£�
A������ʽ�ζ���ȡϡH2SO4 25 mL��ע����ƿ�У�����ָʾ����
B���ô��ⶨ����Һ��ϴ��ʽ�ζ��ܡ�
C��������ˮϴ�ɾ��ζ��ܡ�
D��ȡ�¼�ʽ�ζ����ñ���NaOH��Һ��ϴ����Һע���ʽ�ζ��̶ܿȡ�0������2��3 cm�����ٰѼ�ʽ�ζ��̶ܹ��ã�����Һ�����̶ȡ�0����0���̶����¡�
E�����ζ����Ƿ�©ˮ��
F����ȡ��ƿ�����ظ�����һ�Ρ�
G������ƿ���ڵζ������棬ƿ�µ�һ�Ű�ֽ���ߵα�ҡ����ƿֱ���ζ��յ㣬���µζ���Һ�����ڿ̶ȡ�
�ٵζ���������ȷ˳����(�������д)��_______________��
�ڸõζ�������Ӧѡ�õ�ָʾ���ǣ�____________________��
����G���������ȷ���յ�?__________________________________��
��2����ʽ�ζ���������ˮ��ϴ��δ�ñ�Һ��ϴ���µζ����(�ƫС������ƫ��ǡ�ú��ʡ�)________��ԭ����__________________________��
��3�������������(ϡ��ǰ������)��Һ�����ʵ���Ũ��__________mol��L��������λС����
���𰸡� ECDBAGF ��̪ ���������һ��NaOH��Һ����Һ����ɫ���dz��ɫ���Ұ���Ӳ���ɫ ƫ�� �ζ����ڱ��ϵ�ˮĤ������Һϡ�ͣ�ʹ�������ƫ�� 4.20
��������(1)���ñ�0.14mol/L NaOH��Һ�ζ������ʵ���������Ϊ�����ζ����Ƿ�©ˮ��ϴ�ӵζ��ܡ���ϴ��ʢװ��Һ����ϴʢװ��Һ�ĵζ��ܡ�ʢװ��Һ����ʼ�ζ����ظ��ζ��ȣ�������ȷ�IJ���˳��Ϊ��ECDBAGF���ʴ�Ϊ��ECDBAGF��
��������������������ǡ���кͣ���Һ��pH=7������ѡ�÷�̪(��ɫ��ΧΪ��8-10)��Ϊָʾ�����ʴ�Ϊ����̪��
�۵ζ�����ǰ�������̪��������ҺΪ��ɫ���ζ�����ʱ����Һ��ɺ�ɫ�����Եζ��յ�����Ϊ���������һ��NaOH��Һ����ҺͻȻ��ɺ�ɫ������Ӳ���ɫ���ʴ�Ϊ���������һ��NaOH��Һ����ҺͻȻ��ɺ�ɫ������Ӳ���ɫ��
(2)��ʽ�ζ���������ˮ��ϴ��δ�ñ�Һ��ϴ���൱�ڱ�Һ��ϡ�ͣ��������ĵ���ϡ����ͻ����࣬�ζ����ƫ�ʴ�Ϊ��ƫ�ζ����ڱ��ϵ�ˮĤ������Һϡ�ͣ�ʹ�������ƫ��
(3)���ݷ�Ӧ��2NaOH+H2SO4=Na2SO4+2H2O��ϡ�ͺ��������ҺŨ��Ϊ��c(H2SO4)= 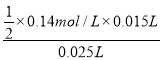 =0.042mol/L��ϡ��ǰϡ�����Ũ��Ϊ��0.042mol/L��
=0.042mol/L��ϡ��ǰϡ�����Ũ��Ϊ��0.042mol/L��![]() =4.20mol/L���ʴ�Ϊ��4.20��
=4.20mol/L���ʴ�Ϊ��4.20��


 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�����͵ġ��-����CO2��ء����ṹ��ͼ��ʾ������˵������ȷ����
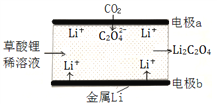
A. ��װ���ǻ�ѧ��ת��Ϊ����
B. ���øü����ɼ�����������CO2���ŷ�
C. �����ĵ缫��ӦΪ��2CO2 + 2e- = C2O42-
D. ÿ����10.2g Li2C2O4����0.2mol Li+������Ǩ��������
���𰸡�D
��������A����װ��Ϊԭ���װ�ã�����ѧ��ת��Ϊ���ܣ���A��ȷ��B����ͼ��֪��CO2ת��ΪC2O42-���ɼ�������������ŷţ���B��ȷ��C��CO2��C2O42-��̼Ԫ�ػ��ϼ۽��ͣ��õ��ӣ���CO2������������Ӧ���缫��ӦΪ��2CO2 +2e-=C2O42-����C��ȷ��D��ԭ����У��������������ƶ�����D����ѡD��
�����͡���ѡ��
��������
27
����Ŀ���ö��Ե缫�������������Һһ��ʱ����ټ���һ���������ڵĴ������ʹ��Һ�ָ���ԭ���ijɷֺ�Ũ�ȵ���
A. AgNO3[AgNO3] B. NaOH[NaOH] C. KCl[H2O] D. CuSO4[CuO]
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��3��5-����������������Ҫ���л��ϳ��м��壬��������Ȼ���ʰ������صĺϳɡ�һ���Լ䱽����Ϊԭ�ϵĺϳɷ�Ӧ���£�

��Ӧ�������ȷ�����״����ټ������ѣ�����õ��л��㣨�������Ȼ��⣩����ϴ�ӣ�Ȼ������ᴿ�õ�����״���3��5-�����������ӵIJ����������ʼ��±�������˵����ȷ����
���� | �е�/�� | �۵�/�� | �ܽ��� |
�״� | 64. 7 | ��97.8 | ������ˮ |
3��5-������������ | 172~175 | 33~36 | �����ڼ״������ѣ�����ˮ |
A. �����ϳɷ�Ӧ����ȡ����Ӧ
B. �䱽�����뱽�ӻ�Ϊͬϵ��
C. ������״��IJ����ǽᾧ
D. ϴ��ʱ�����ñ���Na2CO3��Һ���Ȼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪NO��O2����Ӧ���ͷ�Ӧ��ת��ΪNO2,�������仯�淴Ӧ���̵�ͼʾ���¡�

��2NO(g)![]() N2O2(g)��H1ƽ�ⳣ��K1
N2O2(g)��H1ƽ�ⳣ��K1
��N2O2(g)+O2(g)![]() 2NO2(B)��H2ƽ�ⳣ��K2
2NO2(B)��H2ƽ�ⳣ��K2
����˵������ȷ������ ��
A. ��H1<0,��H2<0
B. 2NO(g)+O2(g)![]() 2NO2(g)��ƽ������K=K1/K2
2NO2(g)��ƽ������K=K1/K2
C. ��ʾ2NO(g)+O2(g)![]() 2NO2(g)�ġ�H=��H1+��H2
2NO2(g)�ġ�H=��H1+��H2
D. ��Ӧ�������ʴ�С����2NO(g)+O2(g)![]() 2NO2(g)�ķ�Ӧ����
2NO2(g)�ķ�Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�����SO42�����Լ��ǣ� ��
A.BaCl2��ϡ����
B.AgNO3��ϡ����
C.ϡ���ᡢBaCl2
D.AgNO3��ϡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ͻ���һ����;�㷺�Ľ������ϣ����й��ںϽ��������ȷ���ǣ� ��
A.�Ͻ��Ӳ�ȱ�������ijɷֽ���С
B.���ҹ���ʹ������ĺϽ�����ͭ
C.�Ͻ���۵�һ���������ijɷֽ�����
D.Ŀǰ���������;���ĺϽ������Ͻ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҷ����������D������ʯ�����ѽ�õ���ϩ���ϳɡ��ش��������⣺

��֪�� R-X![]() R-OH��R-XΪ±������R-����������
R-OH��R-Xڱ������R-����������
��1��B��AΪͬϵ�B�Ľṹ��ʽΪ_______________��
��2��C2H6O�����й����ŵ�����______________����Ӧ���ķ�Ӧ����Ϊ________________��
��3��C�Ľṹ��ʽΪ_______________________��
��4����Ӧ���Ļ�ѧ����ʽΪ__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ù��AFTB1����ṹ��ʽ����ͼ��ʾ��������Ⱦ��ʳ�����ù�أ������P53��������ڻ���ù�ص������»ᷢ��ͻ�䣬�������ΰ��Ŀ����ԡ�����˵����ȷ����
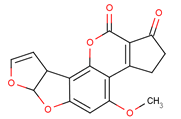
A. ����ù�ط��������е�ԭ�ӿ϶�������
B. ����ù�ط����к���4������̼ԭ��
C. 1mol����ù���������5 mol H2�����ӳɷ�Ӧ
D. ����ù�ؿ��Է���ȡ�����ӳɡ���ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���˵�ѪҺ�е������ǣ����Ѫ�ǣ��ĺ������ԡ�mmol/L����ʾʱ������ֵ��3.61~6.11 mmol/L֮�䡣���ֱ�ʾѪ��ָ�����������
A. �������� B. ���ʵ���Ũ�� C. Ħ������ D. �ܽ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com