
【题目】按要求回答下列问题:
(1)键线式![]() 的系统命名为 __________________;
的系统命名为 __________________;
(2)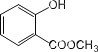 中含有的官能团为_______________;
中含有的官能团为_______________;
(3)2-甲基-1-丁烯的结构简式____________________;
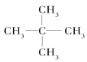
(4)相对分子质量为 72 且一氯代物只有一种的烷烃的结构简式________________;
(5)分子式为 C2H6O 的有机物,有两种同分异构体,乙醇(CH3CH2OH)、甲醚(CH3OCH3),则通过下列方法,不可能将二者区别开来的是________________;
A.红外光谱 B.核磁共振氢谱 C.质谱法 D.与钠反应
【答案】2-甲基戊烷 羟基、酯基 ![]()
 C
C
【解析】
(1)键线式![]() ,主链有5个碳原子,2号碳原子连有1个甲基,系统命名为2-甲基戊烷;
,主链有5个碳原子,2号碳原子连有1个甲基,系统命名为2-甲基戊烷;
(2)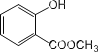 中含有的官能团为羟基、酯基;
中含有的官能团为羟基、酯基;
(3)根据系统命名原则,2-甲基-1-丁烯主链有4个碳,含一个双键,结构简式为![]() ;
;
(4)相对分子质量为 72烷烃分子式是 C5H12,一氯代物只有一种,说明只有一种等效氢,结构对称,该烷烃的结构简式是 ;
;
(5)乙醇(CH3CH2OH)、甲醚(CH3OCH3),官能团不同,能用红外光谱鉴别,不选A;
乙醇(CH3CH2OH)有3种等效氢、甲醚(CH3OCH3) 有1种等效氢,能用核磁共振氢谱鉴别,不选B;
乙醇(CH3CH2OH)、甲醚(CH3OCH3)的相对分子质量相同,不能用质谱法鉴别,故选C;
乙醇(CH3CH2OH)与钠反应放出氢气、甲醚(CH3OCH3)与钠不反应,故不选D。


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:
【题目】室温时,CaCO3在水中的沉淀溶解平衡曲线如图所示。已知CaCO3的溶度积(室温)为2.8×10-9,下列说法中不正确的是

A. x的数值为2×10-5
B. c点时有CaCO3生成
C. 加入蒸馏水可使溶液由d点变成 a点
D. b点与d点对应的溶度积相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某气体反应的平衡常数可表示为K=c(CH3OCH3)c(H2O)/c2(CH3OH),该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44。请回答下列问题:
(1)写出上述反应的化学方程式:_________________________________ 。
(2)该反应的△H _________0。
(3)已知在密闭容器中,测得某时刻各组分的浓度如下:
物质 | CH3OH(g) | CH3OCH3(g) | H2O(g) |
浓度/(molL-1) | 0.54 | 0.68 | 0.68 |
①此时温度400℃,则某时刻υ正_______υ逆(填<、>或=,下同)。
②若以温度为横坐标,以该温度下平衡态甲醇物质的量n为纵坐标,此时反应点在图象的位置是图中____点,比较图中B、D两点所对应的正反应速率υB_______υD,理由是____。

(4)一定条件下要提高反应物的转化率,可以采用的措施是___________。
a.升高温度 b.加入催化剂 c.压缩容器的体积
d.增加水蒸气的浓度 e.及时分离出产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)常作氯化剂或氯璜化剂,用于制作药品、染料、表面活性剂等。有关物质的部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
SO2Cl2 | -54.1 | 69.1 | ①易水解,产生大量白雾②易分解:SO2Cl2 |
H2SO4 | 10.4 | 338 | 具有吸水性且不易分解 |
实验室用干燥而纯净的二氧化硫和氯气合成硫酰氯,反应的化学方程式为SO2(g)+Cl2(g) ![]() SO2Cl2(l)△H=-97.3kJ/mol。装置如图所示(夹持仪器已省略),请回答有关问题:
SO2Cl2(l)△H=-97.3kJ/mol。装置如图所示(夹持仪器已省略),请回答有关问题:
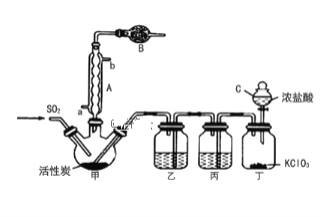
(1)仪器B的名称是______,作用是________。
(2)若无装置乙硫酰氯会发生水解,则硫酰氯水解反应的化学方程式为_______。
(3)写出丁装置中发生反应的化学反应方程式____________。
(4)为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有____(填序号)。
①先通冷凝水,再通气 ②控制气流速率,宜慢不宜快③若三颈烧瓶发烫,可适当降温④加热三颈烧瓶
(5)少量硫酰氯也可用氯磺酸(ClSO3H)分解获得,该反应的化学方程式为______。此方法得到的产品中会混有硫酸,从分解产物中分离出硫酰氯的方法是_____。
(6)工业上处理SO2废气的方法很多,例如可以用Fe2(SO4)3酸性溶液处理,其工艺流程如下,溶液②转化为溶液③发生反应的离子方程式为_________。
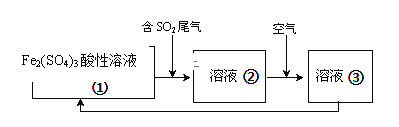
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯及其化合物在工农业生产和人类生活中有着重要的作用。回答下列问题:
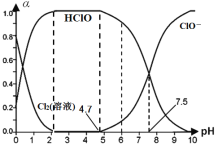
(1)25℃时将氯气溶于水形成“氯气-氯水”体系,该体系存在多个含氯元素的平衡关系,其中之一为:Cl2(溶液)+H2O![]() HClO+H++Cl-,体系中Cl2(溶液)、HClO和ClO-三者的物质的量分数(α)随pH(酸碱度)变化的关系如图所示。已知HClO的杀菌能力比ClO-强,用氯气处理饮用水时,杀菌效果最强的pH范围为__(填字母)。
HClO+H++Cl-,体系中Cl2(溶液)、HClO和ClO-三者的物质的量分数(α)随pH(酸碱度)变化的关系如图所示。已知HClO的杀菌能力比ClO-强,用氯气处理饮用水时,杀菌效果最强的pH范围为__(填字母)。
A.0~2 B.2~4.7 C.4.7~7.5 D.7.5~10
(2)写出次氯酸光照分解的化学方程式___,如果在家中直接使用自来水养金鱼,除去其中残留的次氯酸可采取的简易措施为__。
(3)NaClO、NaClO2、ClO2等含氯化合物都是常见的消毒剂,这是因为它们都具有强氧化性。
①写出工业上用氯气和NaOH溶液生产消毒剂NaClO的化学方程式___;
②84消毒液(主要成分是NaClO)与洁厕灵(主要成分是盐酸)混在一起使用会产生有毒气体Cl2,其反应的离子方程式为__;
③NaClO2中Cl元素化合价为__;
④ClO2的杀菌效果比Cl2好,等物质的量的ClO2杀菌效果是Cl2的__倍(杀菌效果与单位物质的量的氧化剂得电子的物质的量有关,ClO2与Cl2消毒杀菌后均被还原为Cl-)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是一种重要的有机合成中间体,它的合成路线如图:
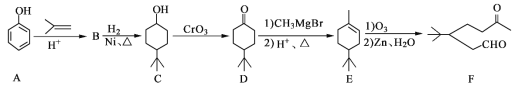
(1)化合物F中含氧官能团的名称是______和______,由A生成B的化学反应类型是______;
(2)写出化合物B的结构简式:______;
(3)写出化合物C与乙酸反应生成酯的化学方程式:______;
(4)某化合物是D的同分异构体,且分子中只有三种不同化学环境的氢。写出该化合物的结构简式:______(任写一种);
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医药阿斯匹林的结构简式如图。试回答:
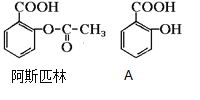
(1)阿斯匹林可看成酯类物质,口服后在胃肠作用下,阿斯匹林发生水解反应,生成A和B两种产物。其中A的结构简式如图,则阿斯匹林的分子式为:____________,B的结构简式为:_______,B中的官能团是:____________(名称)。
(2)上述水解产物B与甲醇、浓硫酸共热反应的化学方程式为:____________。
(3)甲醇在铜作催化剂时与氧气反应的化学方程式为:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
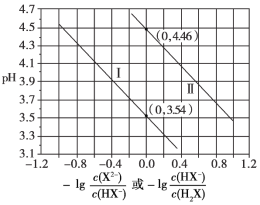
【题目】常温下,H2X溶液中逐滴滴加NaOH溶液,混合溶液的pH与离子浓度变化的关系如图所示,下列说法正确的是( )
A.H2X的电离方程式为:H2X![]() 2H++X2-
2H++X2-
B.pH与-lg![]() 的变化关系是曲线Ⅰ
的变化关系是曲线Ⅰ
C.常温下,水解反应X2-+H2O![]() HX-+OH-的化学平衡常数为10-9.54
HX-+OH-的化学平衡常数为10-9.54
D.NaHX溶液中离子浓度由大到小顺序:c(Na+)>c(HX-)>c(X2-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或有关化学用语的使用正确的是( )
A.在基态多电子原子中,p轨道电子的能量一定高于s轨道电子的能量
B.Fe原子的外围电子排布图为![]()
C.氧的非金属性比氮大,故氧元素的第一电离能比氮元素的第一电离能大
D.铜原子的外围电子排布式为3d94s2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com