
【题目】表为元素周期表的一部分,用化学用语回答下列有关问题: 
(1)⑧的原子结构示意图为:;
(2)②和③气态氢化物稳定性大小顺序是:(写化学式);
(3)③、⑧、⑩的最高价含氧酸的酸性最强的是:(写化学式);
(4)实验室制取③的气态氢化物的化学方程式为
③的气态氢化物与③的最高价氧化物对应的水化物反应生成的盐是(写化学式),它属于(选填“共价化合物”或“离子化合物”)
(5)①、④、⑩三种元素的原子能形成原子数目比为1:1:1的共价化合物,它的电式式为:
(6)欲比较④和⑨两种元素非金属性强弱,可以做为验证的证据是(填序号).
A.比较这两种元素单质的沸点
B.比较这两种元素单质与氢气化合的难易
C.比较这两种元素的最高价氧化物水化物的酸碱性
D.比较这两种元素单质与酸或碱反应的难易性.
【答案】
(1)
(2)NH3>CH4
(3)HClO4
(4)Ca(OH)2+2NH4Cl ![]() CaCl2+2NH3↑+2H2O;NH4NO3;离子化合物
CaCl2+2NH3↑+2H2O;NH4NO3;离子化合物
(5)![]()
(6)C
【解析】解:由元素在周期表中位置,可知①为H、②为C、③为N、④为O、⑤为Na、⑥为Mg、⑦为Al、⑧为P、⑨为S、⑩为Cl.
(1.)⑧为P,质子数为15,原子核外有15个电子,由核外电子排布规律,原子结构示意图为  ,所以答案是:
,所以答案是:  ;
;
(2.)同周期自左而右非金属性增强,非金属性越强,对应氢化物越稳定,故氢化物稳定性NH3>CH4 , 所以答案是:NH3>CH4;
(3.)最高价含氧酸的酸性最强的是高氯酸,化学式为HClO4 , 所以答案是:HClO4;
(4.)实验室用氯化铵与氢氧化钙再加热条件下制备氨气,反应方程式为:Ca(OH)2+2NH4Cl ![]() CaCl2+2NH3↑+2H2O,③的气态氢化物与③的最高价氧化物对应的水化物反应生成的盐是NH4NO3 , 属于离子化合物,所以答案是:Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O,③的气态氢化物与③的最高价氧化物对应的水化物反应生成的盐是NH4NO3 , 属于离子化合物,所以答案是:Ca(OH)2+2NH4Cl ![]() CaCl2+2NH3↑+2H2O;NH4NO3;离子化合物;
CaCl2+2NH3↑+2H2O;NH4NO3;离子化合物;
(5.)①、④、⑩三种元素的原子能形成原子数目比为1:1:1的共价化合物为HClO,分子中氧原子分别与H原子、Cl原子形成1对共用电子对,电子式为: ![]() ,所以答案是:
,所以答案是: ![]() ;
;
(6.)可以根据单质与氢气反应难易程度或剧烈程度、最高价含氧酸的酸性、单质之间相互置换、化合物中元素化合价等判断非金属性强弱.
A.单质的沸点属于物理性质,不能比较元素非金属性强弱,故A错误;
B.非金属性越强,单质与氢气化合越容易,故B正确;
C.非金属性越强,最高价氧化物水化物的酸性越强,但氧元素没有含氧酸,故C错误;
D.通过单质与酸或碱反应不能判断非金属性强弱,故D错误.故选:B.


科目:高中化学 来源: 题型:
【题目】能在水溶液中大量共存的一组离子是
A.H+、I―、NO3―、SiO32-B.Ag+、Fe3+、Cl―、SO42―
C.K+、SO42-、Cu2+、NO3―D.NH4+、OH-、Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W,X,Y,Z在元素周期表中的位置如图所示.下列说法中,正确的是( ) 
A.W的最高价氧化物对应的水化物是强酸
B.Y的原子半径在同周期主族元素中最大
C.W的非金属性比Z的弱
D.Z的气态氢化物的稳定性在同主族元素中最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香烟烟雾中往往含有CO和SO2气体,下列关于它们的说法中正确的是( )
A. 两者都易溶于水
B. 两者都是形成酸雨的主要原因
C. 两者都能使品红溶液褪色
D. 两者都污染环境,危害健康
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们常用“84”消毒液对环境进行消毒。该消毒液无色,对某些有色物质有漂白作用,对该溶液进行焰色反应,呈黄色。你认为它可能的有效成分是( )
A.NaOHB.NaClOC.KMnO4D.Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属的叙述中正确的是( )
A. 常温下所有的金属都是固态
B. 金属具有导电、导热和延展性
C. 金属都具有较高的硬度和密度
D. 金属都具有较高的熔点和沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】缩醛在有机合成中常用于保护羰基或作为合成中间体,同时还是一类重要的香料,广泛应用于化妆品、食物、饮料等行业。G是一种常用的缩醛,分子中含有一个六元环和一个五元环结构。下面是G的一种合成路线:
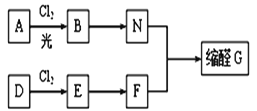
已知:①芳香烃A含氢元素的质量分数为8.7%,A的质谱图中,分子离子峰对应的最大质荷比为92; D的产重可以用来衡量一个国家的石油化工发展水平。
②同一个碳原子连接两个羟基不稳定,易脱水形成羰基。
③
回答下列问题:
(1)A的结构简式是_____________________,E的名称是____________________________。
(2)由D生成E的反应类型是________,E→F的反应条件是_________________________。
(3)由B生成N的化学方程式为___________________________。
(4)有研究发现,维生素C可以作为合成G物质的催化剂,具有价廉、效率高、污染物少的优点。维生素C的结构如右图。则维生素C分子中含氧官能团名称为_____________。

(5)缩醛G的结构简式为______________。G有多种同分异构体,写出其中能同时满足以下条件的所有同分异构体的结构简式:_________________________。
①既能发生银镜反应,又能与FeC13发生显色反应;②核磁共振氢谐为4组峰。
(6)写出用2-丁烯为原料(其他无机试剂任选)制备顺丁橡胶(顺式聚1,3-丁二烯)的合成路线:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾的形成与汽车尾气和燃煤有直接的关系,新近出版的《前沿科学》杂志刊发的中国环境科学研究院研究员的论文《汽车尾气污染及其危害》,其中系统地阐述了汽车尾气排放对大气环境及人体健康造成的严重危害。
(1)用SO2气体可以消除汽车尾气中NO2, 已知NO2(g)+SO2(g)![]() SO3(g)+NO(g)。一定条件下,将NO2与SO2以物质的量比1∶2置于体积为1L 密闭容器中发生上述反应,测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡常数K=____。
SO3(g)+NO(g)。一定条件下,将NO2与SO2以物质的量比1∶2置于体积为1L 密闭容器中发生上述反应,测得上述反应平衡时NO2与SO2体积比为1∶6,则平衡常数K=____。
(2)目前降低尾气中的NO和CO可行方法是在汽车排气管上安装催化转化器。NO和CO在催化转换器中发生反应:2CO(g)+2NO(g)![]() N2(g)+2CO2(g) △H=-a kJ·mol-1。在25℃和101kPa下,将2.0mol NO、2.4mol气体CO通入到固定容积为2L的容器中,反应过程中部分物质的浓度变化如图所示:
N2(g)+2CO2(g) △H=-a kJ·mol-1。在25℃和101kPa下,将2.0mol NO、2.4mol气体CO通入到固定容积为2L的容器中,反应过程中部分物质的浓度变化如图所示:

①有害气体NO的转化率为________。
②20min时,若改变反应条件,导致CO浓度减小,则改变的条件可能是_____(选填序号)。
a.缩小容器体积 b.增加CO的量 c.降低温度 d.扩大容器体积
(3)消除汽车尾气中NO2也可以用CO,已知2NO(g)+O2(g)=2NO2(g) △H=-b kJ·mol-1;CO的燃烧热△H=-c kJ·mol-1。写出消除汽车尾气中NO2的污染时,NO2与CO的反应的热化学反应方程式 ____________________。
(4)已知NH3·H2O的Kb=2.0 ×10-5
①求0.10 mol/L的 NH3·H2O的c(OH-)=______________mol/L
②若向其中加入固体NH4Cl,使c(NH4+)的浓度达到0.20 mol/L,则c(OH-)=______mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com