
【题目】如图表示在一定的温度下,容积固定的密闭容器中,A、B、C三种气体物质的浓度随时间变化的情况,试回答下列问题:
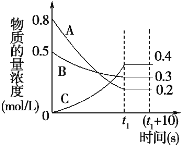
(1)该反应的化学方程式为 。
(2)0~t1s 内B气体的平均反应速率为 。
(3)(t1+10)s 时,A的转化率为 ,此时v(A)正 v(B)逆(填“>”、“<”或“=”)。
(4)关于该反应的说法正确的是 。
a.到达t1时刻该反应已停止
b.在t1时刻之前B气体的消耗速率大于它的生成速率
c.在t1时刻C气体的正反应速率等于逆反应速率
(5)容器中(t1+10)s时的压强与起始时的压强之比为 。
【答案】(1)3A+B![]() 2C (2)0.2/t1mol·L-1·s-1
2C (2)0.2/t1mol·L-1·s-1
(3)75% > (4)bc (5)9:13
【解析】
试题分析:(1)根据图像可知,随着时间的推移,A、B的物质的量浓度不断减少,C的物质的量浓度不断增加,所以A、B为反应物,C为生成物,化学计量数之比为(0.8-0.2):(0.5-0.3):(0.4-0)=3:1:2,该反应为3A+B![]() 2C;
2C;
(2)由图像可知,0~t1 s 内B的物质的量浓度减少0.2mol/L,则B气体的平均反应速率为0.2/t1mol·L-1·s-1。
(3)(t1+10)s 时,A的转化率为(0.8-0.2)÷0.8×100%=75%;在(t1+10)s时,反应达到平衡状态,用相同物质表示的化学反应速率,正反应速率等于逆反应速率,而化学反应速率之比等于化学计量数之比,根据化学反应3A+B![]() 2C,v(A)正>v(B)逆。
2C,v(A)正>v(B)逆。
(4)a.根据图像可知,到达t1时刻反应处于平衡状态,化学平衡状态是动态平衡,该反应没有停止,错误;b.在t1时刻之前,反应正向移动,B气体的消耗速率大于它的生成速率,正确;C.在t1时刻,可逆反应达到平衡状态,C气体的正反应速率等于逆反应速率,正确;答案选bC.
(5)设容器的体积为V,起始物质的量为(0.8+0.5+0)V=1.3V,平衡物质的量为(0.4+0.3+0.2)V=0.9V,相同条件下,压强之比等于物质的量之比,所以容器中(t1+10)s时的压强与起始时的压强之比为0.9V:1.3V=9:13。


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:
【题目】(14分)下表为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列问题:
(1)Z元素在周期表中的位置为 。
(2)表中元素原子半径最大的是(写元素符号) 。
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是 。
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)碳与镁形成的1mol化合物Q与水反应,生成2molMg(OH)2和1mol烃,该烃分子中碳氢质量比为9:1,烃的电子式为 。Q与水反应的化学方程式为 。
(5)X与Z两元素的单质反应生成1molX的最高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出该反应的热化学方程式 。
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L 2.2mol/LNaOH溶液和1molO2,则两种气体的分子式及物质的量分别为 ,生成硫酸铜物质的量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池发生的反应是可自发进行的氧化还原反应,CO/O2燃料电池以熔融状态的碳酸盐为电解质,下列说法正确的是 ( )
A、CO在正极通入
B、CO32— 在电池内部向正极移动
C、当有22.4LCO参加反应时电路中有2mol电子发生转移
D、该电池电解质在固态时,电池无法工作
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.海洋约占地球表面积的71%,所以地球上不缺水
B.海水淡化蒸馏法的成本最低
C.海水淡化的主要方法有蒸馏法、电渗析法和离子交换法等
D.以上说法都正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验是实现科学探究的重要途径。
(1)下列关于教材实验的叙述中正确的是
A.Cu片加入冷的浓硫酸中没有变化,说明Cu在浓硫酸中也会钝化
B.石油分馏时,控制温度,收集到的汽油为纯净物
C.用激光笔照射肥皂水,有丁达尔效应,说明肥皂水是胶体
D.淀粉水解液中加入银氨溶液,水浴加热后无银镜,说明淀粉未水解
E.鸡蛋白溶液中分别加入饱和硫酸铵、硫酸钾溶液时,都发生了盐析
(2)某兴趣小组设计出下图装置(气密性已检查),验证铜与稀硝酸反应的产物。
已知:FeSO4+NO=[Fe(NO)]SO4,该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色。
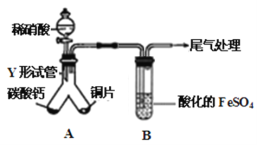
①实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是 。
②由分液漏斗向Y形试管右侧加入稀硝酸,反应的离子方程式是
。
③本实验A生成的气体中,若有NO2,B的实验现象为 ;若只有NO生成,B的实验现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.氯化铝溶液中加入过量氨水:Al3++3NH3.H2O=Al(OH)3↓+3NH4+
B.碳酸钙和盐酸反应:CO32﹣+2H+=CO2↑+H2O
C.三氯化铁溶液与氢氧化钠溶液反应:FeCl3+3OH﹣=Fe(OH)3↓+3Cl﹣
D.铜加入稀硝酸中:Cu+4H++NO3﹣=Cu2++NO↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中存在XO3―,且X为短周期元素,则一定能在该溶液中大量共存的离子组是( )
A.Na+、H+、SO42-、I-
B.Na+、Ca2+、CO32-、Al3+
C.Na+、K+、Fe2+、H+
D.K+、SO42-、Cl-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列事实不能说明上述观点的是
A. 苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应
B. 甲苯能使酸性高锰酸钾溶液褪色,乙烷不能使酸性高锰酸钾溶液褪色
C. 乙烯能发生加成反应,乙烷不能发生加成反应
D. 苯与硝酸在加热时发生取代反应,甲苯与硝酸在常温下就能发生取代反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com