
【题目】某课外活动小组探究NO2性质,其实验装置如下图所示(夹持和固定装置省去)
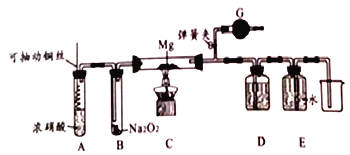
(1)铜与浓硝酸反应的离子方程式为__________,装置A的优点是______________。
(2)G中试剂为_________,作用是________________________。
(3)类比Mg与CO2反应的思路,写出Mg与NO2反应的化学方程式___________________,设计装置D(内装NaOH溶液)和装置E的目的是______________________。
(4)一段时间后,装置B中管壁发烫,瓶内红棕色物质消失,淡黄色粉末变成白色固体(为单一物质)。小组同学认为Na2O2与NO2发生了氧化还原反应,其结果有两种假设:
①NO2被Na2O2氧化,则白色固体是_______(填化学式)。
②NO2被Na2O2还原,为了验证此产物,取适量白色固体于试管中,加蒸馏水溶解,滴加酸性高锰酸钾溶液,则观察到的现象是__________________________。
【答案】 Cu+4H++2NO3-=Cu2++2NO2↑+2H2O 可以控制反应的速率 碱石灰(NaOH固体) 吸收NO2,避免污染环境 Mg+2NO2![]() 4MgO+N2 证明装置C中发生反应生成N2 NaNO3 高锰酸钾溶液褪色
4MgO+N2 证明装置C中发生反应生成N2 NaNO3 高锰酸钾溶液褪色
【解析】试题分析:(1)铜与浓硝酸反应生成硝酸铜、二氧化氮、水;铜丝可以抽动,能控制反应的速率;(2)NO2有毒,G中可以盛放氢氧化钠(或碱石灰)吸收NO2;(3)Mg与CO2反应生成氧化镁和碳, Mg与NO2反应生成氧化镁和氮气;装置D(内装NaOH溶液)可以吸收)NO2,氮气难溶于水,若装置E中收集到气体,该气体是N2;(4)①NO2被Na2O2氧化,则生成硝酸盐;②NO2被Na2O2还原,则生成亚硝酸盐,亚硝酸盐可以被高锰酸钾氧化;
解析:(1)铜与浓硝酸反应生成硝酸铜、二氧化氮、水,反应离子方程式是Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;通过抽动铜丝可以控制反应的速率;(2)NO2有毒,G中可以盛放氢氧化钠(或碱石灰)吸收NO2,避免污染环境;(3)Mg与NO2反应生成氧化镁和氮气,反应方程式是Mg+2NO2![]() 4MgO+N2;装置D(内装NaOH溶液)可以吸收)NO2,氮气难溶于水,若装置E中收集到气体,则证明装置C中发生反应生成N2;(4)①NO2被Na2O2氧化,则生成硝酸盐,白色固体是NaNO3;②NO2被Na2O2还原,则生成亚硝酸盐,亚硝酸盐可以被高锰酸钾氧化,所以高锰酸钾溶液褪色。
4MgO+N2;装置D(内装NaOH溶液)可以吸收)NO2,氮气难溶于水,若装置E中收集到气体,则证明装置C中发生反应生成N2;(4)①NO2被Na2O2氧化,则生成硝酸盐,白色固体是NaNO3;②NO2被Na2O2还原,则生成亚硝酸盐,亚硝酸盐可以被高锰酸钾氧化,所以高锰酸钾溶液褪色。


科目:高中化学 来源: 题型:
【题目】某饱和一元醛发生银镜反应时可析出21.6克银,等量的此醛完全燃烧可生成8.96升CO2(标准状况),则该醛是
A. 乙醛 B. 2—甲基丁醛 C. 丁醛 D. 己醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨硼烷(NH3·BH3)作为一种非常有前景的储氢材料,近年来日益受到人们的重视。氨硼烷(NH3·BH3)电池可在常温下工作,装置如下图所示。该电池的总反应为:NH3·BH3+3H2O2=NH4BO2+4H2O。下列说法正确的是( )

A. 右侧电极发生氧化反应 B. 电池工作时,H+通过质子交换膜向左侧移动
C. 负极的电极反应式为H2O2+2H++2e-=2H2O D. 每消耗31g氨硼烷,理论上应转移6mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在一定容积的密闭容器中加入NH3和O2各1mol,发生反应:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)。下列说法中,表明该反应达到化学平衡状态的是
4NO(g)+6H2O(g)。下列说法中,表明该反应达到化学平衡状态的是
A. 反应速率不再变化 B. NH3和NO的反应速率相等
C. 气体的密度不再变化 D. NO和H2O浓度比不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置,下列叙述不正确的是( )

A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铜片上发生的反应为Cu2++2e-![]() Cu
Cu
C. 无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色
D. a和b分别连接直流电源正、负极,电压足够大时,Cu2+向铜电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X是一种具有果香味的合成香料,下图为合成X的某种流程:
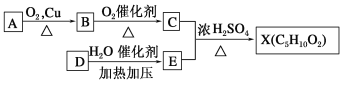
提示:①![]() 不能最终被氧化为-COOH;
不能最终被氧化为-COOH;
②D的产量可以用来衡量一个国家的石油化工水平。
请根据以上信息,回答下列问题:
(1)A分子中官能团的名称是__________,E的结构简式是________。
(2)D→E的化学反应类型为________反应。
(3)上述A、B、C、D、E、X六种物质中,互为同系物的是________。
(4)C的一种同分异构体F可以发生水解反应,则F的结构简式为________、________。
(5)反应C+E→X的化学方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,某浓度的碳酸中含碳微粒的物质的量浓度的对数值与溶液的pH的关系如下图所示。下列说法正确的是( )
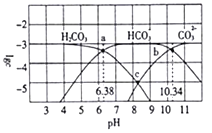
A. lgKa1(H2CO3)=6.38
B. C点对应溶液的pH=8.36
C. 溶液的pH=8时,c(HCO3-)>c(OH-)>c(CO32-)
D. 25℃时,反应CO32-+H2CO3=2HCO3-的平衡常数对数值1gK=-6.96
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.乙烯的分子式可写成(CH2)2
B.乙烯的结构简式为CH—CH
C.乙烯与HCl反应生成CH3CH2Cl
D.乙烯的结构简式为CH2CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验中,用镊子从煤油中取出一小块金属钠,然后用滤纸将煤油吸干,再用小刀切开观察。在这一实验过程中不能得出的钠的物理性质是
A. 钠在常温下是固体 B. 钠的熔点很低
C. 钠具有银白色的金属光泽 D. 金属钠很软
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com