
【题目】25℃时,某浓度的碳酸中含碳微粒的物质的量浓度的对数值与溶液的pH的关系如下图所示。下列说法正确的是( )
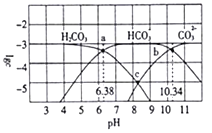
A. lgKa1(H2CO3)=6.38
B. C点对应溶液的pH=8.36
C. 溶液的pH=8时,c(HCO3-)>c(OH-)>c(CO32-)
D. 25℃时,反应CO32-+H2CO3=2HCO3-的平衡常数对数值1gK=-6.96
 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G为7种短周期主族元素,其原子序数依次增大。A、C可形成A2C和A2C2两种化合物,B的最高正化合价与最低负化合价的绝对值之差为2,D和A同主族,E是地壳中含量最高的金属元素,F和C同主族且可形成FC2和FC3两种化合物。
(1)G的元素名称是__________,它在元素周期表中的位置是______________。
(2)F的质子数和中子数相等,F的原子组成符号为______,它的最高价为____价。
(3)C、D可形成一种淡黄色固体化合物,写出此化合物的电子式__________。
(4)由上述7种元素中的4种元素组成的化合物X,X既能与热的NaOH溶液反应,也能与稀盐酸反应,且均能生成无色气体,X的化学式是____________________。
(5)已知Se在第四周期,与S同主族,请任意写出一种含Se物质的化学式,预测其性质,并说明预测依据_______。
含Se物质化学式 | 性质 | 预测依据 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成金刚石的新方法化学原理为:①Na+CO2![]() C(金刚石)+C(石墨)+Na2CO3(未配平);方法比人工首次制得金刚石的旧方法:②C(石墨)=C(金刚石)容易得多。以下表述中正确的是
C(金刚石)+C(石墨)+Na2CO3(未配平);方法比人工首次制得金刚石的旧方法:②C(石墨)=C(金刚石)容易得多。以下表述中正确的是
A. 反应②中既有旧化学键的断裂又有新化学键的形成
B. 新方法利用的是化学变化,旧方法利用的是物理变化
C. 在反应①中每生成12 g金刚石需要消耗46 g金属钠
D. 反应①和反应②中所得的金刚石都是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组探究NO2性质,其实验装置如下图所示(夹持和固定装置省去)
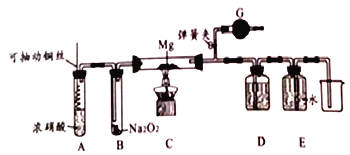
(1)铜与浓硝酸反应的离子方程式为__________,装置A的优点是______________。
(2)G中试剂为_________,作用是________________________。
(3)类比Mg与CO2反应的思路,写出Mg与NO2反应的化学方程式___________________,设计装置D(内装NaOH溶液)和装置E的目的是______________________。
(4)一段时间后,装置B中管壁发烫,瓶内红棕色物质消失,淡黄色粉末变成白色固体(为单一物质)。小组同学认为Na2O2与NO2发生了氧化还原反应,其结果有两种假设:
①NO2被Na2O2氧化,则白色固体是_______(填化学式)。
②NO2被Na2O2还原,为了验证此产物,取适量白色固体于试管中,加蒸馏水溶解,滴加酸性高锰酸钾溶液,则观察到的现象是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. lmol 该有机物( )最多能与4mol 氢气加成
)最多能与4mol 氢气加成
B. 乙醛和丙烯醛(![]() )不是同系物,它们与氢气充分反应后的产物也不是同系物
)不是同系物,它们与氢气充分反应后的产物也不是同系物
C. 乳酸薄荷醇酯( )仅能发生水解、氧化、消去反应
)仅能发生水解、氧化、消去反应
D.  分子中至少有9个碳原子处于同一平面上
分子中至少有9个碳原子处于同一平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,加入3mo1A和1molB,一定条件下发生反应3A(g)+B(g)![]() 2C(g)+D(g),达平衡时,测得C的浓度为wmol·L-1,若保持容器中容积和温度不变,重新按下列配比作起始物质,达到平衡时,C的浓度仍然为wmol·L-1的是
2C(g)+D(g),达平衡时,测得C的浓度为wmol·L-1,若保持容器中容积和温度不变,重新按下列配比作起始物质,达到平衡时,C的浓度仍然为wmol·L-1的是
A. 6molA+2molB B. 1.5molA-0.5molB+1molC+0.5molD
C. 3molA+1molB+2molC+1molD D. 1molB+2molC+1molD
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色化学又称环境友好化学,它的主要特点之一是提高原子的利用率,使原料中所有的原子全部 转化到产品中,实现“零排放”。下列反应符合绿色化学这一特点的是
A. 工业冶炼 Fe2O3+3CO ![]() 2Fe+3CO2
2Fe+3CO2
B. 用生石灰制熟石灰 CaO+H2O=Ca(OH)2
C. 实验室制取二氧化碳 CaCO3+2HCl=CaCl2+H2O+CO2↑
D. 实验室制取氢气 Zn+H2SO4=ZnSO4+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当用酸滴定碱时,下列操作中使测定结果(碱的浓度)偏低的是( )
A. 酸式滴定管滴至终点后,俯视读数
B. 碱液移入锥形瓶后,加入了10mL蒸馏水再滴定
C. 酸式滴定管用蒸馏水润洗后,未用操作液洗
D. 酸式滴定管注入酸液后,尖嘴留有气泡,开始滴定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
用石油产品A(C3H6)为主要原料,合成具有广泛用途的有机玻璃PMMA。流程如图 (部分产物和条件省略) :

试回答下列问题:
(1)A的结构式为__________;在同一平面最多原子个数为________,X试剂电子式为________;E中非含氧官能团的名称为________。
(2) E![]() G的化学方程式为______,反应类型是___________。
G的化学方程式为______,反应类型是___________。
(3) T是G的同分异构体,lmolT 与足量新制Cu(OH)2悬独液反应最多生成2molCu2O沉淀,请写出T的所有结构简式: __________(不含立体结构)。
(4) 若高分子化合物PMMA 的相对分子质量为1.5×106,其聚合度为_________.
(5) 参照上述流程,以 为原料合成
为原料合成 (其他原料自选)。设计合成路线_________。
(其他原料自选)。设计合成路线_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com