
【题目】已知:有机物A的产量可以用来衡量一个国家的石油化工发展水平。现以A为主要原料合成乙酸乙酯,其合成路线如图1所示。
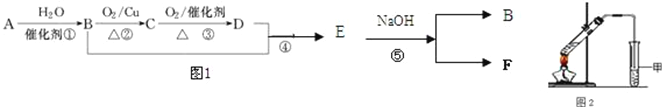
(1)B分子中官能团的名称是________,D中官能团的名称是_________;反应①的反应类型是__________反应。
(2)反应②的化学方程式是________________________________________,反应⑤的化学方程式是_________________________________________________。
(3)①某同学用如图2所示的实验装置制取少量乙酸乙酯.实验结束后,试管甲中上层为透明的、不溶于水的油状液体。上述实验中试管甲中试剂为___________________,其作用是(填字母)_____________。
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
②在实验室利用B和D制备乙酸乙酯的实验中,若用1mol B和1mol D充分反应,_____(能/不能)生成1mol 乙酸乙酯,原因是_____________________________________________________。
【答案】 羟基 羧基 加成 2CH3CH2OH+O2![]() 2CH3CHO+2H2O CH3COOCH2CH3+NaOH
2CH3CHO+2H2O CH3COOCH2CH3+NaOH![]() CH3COONa+CH3CH2OH 饱和Na2CO3溶液 BC 不能 该反应为可逆反应,有一定的限度,不可能完全转化
CH3COONa+CH3CH2OH 饱和Na2CO3溶液 BC 不能 该反应为可逆反应,有一定的限度,不可能完全转化
【解析】分析:有机物A的产量可以用来衡量一个国家的石油化工发展水平,A是乙烯。乙烯与水发生加成反应生成B是乙醇,乙醇发生催化氧化生成C是乙醛,乙醛发生氧化反应生成D是乙酸,乙酸与乙醇发生酯化反应生成E是乙酸乙酯,乙酸乙酯在氢氧化钠溶液中水解生成乙醇和F乙酸钠,据此解答。
详解:根据以上分析可知A是乙烯,B是乙醇,C是乙醛,D是乙酸,E是乙酸乙酯,F是醋酸钠。则
(1)B是乙醇,分子中官能团的名称是羟基,D是乙酸,分子中官能团的名称是羧基;反应①是乙醇与水的加成反应。
(2)反应②是乙醇的催化氧化,反应的化学方程式是2CH3CH2OH+O2![]() 2CH3CHO+2H2O,反应⑤是乙酸乙酯的水解反应,反应的化学方程式是CH3COOCH2CH3+NaOH
2CH3CHO+2H2O,反应⑤是乙酸乙酯的水解反应,反应的化学方程式是CH3COOCH2CH3+NaOH![]() CH3COONa+CH3CH2OH。
CH3COONa+CH3CH2OH。
(3)①由于生成的乙酸乙酯中含有乙酸和乙醇,因此需要利用饱和碳酸钠溶液除杂,其主要作用是中和乙酸并吸收部分乙醇、降低乙酸乙酯的溶解度,便于分层析出,答案选BC;
②由于酯化反应是可逆反应,有一定的限度,不可能完全转化,所以用1mol B和1mol D充分反应,不能生成1mol 乙酸乙酯。


科目:高中化学 来源: 题型:
【题目】一种用于驱动潜艇的液氨-液氧燃料电池原理示意如图,下列有关该电池说法正确的是

A. 电子由电极A经外电路流向电极B
B. 该电池工作时,每消耗22.4L NH3转移3mol电子
C. 电池工作时,OH-向电极B移动
D. 电极B上发生的电极反应为:O2+ 4H++ 4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组学生用![]() 的盐酸与
的盐酸与![]() 的NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量计算反应热。下列说法错误的是
的NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量计算反应热。下列说法错误的是
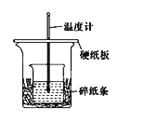
A.如图条件下实验过程中有热量损失
B.图中实验装置缺少环形玻璃搅拌棒
C.烧杯间填满碎纸条的作用是固定小烧杯
D.若改用![]() 的NaOH溶液进行反应,所放出热量相等
的NaOH溶液进行反应,所放出热量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一处于平衡状态的反应:X(s)+3Y(g)![]() 2Z(g);△H<0.为了使平衡向生成Z的方向移动,应选择的条件是( )
2Z(g);△H<0.为了使平衡向生成Z的方向移动,应选择的条件是( )
①高温 ②低温 ③高压 ④低压 ⑤加催化剂 ⑥分离出Z ⑦增加X ⑧增加Y
A.①③⑤⑦B.②③⑤⑦C.②③⑥⑧D.②④⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,磷酸二氢钾(KH2PO4)大晶体已应用于我国研制的巨型激光器“神光二号”中。利用氟磷灰石(化学式为Ca5P3FO12)制备磷酸二氢钾的工艺流程如下图所示(部分流程步骤已省略):
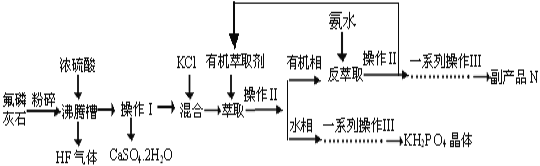
已知萃取的主要反应原理:KCl+H3PO4![]() KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
KH2PO4+HCl;其中,反应产生的HCl易溶于有机萃取剂。
请回答下列问题:
(1)流程中将氟磷灰石粉碎的目的是__________________________________。
(2)不能使用二氧化硅陶瓷材质的沸腾槽的主要原因是___________________(用化学方程式表示)。
(3)副产品N的化学式是____________;在得到KH2PO4晶体的一系列操作Ⅲ,其主要包括______________________________、过滤、洗涤、干燥等。
(4)若用1000kg质量分数为50.4%的氟磷灰石(化学式为Ca5P3FO12)来制取磷酸二氢钾晶体,其产率为80%,则理论上可生产KH2PO4的质量为_______kg。
(5)电解法制备KH2PO4的装置如图所示.该电解装置中,a 区属于_______区(填“阳极”或“阴极”),阴极区的电极反应式是______________________________________。

(6)工业上还可以用氟磷灰石与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,同时逸出SiF4和CO,该反应的化学方程式为________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据烃类化合物和烃类衍生物的有关知识回答下列问题:
(1)用系统命名法命名下列物质
①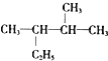 ___________________________________;
___________________________________;
②![]() _____________________________________;
_____________________________________;
(2)某有机物含C、H、O三种元素,分子模型如图所示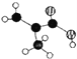 (图中球与球之间的连线代表化学键,如单键、双键等)。该有机物的结构简式为 _______,所含官能团的名称为 __________。
(图中球与球之间的连线代表化学键,如单键、双键等)。该有机物的结构简式为 _______,所含官能团的名称为 __________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应热和热化学方程式的描述中正确的是( )
A. HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的反应热ΔH=2×(-57.3) kJ·mol-1
B. CO(g)的燃烧热是283.0 kJ·mol-1,则反应2CO2(g) =2CO(g)+O2(g)的ΔH=+2×283.0 kJ·mol-1
C. 氢气的燃烧热为285.5 kJ·mol-1,则分解水的热化学方程式为2H2O(l) =2H2(g)+O2(g) ΔH=+285.5 kJ·mol-1
D. 1 mol甲烷完全燃烧生成气态水和二氧化碳时所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)研究大气中含硫化合物(主要是 SO2 和 H2S)的转化具有重要意义。
(1)工业上采用高温热分解H2S的方法制取H2,在膜反应器中分离H2,发生的反应为: 2H2S(g) ![]() 2H2(g)+S2(g) ΔH
2H2(g)+S2(g) ΔH
已知:①H2S(g) ![]() H2(g)+S(g) ΔH1; ②2S(g)
H2(g)+S(g) ΔH1; ②2S(g) ![]() S2(g) ΔH2。
S2(g) ΔH2。
则 ΔH=________________(用含 ΔH1、ΔH2的式子表示)。
(2)土壤中的微生物可将大气中 H2S 经两步反应氧化成 SO42-,两步反应的能量变化示意图如下:

1mol H2S(g)全部氧化成SO42-(aq)的热化学方程式为________________。
(II)100℃时,在1L恒温恒容的密闭容器中,通入0.1mol N2O4,发生反应:N2O4(g) ![]() 2NO2(g) ΔH=+57.0kJ·mol-1,NO2和N2O4的浓度随时间变化情况如图所示。
2NO2(g) ΔH=+57.0kJ·mol-1,NO2和N2O4的浓度随时间变化情况如图所示。
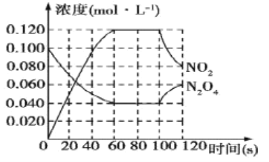
(3)在0~60s内,以N2O4表示的平均反应速率为__________mol·L-1·s-1。
(4)根据图中有关数据,计算100℃时该反应的平衡常数K1=__________。若其他条件不变,升高温度至120℃,达到新平衡时的平衡常数是K2,则K1_____K2(填“>”、“<”或“=”)。
(III)向容积为2L的密闭容器中通入一定量的CO和H2O,发生反应:CO(g)+H2O(g) ![]() H2(g)+CO2(g)。
H2(g)+CO2(g)。
(5)下列说法能作为判断该反应达到化学平衡状态的依据的是____(填字母序号)。
A.容器内CO、H2O、CO2、H2的浓度之比为1:1:1:1
B.CO的消耗速率与H2的消耗速率相等
C.容器内压强保持不变
D.混合气体的密度保持不变
(6)保持其他条件不变:在VL密闭容器中通入10molCO和10molH2O(g)发生上述反应,在T℃达到平衡,然后急速除去水蒸气(除水蒸气时其他各成分的物质的量不变),将混合气体燃烧,测得放出的热量为2842kJ(已知CO的燃烧热为283kJ·mol-1,H2的燃烧热为286kJ·mol-1),则T℃平衡常数K=______。(精确到小数点后两位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 检验KIO3中的碘元素 | 取少量KIO3晶体溶于适量的蒸馏水,再加入硝酸酸化的AgNO3溶液 |
B | 检验石油裂解气中的乙烯 | 将混合气体通入足量酸性KMnO4溶液中 |
C | 比较HClO和CH3COOH的酸性强弱 | 室温下,用pH计测定饱和的NaClO溶液和饱和的 |
D | 硅酸胶体的制备 | 向 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com