
【题目】连二亚硫酸钠(Na2S2O4)是印染工业的一种常用原料,又称保险粉,是一种白色粉末,易溶于水,但不溶于乙醇,在碱性介质中稳定。
(1)Na2S2O4中S元素的化合价为____。
(2)连二亚硫酸钠在潮湿空气中极不稳定,易分解并引起燃烧,甚至发生爆炸,反应的化学方程式为:2Na2S2O4=Na2S2O3+Na2SO3+___。保存“保险粉”时常加入少量Na2CO3固体,目的是___。
(3)Na2S2O4暴露于空气中易吸收氧气和水蒸气而变质,当氧化剂和还原剂的物质的量之比为1:2时,反应产物的化学式为____。
(4)工业上可用如图装置电解NaHSO3和NaC1溶液制Na2S2O4。总反应为:2NaHSO3+2NaC1![]() Na2S2O4+2NaOH+C12↑
Na2S2O4+2NaOH+C12↑

①惰性电极a连接电源的____(填“正极”或“负极”),其电极反应式为____;
②若不加隔膜,则连二亚硫酸钠产率降低,其原因是____。
向银离子的乙二胺四乙酸(EDTA)配合物溶液中,滴加用NaOH碱化的连二亚硫酸钠溶液可生成纳米级银粉,该方法能用来测定Na2S2O4纯度,其反应原理可简单表示为:2Ag++S2O42-+4OH-=2Ag↓+2SO32-+2H2O。现取5.000g粗产品用上述方法测定纯度,将制得纳米级银过滤、洗涤、干燥、称量,其质量为4.320g。计算粗产品中连二亚硫酸钠的质量分数为____。测得连二亚硫酸钠的纯度比实际值小,若排除实验过程中的操作误差,分析可能的原因是____。
【答案】+3 SO2 Na2CO3为碱性物质,可提高“保险粉”的稳定性 NaHSO3 负极 2HSO3-+2e-=S2O42-+2OH- 若不加隔膜,则部分HSO3-到阳极失电子、发生氧化反应生成硫酸根离子,使连二亚硫酸钠产率下降 69.6% 连二亚硫酸钠具有强还原性,部分被空气中的氧气氧化
【解析】
(1)化合物中元素化合价代数和为0;
(2)根据化学反应前后原子种类和数目不变分析解答;由题给信息可知,Na2S2O4在碱性介质中稳定,加入少量Na2CO3固体可防止其分解;
(3)根据电子守恒计算生成物中S的化合价,结合原子守恒推断生成物;
(4)①NaHSO3转化为Na2S2O4,元素化合价降低,亚硫酸氢钠发生得到电子发生还原反应,则a电极为阳极,结合电子守恒、电荷守恒写出电极反应式;
②若不加隔膜,则HSO3-到阳极失电子发生氧化反应生成硫酸根离子,导致连二亚硫酸钠的产率降低;
(5)根据方程式可知n(Na2S2O4)与n(Ag),结合m=nM和质量分数公式计算粗产品中连二亚硫酸钠的质量分数;
由于连二亚硫酸钠具有强还原性,易被空气中氧气氧化,据此分析解答。
(1)Na2S2O4中Na的化合价为+1、O为-2,根据化合物中元素化合价代数和为0计算得出S元素的化合价为+3,故答案为:+3;
(2)根据反应前后原子种类和数目不变可知,Na2S2O4分解还生成SO2气体;Na2S2O4在碱性介质中稳定,加入少量Na2CO3固体可防止其分解,故答案为:SO2;Na2CO3为碱性物质,可提高“保险粉”的稳定性;
(3)Na2S2O4具有强还原性,和O2以2:1反应时,1molO2得到4mol电子、2molNa2S2O4失去4mol电子,所以S的化合价升高1,即生成物中S的化合价为+4,由于Na2S2O4氧气和水蒸气而变质生成+4价生成物,所以生成物为NaHSO3,故答案为:NaHSO3;
(4)由总反应2NaHSO3+2NaC1![]() Na2S2O4+2NaOH+C12↑可知,S的化合价降低、Cl化合价升高,所以NaHSO3在阴极发生得电子的还原反应生成Na2S2O4,即惰性电极a为阴极,与电源负极相接,电极反应式为 2HSO3-+2e-=S2O42-+2OH-;若不加隔膜,则部分HSO3-转移到阳极、被阳极生成的氯气氧化生成硫酸根离子,使连二亚硫酸钠产率下降,故答案为:负极;2HSO3-+2e-=S2O42-+2OH-;若不加隔膜,则部分HSO3-到阳极失电子、发生氧化反应生成硫酸根离子,使连二亚硫酸钠产率下降(或部分HSO3-被阳极产生的 Cl2氧化生成SO42-,使连二亚硫酸钠产率下降);
Na2S2O4+2NaOH+C12↑可知,S的化合价降低、Cl化合价升高,所以NaHSO3在阴极发生得电子的还原反应生成Na2S2O4,即惰性电极a为阴极,与电源负极相接,电极反应式为 2HSO3-+2e-=S2O42-+2OH-;若不加隔膜,则部分HSO3-转移到阳极、被阳极生成的氯气氧化生成硫酸根离子,使连二亚硫酸钠产率下降,故答案为:负极;2HSO3-+2e-=S2O42-+2OH-;若不加隔膜,则部分HSO3-到阳极失电子、发生氧化反应生成硫酸根离子,使连二亚硫酸钠产率下降(或部分HSO3-被阳极产生的 Cl2氧化生成SO42-,使连二亚硫酸钠产率下降);
(5)方程式2Ag++S2O42-+4OH-=2Ag↓+2SO32-+2H2O可知,n(Na2S2O4)=![]() n(Ag)=0.5×
n(Ag)=0.5×![]() =0.02mol,m(Na2S2O4)=nM=0.02mol×174g/mol=3.480g,所以粗品中连二亚硫酸钠的质量分数为
=0.02mol,m(Na2S2O4)=nM=0.02mol×174g/mol=3.480g,所以粗品中连二亚硫酸钠的质量分数为![]() ×100%=69.6%;
×100%=69.6%;
由于连二亚硫酸钠具有强还原性,易被空气中的氧气氧化导致粗品中连二亚硫酸钠的质量减少,故答案为:69.6%; 连二亚硫酸钠具有强还原性,部分被空气中的氧气氧化(或生成的纳米级的银粉有部分穿过滤纸进入滤液中导致银质量减少)。


科目:高中化学 来源: 题型:
【题目】天然气是一种重要的清洁能源和化工原料,其主要成分为甲烷。
I.(1)已知:一定条件下![]() 可被甲烷还原“纳米级”的金属铁。其反应为:
可被甲烷还原“纳米级”的金属铁。其反应为:
![]()
①此反应的化学平衡常数表达式为______
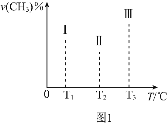
②在容积均为VL的I、II、III三个相同密闭容器中加入足量![]() ,然后分别充入amol
,然后分别充入amol![]() ,三个容器的反应温度分别为
,三个容器的反应温度分别为![]() 、
、![]() 、
、![]() 且恒定不变,在其他条件相同的情况下,实验测得反应均进行到tmin时
且恒定不变,在其他条件相同的情况下,实验测得反应均进行到tmin时![]() 的体积分数如图1所示,此时I、II、III三个容器中一定处于化学平衡状态的是______;上述反应的
的体积分数如图1所示,此时I、II、III三个容器中一定处于化学平衡状态的是______;上述反应的![]() ______
______![]() 填“大于”或“小于”
填“大于”或“小于”![]() ,该反应在______
,该反应在______![]() 填“高温”、“低温”或“任意温度”
填“高温”、“低温”或“任意温度”![]() 下可自发进行。
下可自发进行。
![]() 利用天然气为原料的一种工业合成氨简式流程图如图2:
利用天然气为原料的一种工业合成氨简式流程图如图2:
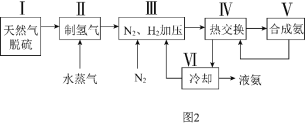
(1)步骤Ⅱ中制氢气的原理如下:Ⅰ![]() ;
;![]()
Ⅱ![]() ;
;![]()
①对于反应Ⅰ,在一定温度下的恒容容器中,表示其已达到最大化学反应限度的叙述正确的是______。
A.单位时间内1mol![]() 消耗,同时有3mol
消耗,同时有3mol![]() 生成;
生成;
B.![]() 、
、![]() 、CO的物质的量浓度相等;
、CO的物质的量浓度相等;
C.混合气体的密度不再改变;
D.混合气体的压强不再改变。
②则反应![]() ;
;![]() ______
______![]() 用含
用含![]() 、
、![]() 的代数式表示
的代数式表示![]() 。
。
(2)合成氨是人类科学技术上的一项重大突破,反应原理为:![]() 在容积为10L的密闭容器中进行,起始时充入
在容积为10L的密闭容器中进行,起始时充入![]()
![]() 、
、![]()
![]() 反应在不同条件下进行,反应体系总压强随时间的变化如图3所示。
反应在不同条件下进行,反应体系总压强随时间的变化如图3所示。
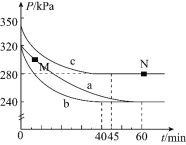
①实验a从开始至平衡时的反应速率![]() ______;实验c中
______;实验c中![]() 的平衡转化率
的平衡转化率![]() 为______。
为______。
②与实验a相比,其他两组改变的实验条件是:b______,c______。
③M点的逆反应速率![]() ______N点的正反应速率
______N点的正反应速率![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() ;N点时再加入一定量
;N点时再加入一定量![]() ,平衡后
,平衡后![]() 的体积分数______
的体积分数______![]() 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变”![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=-24.8kJ·mol-1
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH=-47.2kJ·mol-1
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH=+640.5kJ·mol-1
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:___。
(2)微型纽扣电池在现代生活中应用广泛。有一种银锌电池,其电极材料分别是Ag2O和Zn,电解质溶液为KOH溶液,总反应是Zn+Ag2O=ZnO+2Ag。请回答下列问题。
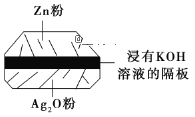
①该电池属于___电池(填“一次”或“二次”)。
②负极材料是___,电极反应式是___。
③使用时,正极区的pH__(填“增大”“减小”或“不变”,下同),电解质溶液的pH___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学研究性学习小组设计如下实验方案,测定NaHCO3和Na2CO3混合物中NaHCO3的质量分数。
方案一:按下图装置进行实验。并回答以下问题。
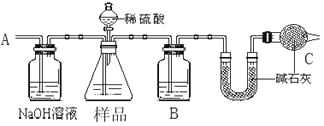
①按图组装仪器并检查装置的气密性。
②实验前称取17.90g样品,从分液漏斗滴入6mol·L-1的硫酸,直到不再产生气体时为止, 从导管A处缓缓鼓入一定量的空气。
③实验结束后测得U型管增重 8.80g。
(1)B瓶中装的试剂为______,C装置的作用是__________________________。
(2)从导管A处缓缓鼓入一定量的空气的目的是_______________。
(3)该样品中NaHCO3的质量分数为_____________。
方案二:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量Ba(OH)2溶液。过滤洗涤,干燥沉淀,称量固体质量,进行有关计算。
请回答:实验中判断沉淀是否完全的方法是_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M(结构式如下图)是最常用的还原剂,由H·C· Brown和 Schlesinger于1942年在芝加哥大学发现,其中X、Y、Z是原子序数依次减小的不同短周期主族元素,X与W、Z与W均能形成原子个数比为1:1和2:1的化合物,W原子的最外层电子数是电子层数的3倍,下列叙述正确的是( )
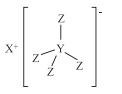
A.Y的最高价氧化物对应的水化物是一种一元弱酸
B.Z元素位于第3周期第ⅦA族
C.X和Z形成的化合物的水溶液呈酸性
D.化合物M不能与Z2W2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]铬元素在地壳中含量占第21位,是一种重要的金属。回答下列问题:
(1)基态铬原子的价电子排布式为_________________,根据价层电子判断铬元素中最高价态为___________价。铬元素的第二电离能________锰元素的第二电离能(填“>”“<”填“=”)。
(2)无水氯化亚铬(CrCl2)的制备方法为在500℃时用含HCl的H2气流还原CrCl3,该过程涉及到的反应原理为____________________________________________(用化学方程式表示)。
已知:氯化亚铬的熔点为820~824℃,则其晶体类型为___________晶体。二价铬还能与乙酸根形成配合物,在乙酸根中碳原子的杂化形式为___________
(3)已知CrO5中铬元素为最高价态,画出其结构式:______________________
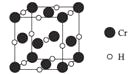
(4)Cr元素与H元素形成化合物的晶胞结构如图所示,则该化合物的化学式为___________。已知:该晶胞的边长为437.6 pm,NA表示阿伏加德罗常数的值,则晶体的密度为____g/cm3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)写出下列物质在水中电离方程式:
NaHSO4_____________________________NH3·H2O______________________________________________________
(2)写出下列物质水解的离子方程式:
NaHCO3___________________________ FeCl3_____________________________
(3)常温时,0.1mol/L的NaOH和0.06mol/L 的H2SO4溶液等体积混合,求混合溶液的pH为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于金属腐蚀的叙述中,正确的是( )
A.金属被腐蚀的本质是M+nH2O=M(OH)n+![]() H2↑
H2↑
B.马口铁(镀锡铁)镀层破损后被腐蚀时,首先是镀层被氧化
C.金属在一般情况下发生的电化学腐蚀主要是吸氧腐蚀
D.常温下,置于空气中的金属主要发生化学腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组为了探究固体甲(含两种元素)和固体乙(无机矿物盐,含五种元素)的组成和性质,设计并完成了如下实验:
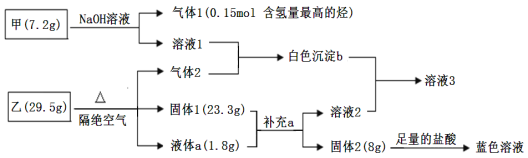
已知:向溶液1中连续滴加盐酸,先产生白色沉淀,后沉淀溶解;向溶液2中连续通入气体2,也是先产生白色沉淀,后沉淀溶解。请回答下列问题:
(1)甲的化学式____________,乙的化学式______________。
(2)加热条件下,气体1与固体2反应,产物中有一种气体和一种固体,该反应的化学方程式为__________________。
(3)气体2与足量溶液1反应的离子方程式为____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com