
����Ŀ�� �����£���20 mL 0.01mol/L CH3COOH��Һ����μ���0.01mol/L ��NaOH��Һ����Һ��ˮ���������c(H+)�����NaOH��Һ������仯ʾ��ͼ��ͼ��ʾ������˵������ȷ����

A����a��c������ĵ���ʼ���ܵ��ٽ�
B��a��d��Ӧ����������ֵ�ֱ��ǣ���10-12����10-7
C��b�㣺2c(Na+)��c(CH3COO-)��c(CH3COOH)
D����b��c�Ĺ����У��ȴ�����pH=7�ĵ㣬Ҳ��������Һ��ˮ���������c(H+)=10-7�ĵ�
���𰸡�B
��������
���������A��������Һ�д���CH3COOHCH3COO-+H+����NaOH��Һ���������ӣ�����ĵ���ƽ�����ƣ����Դ�a��c������ĵ���ʼ���ܵ��ٽ�����A��ȷ��B��a����Ჿ�ֵ��룬��������������Ũ��С��0.01mol/L������ˮ�����������Ũ�ȣ�10-12mol/L��d�㣬NaOH������pH����7��ˮ�ĵ��뱻���ƣ���d��ˮ�����������Ũ�ȣ�10-7mol/L����B����C��c�㣬��������ʵ�����NaOH�����ʵ���2������Һ�������غ�Ϊ2c��Na+��=c��CH3COO-��+c��CH3COOH������C��ȷ��D��c�㣬��������������ǡ�÷�Ӧ���ɴ����ƣ���Һ�Լ��ԣ������������С��20mLʱ��ijһ��ֵǡ��ʹ��Һ�����ԣ����Դ�b��c�Ĺ����У��ȴ�����pH=7�ĵ㣬Ҳ��������Һ��ˮ���������c��H+��=10-7�ĵ㣬��D��ȷ����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؾ���������У��������
A.�Ȼ��ƾ����У�ÿ��Na+��Χ��������������Na+����6��
B.���������У��ԡ���ABCABCABC������ʽ�Ķѻ���Ϊ���������ѻ�
C.�ɱ������У�ÿ��CO2������Χ��������������CO2���ӹ���12��
D.���ʯ��״�ṹ�У��ɹ��ۼ��γɵ�̼ԭ�ӻ��У���С�Ļ�����6��̼ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪25��ʱ��
��HF(aq)��OH��(aq)=F��(aq)��H2O(l) ��H1����67.7 kJ��mol��1
��H��(aq)��OH��(aq)=H2O(l) ��H2����57.3 kJ��mol��1
��Ba2��(aq)��SO42��(aq)=BaSO4(s) ��H3��0
����˵����ȷ����(����)
A.HF�ĵ��뷽��ʽ����ЧӦ��HF(aq)=H��(aq)��F��(aq) ��H��0
B.������������Һ������ķ�Ӧ�У�������һ��������������Һ��Խ�࣬�к���Խ��
C.��H2����57.3 kJ��mol��1��ǿ���ǿ����ϡ��Һ�з�Ӧ���ɿ����ε��к���
D.ϡ������ϡ����������Һ��Ӧ���Ȼ�ѧ����ʽΪH2SO4(aq)��Ba(OH)2(aq)=BaSO4(s)��2H2O(l)��H����114.6 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУ��ȤС���ͬѧΧ��Fe3+��S2-�ķ�Ӧ�������˼��ҵ����磬����������������Ӧ�ļ�¼
(1)��ͬѧ��Ϊ��������Fe3+��I-��Fe3+��S2-Ҳ�ܷ���������ԭ��Ӧ�����У���ͬѧ�ᵽ��Fe3+��I-������Ӧ�����ӷ���ʽ��______��
(2)��ͬѧ��Ϊ��ͬѧ����Ƿ�ܣ�����ΪFe3+��S2-������Ӧ�����ӷ���ʽ���ܸ��μ�˳���йء���������Ȼ�����Һ����μ���������Һ�����ӷ���ʽ������(1)�е����ӷ���ʽ���������������Һ����μ����Ȼ�����Һ�����ӷ���ʽ��������ͬ��Ӧ��Ϊ______��
(3)��ͬѧ�Ŀ�����ף�����λͬѧ����ͬ����Ȼ��ȣ�������������![]() ��
��![]() �ķ�Ӧ��ȡ�����˵������ͬѧԤ�ڵ�Fe3+��S2-������Ӧ�����ӷ���ʽӦΪ______��
�ķ�Ӧ��ȡ�����˵������ͬѧԤ�ڵ�Fe3+��S2-������Ӧ�����ӷ���ʽӦΪ______��
(4)������ͼ���λͬѧ���ˣ���Լ������ʵ���ҡ����ж�ͬѧ����������ʵ�飺��ȡ______gFeCl3���������ձ��У���______�ܽ⣬�ټ�����ˮ���100 mL��Һ���á�ȡ2 mL1 mol/L��FeCl3��Һ���Թ��У���εμ�0.1 mol/L��Na2S��Һ����ʼ�ֲ����������ĺ�ɫ����������ɫ����������ʧ(��������ɫ����������ʧ)��ͬʱ��Һ��dz��ɫ���ǣ����������ĺ��ɫ��״�����������ŵ����ij�������ζ���μӵ�5��Na2S��Һʱ����Һ��ʼ��������������ɫ����������������ʧ�������μ�Na2S��Һ������������������ͬѧ������ʵ�����ͬѧ������ʵ��ֻ�ڵμ�˳���ϴ��ڲ�ͬ���պ��γɲ��䡣������ͬѧ��ʵ�����______��
(5)��ͬѧ����ͬѧ��ʵ������еõ��ĺ�ɫ����A����ͬʵ�������е�FeSҩƷ(������)һ����������Сʵ�顣
ʵ������ | ʵ������ |
��A+H2O | ��������������������ڣ�����Ҳ���ܽ⣬��Һ��ɫҲ���ı䣬��û�г�������ζ���������� |
��A+HCl | ��ɫ�����ܽ⣬�����ִ���dz��ɫ�����������г�������ζ���������� |
��FeS+HCl | ���ɴ�����������ζ�����壬��û��dz��ɫ�������� |
������ͬѧ��ʵ���֪����ɫ����A����Ϊ______![]() �ѧʽ
�ѧʽ![]() ���������Ի������Һ�����ȶ����ڡ��ݴ˿�֪��������Һ�м��������Ȼ�����Һ�����ӷ���ʽ����Ϊ______��
���������Ի������Һ�����ȶ����ڡ��ݴ˿�֪��������Һ�м��������Ȼ�����Һ�����ӷ���ʽ����Ϊ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��� 0.1000 mol��L��1 NaOH��Һ�ζ� 20.00 mL 0.1000 mol��L��1 CH3COOH��Һ��������Һ��pH�����NaOH��Һ������仯����ͼ������˵����ȷ����

A.V(NaOH)��5 mL��c(Na��)��c(CH3COO��)
B.V(NaOH)��10 mL��c(Na��)��c(CH3COO��)
C.pH��7��c(Na��)��c(CH3COOH)��c(CH3COO��)
D.V(NaOH)��15 mL��3c(CH3COOH)��4c(H��)��c(CH3COO��)��4c(OH��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.������ȼ����Ϊ285 . 5KJ/mol ������ˮ���Ȼ�ѧ����ʽΪ2H2O(l)![]() 2H2(g)+O2(g) ��H=+285.5kJ/mol
2H2(g)+O2(g) ��H=+285.5kJ/mol
B.��֪H+(aq)+OH-(aq)=H2O(l) ��H= -57.3 kJ/mol����ϡH2SO4��Һ��ϡBa(OH)2��Һ��Ӧ�ķ�Ӧ����H=2 ��(-57.3) kJ/mol
C.��CO2�У�Mgȼ������MgO��C���÷�Ӧ�л�ѧ��ȫ��ת��Ϊ����
D.��֪AX3���۵�ͷе�ֱ�Ϊһ93 .6���76�棬 AX5���۵�Ϊ167�档����ʱAX3������X2��Ӧ����1 mol AX5���ų�����123.8 KJ/mol���÷�Ӧ���Ȼ�ѧ����ʽΪAX3(l)+ X2(g)= AX5(s) ��H= һ123.8 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڸ�ͼ��Ľ��ͻ�ó��Ľ�����ȷ����

A��ͼ1��ʾ��0.10 mol��L��1 NaOH��Һ�ζ�20.00 mL 0.10 mol��L��1������Һ�ĵζ�����
B��ͼ2��ʾ������Һ��ͨ�백����������������Һ������I�ı仯
C������ͼ3��ʾ��֪��ʯī�Ƚ��ʯ�ȶ�
D��ͼ4��ʾ��Ӧ2SO2��O2![]() 2SO3��t1ʱ��ֻ��С��SO3��Ũ��
2SO3��t1ʱ��ֻ��С��SO3��Ũ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ��ɽ���ǽ�ɽ�yɽ��������������Ⱦ��ĺ��������Ի�������������Ҫ���塣
(1)����ijЩ�������ɹ�ʵ�ֽ������е�̼��������͵���������ת��Ϊ���Ĵ���ѭ�����ʡ�
��֪����![]()
![]()
��NO(g)+CO(g)![]()
![]() N2(g)+CO2(g)
N2(g)+CO2(g)![]()
��2NO(g)+O2(g)![]() 2NO2(g)
2NO2(g) ![]()
��Ӧ![]() ��
��![]() ________
________![]() ��ij�¶��£���Ӧ�٢ڢ۵�ƽ�ⳣ���քe��
��ij�¶��£���Ӧ�٢ڢ۵�ƽ�ⳣ���քe��![]() ��
��![]() ��
��![]() ����÷�Ӧ��K=________(��
����÷�Ӧ��K=________(��![]() ��
��![]() ��
��![]() ��ʾ)��
��ʾ)��
(2)�¶�Ϊ![]() �慼�����ĸ��ݻ���Ϊ1L�ĺ����ܱ������з�����Ӧ��
�慼�����ĸ��ݻ���Ϊ1L�ĺ����ܱ������з�����Ӧ��
![]()
![]() ������й�ʵ���������£�
������й�ʵ���������£�
������� | ���ʵ���ʼŨ��( | ���ʵ�ƽ��Ũ��( | |
|
|
| |
�� |
|
|
|
�� |
|
| |
�� |
|
| |
�� |
|
| |
��ƽ��ʱ�������������������ѹǿ֮��___________��
���¶Ȳ��䣬�������дﵽƽ����ٳ���NO��![]() (g)��
(g)��![]() mol����Ӧ����_____________��(����������������)������С�
mol����Ӧ����_____________��(����������������)������С�
(3)��������0.100![]() ����ֱ�ζ�10.00mLŨ�Ⱦ�Ϊ0.100
����ֱ�ζ�10.00mLŨ�Ⱦ�Ϊ0.100![]() ��NaOH��Һ�Ͷ��װ�[
��NaOH��Һ�Ͷ��װ�[![]() ]
]

��a��b��c��d�ĵ��ˮ��Һ�У���ˮ�����������Ũ�ȴ���![]()
![]() ����________________��ԭ��Ϊ_____________________��
����________________��ԭ��Ϊ_____________________��
�ڻ�ѧ��Ӧ����������ЧӦ��Ϊ������ϵa���¶�______________(����>������=������<��)c����¶ȡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ά����C�Ľṹ��ʽ��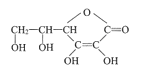 ��ά����C�ܷ��λ�Ѫ����
��ά����C�ܷ��λ�Ѫ����
��1��ά����C�ķ���ʽΪ_____________��
��2��ά����C�к�����������������_______________�������ƣ���
��3����ά����C��Һ�е��뼸����ɫʯ����Һ����Һ��ɫ��죬˵��ά����C��Һ����____�ԡ�
��4��ά����C���л�ԭ�ԡ���ά����C��Һ�е��뼸������KMnO4��Һ������Ϊ_____________
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com