
【题目】亚硝酰氯![]() 是有机物合成中的重要试剂,为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水反应生成一种氢化物和两种氧化物。某学习小组在实验室用
是有机物合成中的重要试剂,为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水反应生成一种氢化物和两种氧化物。某学习小组在实验室用![]() 和NO制备ClNO并测定其纯度。请回答:
和NO制备ClNO并测定其纯度。请回答:
I.甲组的同学拟制备原料气NO和![]() ,制备装置如下图所示:
,制备装置如下图所示:
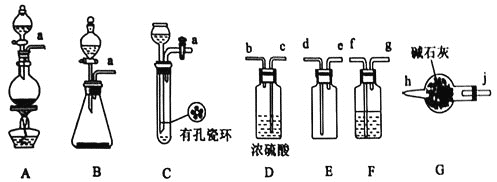
(1)若制备![]() 发生装置选B,则反应的离子方程式为_________________。若制备NO发生装置也选B,锥形瓶中放的是Cu片,则分液漏斗中的试剂为_______。
发生装置选B,则反应的离子方程式为_________________。若制备NO发生装置也选B,锥形瓶中放的是Cu片,则分液漏斗中的试剂为_______。
(2)欲收集一瓶干燥纯净的氯气,选择装置其连接顺序为:![]() ___
___![]() ___
___![]() ___
___![]() ___
___![]() ___
___![]() ___
___![]() 按气流方向,用小写字母表示
按气流方向,用小写字母表示![]() ,其中F装置的作用为________。
,其中F装置的作用为________。
II.乙组同学利用甲组制得的NO和![]() 制备NOCl,装置如图所示:
制备NOCl,装置如图所示:
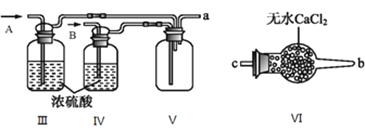
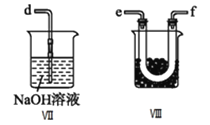
(3)为了使气体充分反应,从A处进入的气体是_______![]() 填
填![]() 或
或![]() 。
。
(4)装置Ⅲ、Ⅳ除可干燥NO、![]() 外,另一个作用是_________________。
外,另一个作用是_________________。
(5)装置Ⅷ的烧杯中盛放的试剂是______![]() 填编号:
填编号:![]() 水
水 ![]() 热水
热水 ![]() 冰水
冰水![]()
【答案】![]() 稀硝酸 g c b e j h 除去
稀硝酸 g c b e j h 除去![]() 中的HCl
中的HCl ![]() 通过观察气泡调节气体流速
通过观察气泡调节气体流速 ![]()
【解析】
(1)根据反应原理,反应条件,反应物的状态确定装置;
(2)收集一瓶干燥纯净的氯气,选择装置是顺序是除杂、干燥、收集;
(3)为了使气体充分反应,依据氯气的密度大于空气的性质,为了使气体充分接触;
(4)装置Ⅲ、Ⅳ除可干燥NO、![]() 外,另一个作用是:通过观察气泡调节气体流速;
外,另一个作用是:通过观察气泡调节气体流速;
(5)烧杯中盛放的试剂是了降低温度使亚硝酰氯成为液体;
(1)若制备![]() 发生装置选A,则反应的离子方程式为:
发生装置选A,则反应的离子方程式为:![]() ;若制备NO发生装置选B,锥形瓶中放的是Cu片,依据NO的制备是用Cu和稀硝酸的反应,所以分液漏斗中的试剂为:稀硝酸;
;若制备NO发生装置选B,锥形瓶中放的是Cu片,依据NO的制备是用Cu和稀硝酸的反应,所以分液漏斗中的试剂为:稀硝酸;
(2)欲收集一瓶干燥纯净的氯气,选择装置是顺序是除杂、干燥、收集,所以其连接顺序为:![]() ;
;![]() 按气流方向,用小写字母表示
按气流方向,用小写字母表示![]() ,其中F装置的作用为:除去
,其中F装置的作用为:除去![]() 中的HCl;
中的HCl;
(3)为了使气体充分反应,依据氯气的密度大于空气的性质,为了使气体充分接触,所以从A处进入的气体是:![]() ;
;
(4)装置Ⅲ、Ⅳ除可干燥NO、![]() 外,另一个作用是:通过观察气泡调节气体流速;
外,另一个作用是:通过观察气泡调节气体流速;
(5)装置Ⅷ的作用收集亚硝酰氯![]() ,是红褐色液体或黄色气体,所以烧杯中盛放的试剂是了降低温度使亚硝酰氯成为液体,所以烧杯中盛放的试剂是:③。
,是红褐色液体或黄色气体,所以烧杯中盛放的试剂是了降低温度使亚硝酰氯成为液体,所以烧杯中盛放的试剂是:③。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下图所示为“双色双喷泉”实验装置,图中烧瓶内分别充满氨气和氯化氢,烧杯内盛装滴有石蕊试液的蒸馏水。下列说法错误的是
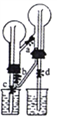
A. 在实验室中,可用浓氨水和生石灰制备氨气,用浓盐酸和浓硫酸制备氯化氢
B. 在实验室中制备干燥的氨气和氯化氢时,可选用相同的干燥剂
C. 实验中同时打开止水夹a、c、d,即可分别形成蓝色和红色喷泉
D. 喷泉结束后,将烧瓶内溶液混合后呈紫色,蒸干可得氯化铵固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某绿色溶液A含有H+、Na+、Mg2+、Fe2+、Cu2+、SO![]() 、Clˉ、CO
、Clˉ、CO![]() 和HCO
和HCO![]() 离子中的若干种。取该溶液进行如下实验(已知Ag2SO4微溶于水,可溶于硝酸):
离子中的若干种。取该溶液进行如下实验(已知Ag2SO4微溶于水,可溶于硝酸):
①向溶液中滴加少量![]() 溶液,过滤,得到不溶于酸的白色沉淀和绿色滤液B;
溶液,过滤,得到不溶于酸的白色沉淀和绿色滤液B;
②取滤液B,先用HNO3酸化,再滴加0.001 mol·Lˉ1 AgNO3溶液,有白色沉淀生成。
下列说法不正确的是
A.溶液A中一定存在H+、SO![]() 和Clˉ
和Clˉ
B.溶液A中不存在Mg2+、CO![]() 和HCO
和HCO![]() ,不能确定Na+的存在
,不能确定Na+的存在
C.第②步生成的白色沉淀中只有AgCl,没有Ag2CO3
D.溶液A中存在Fe2+与Cu2+中的一种或两种,且可用NaOH溶液判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮、磷、砷![]() 、锑
、锑![]() 、铋
、铋![]() 、镆
、镆![]() 为元素周期表中原子序数依次增大的同族元素。回答下列问题:
为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)砷在元素周期表中的位置______。![]() 的中子数为______。已知:
的中子数为______。已知:![]() (
(![]() ,白磷)=
,白磷)=![]() (
(![]() ,黑磷)
,黑磷) ![]() ;
;![]() (
(![]() ,白磷)=
,白磷)=![]() (
(![]() ,红磷)
,红磷) ![]() ; 由此推知,其中最稳定的磷单质是______。
; 由此推知,其中最稳定的磷单质是______。
(2)氮和磷氢化物性质的比较:热稳定性:![]() ______
______![]() (填“>”“<”)。 沸点:
(填“>”“<”)。 沸点:![]() ______
______![]() (填“>”“<”),判断依据是______。
(填“>”“<”),判断依据是______。
(3)![]() 和
和![]() 与卤化氢的反应相似,产物的结构和性质也相似。下列对
与卤化氢的反应相似,产物的结构和性质也相似。下列对![]() 与
与![]() 反应产物的推断正确的是______(填序号)。
反应产物的推断正确的是______(填序号)。
a.不能与![]() 反应 b.含离子键、共价键 c.能与水反应
反应 b.含离子键、共价键 c.能与水反应
(4)![]() 能发生较烈的水解,生成难溶的
能发生较烈的水解,生成难溶的![]() ,写出该反应的化学方程式 ______________,因此,配制
,写出该反应的化学方程式 ______________,因此,配制![]() 溶液应注意_____________。
溶液应注意_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题:
(1)Zn原子核外电子排布式为________________。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)_______Ⅰ1(Cu)(填“大于”或“小于”)。原因是________________。
(3)ZnF2具有较高的熔点(872 ℃),其化学键类型是_________;ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂,原因是________________。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为________________,C原子的杂化形式为________________。
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______________。六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为NA,Zn的密度为________________g·cm-3(列出计算式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有7瓶失去标签的试剂瓶,已知它们盛装的液体可能是乙醇、乙酸、苯、乙酸乙酯、油脂、葡萄糖溶液、蔗糖溶液。现通过如下实验来确定各试剂中所装液体的名称。
实验步骤和方法 | 实验现象 |
①把7瓶液体依次标号为A、B、C、D、E、F、G后闻气味 | 只有F、G两种液体没有气味 |
②各取少量于试管中加水稀释 | 只有C、D、E三种液体不溶解而浮在水上层 |
③分别取少量7种液体于试管中加新制的 | 只有B使沉淀溶解,F中产生砖红色沉淀 |
④各取C、D、E少量于试管中,加稀 | 只有C中仍有分层现象,且在D的试管中闻到特殊香味 |
试写出下列序号代表的液体名称:
A___________________,B___________________,C___________________,D___________________,E___________________,F___________________,G___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有资料显示过量的氨气和氯气在常温下可合成岩脑砂![]() 主要成分为
主要成分为 ![]() ,某实验小组对该反应进行探究,并对岩脑砂进行元素测定,回答下列问题:
,某实验小组对该反应进行探究,并对岩脑砂进行元素测定,回答下列问题:
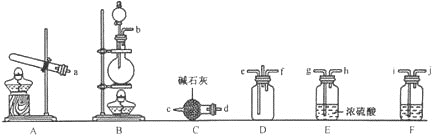
(1)岩脑砂的制备
![]() 利用装置A制取实验所需的氨气,写出反应的化学方程式:_____________。
利用装置A制取实验所需的氨气,写出反应的化学方程式:_____________。
![]() 该实验中用浓盐酸与
该实验中用浓盐酸与![]() 反应制取所需氯气,则装罝F中的试剂是
反应制取所需氯气,则装罝F中的试剂是![]() 填写试剂名称
填写试剂名称![]() ___________________。
___________________。
![]() 为了使氨气和氯气在D中充分混合,请确定上述装置的合理连接顺序:
为了使氨气和氯气在D中充分混合,请确定上述装置的合理连接顺序:![]() _____
_____![]() ________
________![]() 提示:氨气和氯气形成逆向流动,更有利于二者充分混合
提示:氨气和氯气形成逆向流动,更有利于二者充分混合![]()
![]() 证明氨气和氯气反应有岩脑砂生成,需要的检验试剂中,除了蒸馏水、稀
证明氨气和氯气反应有岩脑砂生成,需要的检验试剂中,除了蒸馏水、稀![]() 、NaOH溶液外,还需要____________________。
、NaOH溶液外,还需要____________________。
(2)岩脑砂中元素的测定
准确称取![]() 岩脑砂,与足量的氧化铜混合加热
岩脑砂,与足量的氧化铜混合加热![]() 发生的反应为
发生的反应为![]() ,利用下列装置测定岩脑砂中氮元素和氯元素的质量之比。
,利用下列装置测定岩脑砂中氮元素和氯元素的质量之比。
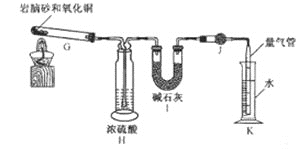
![]() 设置装置H的目的是____________________。
设置装置H的目的是____________________。
![]() 若装置Ⅰ增重
若装置Ⅰ增重 ![]() ,利用装置 K测得气体体积为
,利用装置 K测得气体体积为 ![]() 已知常温常压下气体摩尔体积为
已知常温常压下气体摩尔体积为 ![]() ,则岩脑砂中
,则岩脑砂中 ![]() _____________
_____________![]() 用含 b、V的代数式表示,不必化简
用含 b、V的代数式表示,不必化简![]() 。若测量体积时气体温度高于常温
。若测量体积时气体温度高于常温![]() 其他操作均正确
其他操作均正确![]() ,则
,则 ![]() 比正常值______________
比正常值______________![]() 填“偏高”“偏低”或“无影响”
填“偏高”“偏低”或“无影响”![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为某机物与对应试剂的反应现象或是否反应,则这种有机物可能是( )
试剂 | 钠 | 溴的四氯化碳溶液 | 新制 | 乙酸 |
现象或是否反应 | 放出气体 | 褪色 | 逐渐溶解 | 不反应 |
A.![]() B.
B.![]()
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫单质和化合物在工农业生产中有着重要的应用,而![]() 直接排放会对环境造成危害。
直接排放会对环境造成危害。
I.已知:重晶石![]() 高温缎烧可发生一系列反应,其中部分反应如下:
高温缎烧可发生一系列反应,其中部分反应如下:
![]()
![]()
![]()
![]()
已知:![]()
![]()
则:![]()
![]() _____________;
_____________;
![]() 的尾气处理通常有以下几种方法:
的尾气处理通常有以下几种方法:
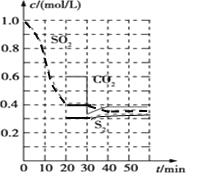
(1)活性炭还原法 反应原理:恒温恒容时![]() 反应进行到不同时间测得各物质的浓度如上图:
反应进行到不同时间测得各物质的浓度如上图:
![]() 反应速率表示为
反应速率表示为![]() _________________;
_________________;
![]() 时,改变某一条件平衡发生移动,则改变的条件最有可能是________________________;
时,改变某一条件平衡发生移动,则改变的条件最有可能是________________________;
![]() 时,平衡常数
时,平衡常数![]() _____________。
_____________。
(2)亚硫酸钠吸收法
![]() 溶液吸收
溶液吸收![]() 的离子方程式为____________
的离子方程式为____________
![]() 常温下,当吸收至
常温下,当吸收至![]() 时,吸收液中相关离子浓度关系一定正确的是_______
时,吸收液中相关离子浓度关系一定正确的是_______![]() 填序号
填序号![]()
![]()
![]()
![]()
![]() 水电离出
水电离出![]()
(3)电化学处理法
![]() 如下图所示,
如下图所示,![]() Ⅰ
Ⅰ![]() 电极的反应式为___________________;
电极的反应式为___________________;
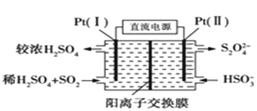
![]() 当电路中转移
当电路中转移![]() 时
时![]() 较浓
较浓![]() 尚未排出
尚未排出![]() ,交换膜左侧溶液中增加_______mol离子.
,交换膜左侧溶液中增加_______mol离子.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com