
 白磷(P4)是磷的单质之一,易氧化,与卤素单质反应生成卤化磷.卤化磷通常有三卤化磷或五卤化磷,五卤化磷分子结构(以PCl5为例)如右图所示.该结构中氯原子有两种不同位置.
白磷(P4)是磷的单质之一,易氧化,与卤素单质反应生成卤化磷.卤化磷通常有三卤化磷或五卤化磷,五卤化磷分子结构(以PCl5为例)如右图所示.该结构中氯原子有两种不同位置.| 6 |
| 128g/mol |
| ||
| 1 |
| 0.05 |
| 5 |
| x |
| 0.20mol |
| 0.05L |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
1 1 |
2 1 |
 与
与
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量.量筒的规格为1000mL,供选择的电极材料有纯镁片和纯铝片.请回答下列问题:
现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量.量筒的规格为1000mL,供选择的电极材料有纯镁片和纯铝片.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
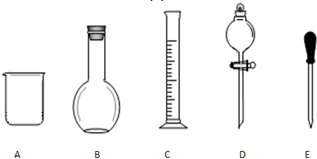 实验室需要0.1mol/L NaOH溶液480mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/L NaOH溶液480mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、m=3 n=6 |
| B、m=3 n=4 |
| C、m=4 n=1 |
| D、m=4 n=5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸发时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C、分液时,分液漏斗中下层液体从下口放出,上层液体也从下口放出 |
| D、过滤时,要用玻璃棒引流,并不断用玻璃棒搅拌,加快过滤速度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com