
| 1000�Ѧ� |
| M |
| n |
| V |
| 1000��1.84g/ml��98% |
| 98g/mol |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��2CH4��g��+
| ||
B��2CH4��g��+
| ||
| C��3CH4��g��+5O2��g��=CO2��g��+2CO��g��+6H2O��g������H=-1840kJ?mol-1 | ||
| D��3CH4��g��+5O2��g��=CO2��g��+2CO��g��+6H2O��1������H=-1538kJ?mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
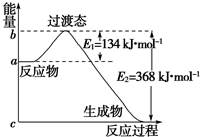 �ο�����ͼ�����й�Ҫ��ش����⣺
�ο�����ͼ�����й�Ҫ��ش����⣺| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
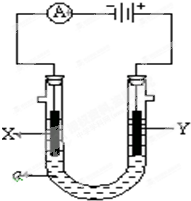 ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������FeCl3��Һʱ��Ӧ��FeCl3�ܽ��������������� |
| B��������ɫ��Ӧʱ�����ò�˿����NaOH��Һϴ�Ӳ�������� |
| C����CCl4��ȡ��ˮ�е�I2ʱ���л���ӷ�Һ©�����¶˷ų� |
| D������к͵ζ�ʱ����ƿ���ô���Һ��ϴ2�飬�ټ������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ȥFe2��SO4��3��Һ�л��е�Fe SO4����������������ˮ |
| B����ȥFeCl2��Һ�л��е�FeCl3�������������ۣ����� |
| C�������е�þ�ۣ�������������������Һ������ |
| D����ȥCu���л��е�CuO��������ϡ������ˡ�ϴ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��
| ||
B��
| ||
| C��5��10-10 | ||
| D��5��10-12 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com