
【题目】设NA为阿伏加德罗常数的值.下列说法正确的是( )
A.常温常压下,7.8 gNa2S和Na2O2的混合物中,阴离子所含电子数为1.8NA
B.标准状况下,11.2 L 二氯甲烷中含有的分子数目为0.5NA
C.常温常压下,28 g乙烯与丙烯的混合气体含有的碳原子数目无法计算
D.0.1 molL﹣1MgCl2溶液中含有的Mg2+数目小于0.1NA
 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:
【题目】常温下,下列有关叙述正确的是( )
A.水的离子积KW只与温度有关,但水的电离程度一定会受外加酸、碱、盐的影响
B.若HA的Ka=1.7×10﹣5 , BOH的Kb=1.7×10﹣5 , 则HA溶液中的c(H+)与BOH中的c(OH﹣)相等
C.将0.2mol/L HA溶液和0.1mol/L NaOH溶液等体积混合,则反应后的混合液中:c(OH﹣)+c(A﹣)=c(H+)+c(HA)
D.Mg(OH)2能溶于NH4Cl浓溶液的主要原因是NH4+结合OH﹣使沉淀溶解平衡发生正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在工农业生产及日常生活中应用非常广泛.
(1)由辉铜矿制取铜的反应过程为:
2Cu2S(s)+3O2 (g)=2Cu2O(s)+2SO2(g)△H=﹣768.2kJmol﹣1 ,
2Cu2O(s)+Cu2S(s)=6Cu(s)+SO2(g)△H=+116.0kJmol﹣1 ,
请写出Cu2S与O2反应生成Cu与SO2的热反应方程式: .
(2)氯化铜溶液中铜各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与c(Cl﹣) 的关系如图1.①当c(Cl﹣)=9molL﹣1时,溶液中主要的3种含铜物种浓度大小关系为 . 
②在c(Cl﹣)=1molL﹣1的氯化铜溶液中,滴入AgNO3溶液,含铜物种间转化的离子方程式为(任写一个).
(3)电解Na2HPO3溶液可得到亚磷酸,装置如图2
(说明:阳膜只允许阳离子通过,阴膜只允许阴离子通过)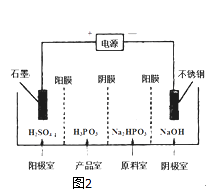
①阳极的电极反应式为: .
②产品室中反应的离子方程式为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】单质钛(Ti)的机械强度高,抗腐蚀能力强,有“未来金属”之称。以TiO2制金属钛,主要反应有:
①TiO2+2C+2Cl2 ![]() TiCl4+2CO; ②TiCl4+2Mg
TiCl4+2CO; ②TiCl4+2Mg![]() 2MgCl2+Ti
2MgCl2+Ti
下列叙述不正确的是
A. 反应①中TiO2是氧化剂 B. 反应②表现了金属镁还原性比金属钛强
C. 反应①中碳是还原剂 D. 反应①中氧化剂与还原剂物质的量之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘具有多种放射性同位素. ![]() I俗称“碘131”,广泛地用于医学诊断作为追踪剂和甲状腺内分泌失调症的治疗.下列有关
I俗称“碘131”,广泛地用于医学诊断作为追踪剂和甲状腺内分泌失调症的治疗.下列有关 ![]() I叙述正确的是( )
I叙述正确的是( )
A.碘元素的相对原子质量为131
B.![]() I是一种新发现的碘的核素
I是一种新发现的碘的核素
C.![]() I位于元素周期表中第4周期ⅦA族
I位于元素周期表中第4周期ⅦA族
D.![]() I核内的中子数与核外电子数之差为29
I核内的中子数与核外电子数之差为29
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式不正确的是
A. 向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO![]() ===3Fe3++NO↑+2H2O
===3Fe3++NO↑+2H2O
B. 铜片与浓HNO3:Cu+2NO![]() +4H+===Cu2++NO2↑+2H2O
+4H+===Cu2++NO2↑+2H2O
C. 氯化铵浓溶液跟浓NaOH溶液混合后加热:NH![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
D. 碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)下列实验操作或对实验事实的描述中,正确的是(填序号)
①为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
②化学药品着火,都要立即用水或泡沫灭火器灭火
③配制一定物质的量浓度的稀硫酸溶液时,量取浓硫酸后的量筒要用蒸馏水洗涤,并把洗涤液转入容量瓶中
④配制一定物质的量浓度的溶液在定容时,俯视容量瓶的刻线,会使配制的浓度偏高
⑤检验红砖中的红色物质是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液
(2)将下列物质进行分类:
①11H 与13H ②O2与O3 ③乙醇与甲醚(CH3﹣O﹣CH3)④ 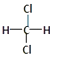 与
与 
⑤CH3CH2CH2CH3与CH3﹣CH(CH3)﹣CH3⑥C60与金刚石 ⑦乙醇与甘油
互为同位素的是(填编号,下同);互为同素异形体的是互为同分异构体的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,称量一个充满氯气的容器质量为74.6g,若改充氮气,其质量为66g,则容器的容积为
A.11.2LB.5.6LC.4.48LD.2.24L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各表述与示意图一致的是( )
A.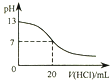 图表示25℃时,用0.1 molL﹣1盐酸滴定20 mL 0.1 molL﹣1 NaOH溶液,溶液的pH随加入酸体积的变化
图表示25℃时,用0.1 molL﹣1盐酸滴定20 mL 0.1 molL﹣1 NaOH溶液,溶液的pH随加入酸体积的变化
B.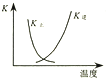 图中曲线表示反应2SO2(g)+O2(g)═2SO3(g);△H<0 正、逆反应的平衡常数K随温度的变化
图中曲线表示反应2SO2(g)+O2(g)═2SO3(g);△H<0 正、逆反应的平衡常数K随温度的变化
C. 图③表示10 mL 0.01 molL﹣1 KMnO4 酸性溶液与过量的0.1 molL﹣1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化
图③表示10 mL 0.01 molL﹣1 KMnO4 酸性溶液与过量的0.1 molL﹣1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化
D.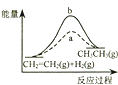 图中a、b曲线分别表示反应CH2=CH2 (g)+H2(g)→CH3CH3(g);△H<0使用和未使用催化剂时,反应过程中的能量变化
图中a、b曲线分别表示反应CH2=CH2 (g)+H2(g)→CH3CH3(g);△H<0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com