
【题目】某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100 mL,已知溶液中阳离子的浓度相同,且SO42-物质的量浓度为6 mol/L,则此溶液最多溶解铁粉的质量为( )
A.11.2 gB.16.8 gC.19.6 gD.22.4 g
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
【题目】如图所示是![]() 的两个性质实验,下列有关说法中正确的是
的两个性质实验,下列有关说法中正确的是![]()

A. 两个实验均表现了![]() 易溶于水
易溶于水
B. 两个实验均表现了![]() 易挥发
易挥发
C. 两个实验均表现了![]() 是碱性气体
是碱性气体
D. 两个实验均表现了![]() 是还原性气体
是还原性气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】贝诺酯是由阿司匹林、扑热息痛经化学法拼合制备的解热镇痛抗炎药,其合成反应式(反应条件略去)如下:
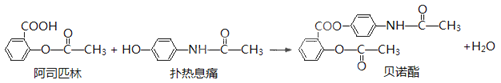
下列叙述错误的是
A. FeCl3溶液可区别阿司匹林和扑热息痛
B. 1mol阿司匹林最多可消耗2mol NaOH
C. 常温下贝诺酯在水中的溶解度小于扑热息痛
D. C6H7NO是扑热息痛发生类似酯水解反应的产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。
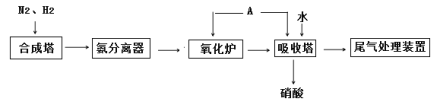
(1)写出合成塔中发生反应的化学方程式____________________,
(2)写出氧化炉中发生反应的化学方程式____________________
(3)A物质为______,向吸收塔中通入A的作用__________
(4)工业生产中为了盛装大量浓硝酸,可选择___作为罐体材料
A. 铜 B.铂 C.铝 D.镁
(5)为避免尾气氮氧化物污染环境,人们开发了溶液吸收、催化还原等尾气处理方法。前者使用具有碱性的Na2CO3溶液等吸收尾气,后者在催化下使用NH3或其他物质将氮氧化物还原为N2。请以尾气中的NO2处理为例,写出相关反应的化学方程式____________、_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体的结构如图所示,下列说法中不正确的是 ( )


A. 在NaCl晶体中,距Na+最近的Cl-形成正八面体
B. 在CaF2晶体中,每个晶胞平均占有4个Ca2+
C. 在金刚石晶体中,碳原子与碳碳键个数的比为1∶2
D. 该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种化合物的结构如图所示,其中X、Y、Z、Q、W为原子序数依次增大的五种短周期主族元素,Q核外最外层电子数与Y核外电子总数相同,X的原子半径是元素周期表中最小的。下列叙述正确的是( )

A.WX的水溶液呈碱性
B.元素非金属性的顺序为:Y>Z>Q
C.由X、Y、Q、W四种元素形成的化合物的水溶液一定呈碱性
D.该化合物中与Y单键相连的Q满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种优良的水处理剂。25℃,其水溶液中加酸或碱改变溶液的pH时,含铁粒子的物质的量分数δ(X)随pH的变化如图所示[已知![]() ]。下列说法正确的是( )
]。下列说法正确的是( )
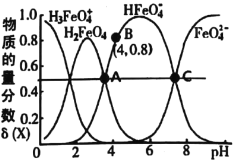
A.K2FeO4、H2FeO4都属于强电解质
B.由B点数据可知,H2FeO4的第一步电离常数Ka1=4.0×10-4
C.25℃,H2FeO4(aq)+H+![]() H3FeO4+(aq)的平衡常数K>100
H3FeO4+(aq)的平衡常数K>100
D.A、C两点对应溶液中水的电离程度不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用有机物X在一定条件下可合成植物生长所需的“平衡因子”Y(部分产物未写出)。已知含有“手性碳原子”的分子可形成对映异构体。下列有关说法中正确的是( )
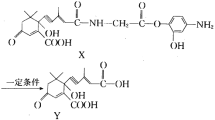
A.X,Y分子都不存在对映异构体
B.X分子中所有碳原子可能都在同一平面
C.Y分子可以发生取代、酯化、消去、加成、氧化等反应
D.未写出的产物可能有2种,且都具有两性化合物的特性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com