
科目: 来源: 题型:选择题
| A. | CH2=CH-CH=CH2 | B. | HOCH2-CH2OH | C. | 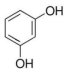 | D. | HCOOH |
查看答案和解析>>
科目: 来源: 题型:实验题
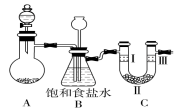 某学习小组围绕氯气设计了一系列实验.
某学习小组围绕氯气设计了一系列实验.| A | B | C | D | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
科目: 来源: 题型:实验题
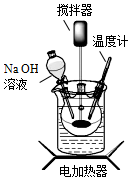 超细Fe3O4粉体可制成磁流体,一种制备超细Fe3O4粉体的实验步骤如下:
超细Fe3O4粉体可制成磁流体,一种制备超细Fe3O4粉体的实验步骤如下:查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氢氧两种元素只能组成H2O | |
| B. | 导热性等属于水的化学性质 | |
| C. | 0℃时冰的密度比液态水的密度小 | |
| D. | 液态水两种形态间转化需断裂O-H键 |
查看答案和解析>>
科目: 来源: 题型:填空题
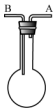 利用如图装置收集以下气体:①H2、②Cl2、③CH4、④HCl、⑤HBr
利用如图装置收集以下气体:①H2、②Cl2、③CH4、④HCl、⑤HBr查看答案和解析>>
科目: 来源: 题型:选择题
| A. | BOH 溶于水,其电离方程式是 BOH═B++OH- | |
| B. | 在 0.1 mol•L-1 BA 溶液中,c(B+)>c(A-)>c(OH-)>c(H+) | |
| C. | 若一定量的上述两溶液混合后 pH=7,则 c(A- )=c(B+ ) | |
| D. | 若将 0.1 mol•L-1 BOH 溶液稀释至 0.001 mol•L-1,则溶液的 pH=9 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1.2×10-3mol•L-1 | B. | 1.2×10-9mol•L-1 | C. | 2.4×10-5mol•L-1 | D. | 3.2×10-6mol•L-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| 阳极 | 阴极 | 溶液甲 | 物质乙 | |
| A | Pt | Pt | NaOH | NaOH固体 |
| B | Pt | Pt | H2SO4 | H2O |
| C | Pt | Pt | NaCl | NaOH |
| D | 粗铜 | 精铜 | CuSO4 | Cu(OH)2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com