
科目: 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是
A.124 g P4含有P—P键的个数为4NA
B.12 g石墨烯(单层石墨)中含有C-C键的数目为3NA
C.60gSiO2中含Si—O键的个数为2NA
D. 六方最密堆积的配位数是12,空间利用率是74%
查看答案和解析>>
科目: 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:选择题
下列关于晶体的叙述中,不正确的是
A、金刚石网状结构中,由共价键形成的碳原子环其中最小环有6个碳原子
B、在氯化钠的晶体中,每个Na+或Cl-的周围都紧邻6个Cl-或Na+
C、在氯化铯晶体中,每个Cs+周围都紧邻8个Cl—,每个Cl—周围也紧邻8个Cs+
D、在干冰的晶体中,每个CO2分子周围都紧邻4个CO2分子
查看答案和解析>>
科目: 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:选择题
下列FeCl3的性质中,能够证明FeCl3是共价化合物的是( )
A.FeCl3易溶于水
B.液态的FeCl3不导电
C.FeCl3常温下不易分解
D.FeCl3溶于水能电离,呈酸性
查看答案和解析>>
科目: 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:选择题
磷化硼是一种超硬耐磨涂层材料。下图为其晶体结构中最小的重复结构单元,其中的每个原子均满足8电子稳定结构。下列有关说法正确的是( )
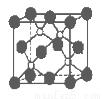
A.磷化硼晶体的化学式为BP,属于离子晶体
B.磷化硼晶体的熔点高,且熔融状态下能导电
C.磷化硼晶体中每个原子均形成4条共价键
D.磷化硼晶体结构微粒的空间堆积方式与氯化钠相同
查看答案和解析>>
科目: 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:选择题
下列对分子及其性质的解释中,不正确的是
A. 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释
B. 乳酸[CH3CH(OH)COOH]中存在一个手性碳原子
C. 水加热到很高的温度都难以分解是因为水分子间有氢键。
D. 已知酸性:H3PO4>HClO,是因为H3PO4分子中有1个非羟基氧原子,而 HClO分子中非羟基氧原子数目为0
查看答案和解析>>
科目: 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:选择题
下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热为2×(-57.3)kJ/mol
B.已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g) △H = +285.5kJ/mol
C.CO(g)的燃烧热是283.0 kJ/mol,则表示CO燃烧热的热化学方程式为CO(g) +1/2O2(g)=CO2 (g);△H=-283.0 kJ/mol
D.需要加热才能发生的反应一定是吸热反应
查看答案和解析>>
科目: 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:选择题
下列关于晶体的说法正确的组合是 ( )
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤CaTiO3晶体中(晶胞结构如图所示),已知Ca2+、O2—、Ti4+分别位于立方体的体心、面心和顶点,则每个Ti4+和12个O2—相紧邻
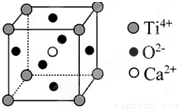
⑥SiO2晶体中每个硅原子与两个氧原子以共价键相结合
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
A.①②③⑥ B.①②④ C.③⑤⑦ D.③⑤⑧
查看答案和解析>>
科目: 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:填空题
下图表示一些晶体中的某些结构,他们分别是氯化钠、氯化铯、干冰、金刚石、石墨结构中的某一种的某一部分(黑点可表示不同或相同的粒子)。
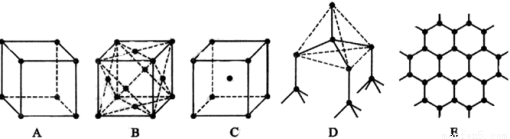
(1)其中代表金刚石的是 (填编号字母,下同),金刚石 中每个碳原子与 个碳原子最接近且距离相等。
中每个碳原子与 个碳原子最接近且距离相等。
(2)其中代表石墨的是 ,其中每个正六边形占有的碳原子数平均为____ 个;
(3)其中表示氯化钠的是 ,每个钠离子周围与它最接近且距离相等的钠离子有 个;
(4)代表氯化铯的是 ,每个铯离子与 个氯 离子紧邻;
离子紧邻;
(5)代表干冰的是 ,每个二氧化碳分子与 个二氧化碳分子紧邻;
(6)由Mg、C、Ni三种元素形成的一种具有超导性的晶体,晶胞如图2所示。Mg位于C 和Ni原子紧密堆积所形成的空隙当中。与一个Ni原子距离最近的Ni原子的数目为 ,该晶体的化学式为 。


(图2) (图3)
查看答案和解析>>
科目: 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:实验题
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的(图3)装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是 。
(2)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(3)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶 液进行反应,与上述实验相比,所放出
液进行反应,与上述实验相比,所放出 的热量 (填“相等、不相等”),所求中和热△H_____ (填“相等、不相等”)
的热量 (填“相等、不相等”),所求中和热△H_____ (填“相等、不相等”)
(4)如果用相同浓度和体积的氨水代替NaOH溶液进行上述实验,所求的中和热△H会 (填“偏大”、“偏小”、“无影响”) 若用KOH代替NaOH,实验所测的热量会_________________(填“偏大”、“偏小”、“无影响”)。
(5)他们记录的实验数据如下:
实验用品[ | 溶液温度 | 中和热 △H | |||
起始平 均温度 | 反应最高温度 | ||||
① | 50mL,0.55mol.L-1NaOH | 50mL,0.5mol.L-1HCl | 20℃ | 23.3℃ | |
② | 50mL,0.55mol.L-1N | 50mL,0.5mol.L-1HCl | 20℃ | 23.5℃ | |
已知反应后溶液的比热容C为4.18KJ·℃-1· Kg-1,各物质的密度均视为1g·cm-3。
①根 据上表数据计算中和
据上表数据计算中和 热△H=__________(保留至小数点后一位)
热△H=__________(保留至小数点后一位)
②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式: 。
(6)上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)_______________。
A.实验装置保温、隔热效果差
B.量取稀盐酸溶液的体积时仰视读数
C.一次性把NaOH溶液倒入盛有盐酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后直接测定HCl溶液的温度
查看答案和解析>>
科目: 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:填空题
原子序数依次递增 且都小于36的X、Y、Z、Q、W五种元素,其中X是原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Q原子基态时2p原子轨道上有2个未成对的电子,W元素的原子结构中3d能级有4个未成对电子。回答下列问题:
且都小于36的X、Y、Z、Q、W五种元素,其中X是原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Q原子基态时2p原子轨道上有2个未成对的电子,W元素的原子结构中3d能级有4个未成对电子。回答下列问题:
(1)Y2X2分子中Y原子轨道的杂化类型为 ,Y2X2分子中σ键和π键个数比为 。
(2)化合物ZX3的沸点比化合物YX4的高,其主要原因是 。
(3)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是 。
(4)元素W能形成多种配合物,如:W(CO)5等。
①基态W3+的M层电子排布式为 。
② W(CO)5常温下呈液态,熔点为—20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断W(CO)5晶体属于 晶体(填晶体类型),该晶体中W的化合价为 。
W(CO)5常温下呈液态,熔点为—20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断W(CO)5晶体属于 晶体(填晶体类型),该晶体中W的化合价为 。
(5)下列有关的说法正确的是 。
A.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
B.电负性顺序:X<Y<Z<Q
C.因为晶格能CaO比KCl高,所以KC l比CaO熔点低
l比CaO熔点低
D.H2 YO3的分子结构中含有一个非羟基氧,故其为中强酸
(6)Q和Na形成的一种只含有离子键的离子化合物的晶胞结构如图4,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为 。已知该晶胞密度为ρ g/cm3,阿伏加德罗常数为NA,求晶胞边长a= pm。(用含ρ、NA的计算式表示)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com