
科目: 来源: 题型:
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间的变化曲线如图,下列表述中正确的是( )
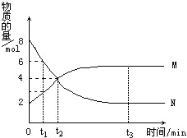
A、反应的化学方程式为:2M![]() N
N
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目: 来源: 题型:
【题目】印尼火山喷发不仅带来壮观的美景,还给附近的居民带来物质财富,有许多居民冒着生命危险在底部的火山口收集纯硫磺块来赚取丰厚收入。硫磺可用于生产化工原料硫酸。某工厂用下图所示的工艺流程生产硫酸:
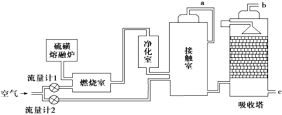
请回答下列问题:
(1)为充分利用反应放出的热量,接触室中应安装______________(填设备名称)。吸收塔中填充有许多瓷管,其作用是_____________________________________________。
(2)为使硫磺充分燃烧,经流量计1通入燃烧室的氧气过量50%,为提高SO2转化率,经流量计2的氧气量为接触室中二氧化硫完全氧化时理论需氧量的2.5倍,则生产过程中流经流量计1和流量计2的空气体积比应为________。假设接触室中SO2的转化率为95%,b管排出的尾气中二氧化硫的体积分数为__________(空气中氧气的体积分数按0.2计),该尾气的处理方法是________。
(3)与以硫铁矿为原料的生产工艺相比,该工艺的特点是________(可多选)。
A.耗氧量减少 B.二氧化硫的转化率提高
C.产生的废渣减少 D.不需要使用催化剂
(4)硫酸的用途非常广,可应用于下列哪些方面__________________________。
A.橡胶的硫化 B.表面活性剂“烷基苯磺酸钠”的合成
C.铅蓄电池的生产 D.过磷酸钙的制备
(5)矿物燃料的燃烧是产生大气中SO2的主要原因之一。在燃煤中加入适量的石灰石,可有效减少煤燃烧时SO2的排放,请写出此脱硫过程中反应的化学方程式_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上曾经通过反应“3Fe+4NaOH![]() Fe3O4+2H2↑+4Na↑”生产金属钠。下列有关说法正确的是( )
Fe3O4+2H2↑+4Na↑”生产金属钠。下列有关说法正确的是( )
A.用磁铁可以将Fe与Fe3O4分离
B.将生成的气体在空气中冷却可获得钠
C.该反应条件下铁的氧化性比钠强
D.每生成1molH2,转移的电子数约为4×6.02×1023
查看答案和解析>>
科目: 来源: 题型:
【题目】现有反应:mA(g)+nB(g) ![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
(1)该反应的逆反应为________热反应,且m+n______p (填“>”、“=”或“<”) 。
(2)减压时,A的质量分数__________。(填“增大”、“减小”或“不变”,下同)
(3)若容积不变加入B,则B的转化率__________。
(4)若升高温度,则平衡时B、C的浓度之比将__________。
(5)若加入催化剂,平衡时气体混合物的总物质的量__________。
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色__________;而维持容器内压强不变,充入氖气时,混合物颜色 。(填“变深”、“变浅”或“不变”)
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+。取该溶液100 mL,加入过量NaOH溶液,加热,得到0.02 mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6 g固体;向上述滤液中加足量BaCl2溶液,得到4.66 g不溶于盐酸的沉淀。由此可知原溶液中( )
A.至少存在5种离子 B.SO42-、NH4+一定存在,Cl-可能不存在
C.Cl-一定存在,且c(Cl-)≥0.4 mol/L D.CO32-、Al3+一定不存在,K+可能存在
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列反应合成甲醇CO(g)+2H2 (g)![]() CH3OH(g) ΔH
CH3OH(g) ΔH
(1)下表所列数据是反应在不同温度下的化学平衡常数(K)。
![]()
由表中数据判断ΔH________0 (填“>”、“=”或“<”),化学平衡常数表达式K=________;
(2)300℃时,在体积为2.0 L的密闭容器中通入2 mol CO和4 mol H2,经过20 s达到平衡状态,
①计算20 s内CO的反应速率为________,此时容器中甲醇的体积分数为_________;
②若向上述平衡体系中同时加入1mol CO,2mol H2和1mol CH3OH气体,平衡移动情况是__________(填“向右”、“向左”或“不移动”),原因是________________________
(3)已知在常温常压下:
①2CH3OH(l)+3O2 (g) = 2CO2 (g)+4H2O(g) ΔH=-1277.0kJ/mol
②2CO(g)+O2 (g) = 2CO2(g) ΔH=-566.0kJ/mol
③H2O(g) =H2O(l) ΔH=-44kJ/mol写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
__________________;
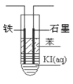
(4)甲醇、氧气可制作燃料电池,写出以氢氧化钾为电解质甲醇燃料电池负极反应式_______________;如图,电解KI溶液制碘,在粗试管中加入饱和的KI溶液,然后再加入苯,插入一根石墨电极和一根铁电极,使用该燃料电池做电源,铁电极与极___________(填正或负)相连接,通电一段时间后,断开电源,振荡试管,上层溶液为_______色,当有 1.27g碘单质生成时,需要_______g CH3OH。
查看答案和解析>>
科目: 来源: 题型:
【题目】最近我们复习了常见的几种金属:Na、Mg、Al、Fe、Cu。请结合我们所学知识回答下列问题:
(1)钠原子核外电子有________运动状态,其化合物Na2O2可用作________________。
(2)镁在二氧化碳中点燃的化学方程式为______________________________。
(3)铝在元素周期表中位于______________________________。
(4)除去Fe中的杂质Al所发生反应的离子方程式为_____________________________。
(5)上面几种金属中可用热还原法冶炼的是______________________________。
(6)铜的价电子排布式为3d104s1而不是3d94s2是依据_________________。
查看答案和解析>>
科目: 来源: 题型:
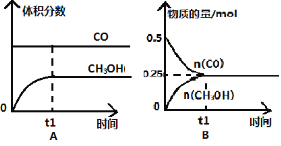
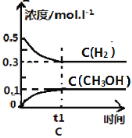
【题目】工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g) ![]() CH3OH(g)。一定条件下,将0.5molCO和0.5molH2在体积为2L的密闭容器中发生上述反应,则下列示意图合理的是 ( )
CH3OH(g)。一定条件下,将0.5molCO和0.5molH2在体积为2L的密闭容器中发生上述反应,则下列示意图合理的是 ( )

查看答案和解析>>
科目: 来源: 题型:
【题目】某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)NaN3是气体发生剂,受热分解产生N2和Na,N2的电子式为________。
(2)Fe2O3是主氧化剂,与Na发生置换反应生成的还原产物为________。
(3)KClO4是助氧化剂,反应过程中与Na作用生成KCl和Na2O。KClO4含有化学键的类型为________,金属晶体K的堆积方式为________。
(4)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为______
__________________________________。
(5)100 g上述产气药剂产生的气体通过碱石灰后得到N2 33.6 L(标准状况)。
①用碱石灰除去的物质为________________;
②该产气药剂中NaN3的质量分数为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在体积不变的绝热密闭容器中,2molSO2与1molO2在催化剂作用下发生反应:2SO2(g)+O2(g)![]() 2SO3(g)△H=﹣QkJ/mol(Q>0)。当气体的物质的量减少0.5mol时反应达到平衡。下列叙述错误的是( )
2SO3(g)△H=﹣QkJ/mol(Q>0)。当气体的物质的量减少0.5mol时反应达到平衡。下列叙述错误的是( )
A.增大氧气浓度,平衡正向移动,平衡常数不变
B.降低温度,正反应速率比逆反应速率减小的程度小
C.平衡时SO2气体的转化率为50%
D.该条件下反应放出0.5QkJ的热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com