
科目: 来源: 题型:
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题。

(1)B物质的化学式为。
(2)在蒸发操作中必须用到蒸发皿,下面对蒸发皿的操作中正确的是
A.将蒸发皿放置在铁架台的铁圈上直接用酒精灯火焰加热
B.将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热
C.将蒸发皿放置在三脚架上直接用酒精灯火焰加热
D.在三脚架上放置泥三角,将蒸发皿放置在泥三角上加热
(3)该方案的明显失误是因为某一步设计不当而使分离产物不纯,该步正确的方案可以设计为。
(4)若要测定原混合物中KCl和BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是的质量。
(5)请按要求写出下列离子方程式:
生成沉淀A:_____________________________________________________
沉淀A与盐酸反应:______________________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关组成生物体的化学元素的叙述,正确的是( )
A. 微量元素在生物体内含量很少,所以人体不存在微量元素缺乏症
B. 每种大量元素在不同的生物体内的含量都是相同的
C. 组成生物体的化学元素根据其含量不同分为大量元素和微量元素两大类
D. 组成生物体的大量元素中,C是最基本的元素,在细胞鲜重中含量总是最多的
查看答案和解析>>
科目: 来源: 题型:
【题目】某气态烃A,标准状况下的密度为1.25g/L。B和D都是生活中常见的有机物,D能跟碳酸氢钠反应,E有香味。它们之间的转化关系如下图所示:


(1)A的电子式为 ,D中官能团的名称为 。
(2)以A为原料自身合成高分子化合物的化学方程式为 ,反应类型是 。
(3)反应②在Cu做催化剂的条件下进行,该实验的步骤是将红亮的铜丝置于酒精灯上加热,待铜丝变为黑色时,迅速将其插入到装有B的试管中(如右图所示)。观察到的现象是 ,重复操作2-3次。写出过程②反应方程式 。
(4)B、D在浓硫酸的作用下实现反应③,实验装置如下图所示:

①试管1中实现反应③的化学方程式为 ,
②反应开始时用酒精灯对试管小火加热的原因是: 。(已知乙酸乙酯的沸点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)
查看答案和解析>>
科目: 来源: 题型:
【题目】I、现有含CaO杂质的CaC2试样。设计以下实验,测定CaC2试样的纯度。(反应方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑),请从下图中选用适当的装置,完成该实验。
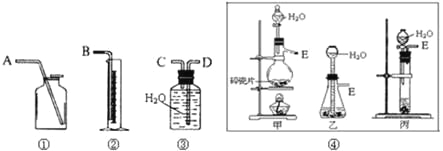
(1)制取C2H2最好选④中的 装置(填“甲”“乙”或“丙”),所选用装置的连接顺序是 (填各接口A~E的顺序)。
(2)若实验时称取的试样为1.4g,产生的乙炔在标准状况下的体积为448mL,此试样中CaC2的质量分数为 。(保留3为有效数字)

II、某同学在实验室从如图标签的试剂瓶中取少许钠进行燃烧实验,实验后 发现还有少许黑色固体生成。从反应物及实验操作猜测:
该黑色物质可能为碳与另一种氧化物组成的混合物。
根据题意和图示回答下面问题:
(1)装置图⑤中A的名称 。
(2)此氧化物可能是 或 (写化学式)。
(3)对黑色固体物质的组成作如图⑥所示研究
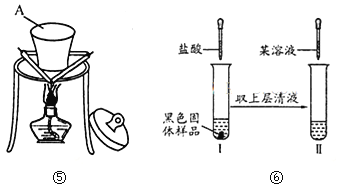
①实验I中加入盐酸溶液的目的是 。
②仅通过实验II,用最简步骤能快速确定黑色氧化物的组成,请完善该设计。(限选试剂:稀盐酸、KSCN溶液、10%H2O2溶液)
实验操作 | 预期现象与结论 | 相关离子方程式 |
取少量实验I中的澄清溶液,加入试剂 |
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是a、b两种固体物质的溶解度曲线,下列说法中,正确的是( )

A.a的溶解度大于b的溶解度
B.在t℃时,a、b的饱和溶液中溶质的物质的量浓度相同
C.当a中含有少量b时,可以用冷却结晶法提纯a
D.在t℃时,将a、b的饱和溶液升温后,溶质的质量分数:a﹥b
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊进入患者腹中。明胶是水溶性蛋白质混合物,溶于水形成胶体。由工业明胶制成的胶囊往往含有超标的重金属Cr,从而对人体造成伤害。
①已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是 价。
②CrO2-是一种酸根离子,则Fe(CrO2)2属于__ _(填“酸”、“碱”、“盐”或“氧化物”)。
③明胶的水溶液和K2SO4溶液共同具备的性质是 。
A.都不稳定,密封放置会产生沉淀
B.两者均有丁达尔现象
C.分散质粒子都可通过滤纸
Ⅱ.Cr是一种银白色金属,化学性质稳定,以+3和+6价为常见价态。工业上以铬铁矿(主要成分为FeO·Cr2O3 ,含有Al2O3、SiO2等杂质)为主要原料生产金属铬和重铬酸钠Na2Cr2O7·2H2O(已知Na2Cr2O7是一种强氧化剂),其主要工艺流程如下:
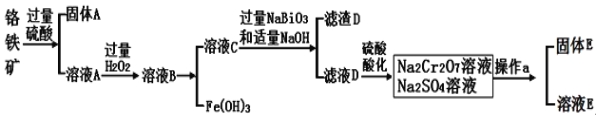
查阅资料:
常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO42-
(1)工业上常采用热还原法制备金属铬,写出以Cr2O3为原料,利用铝热反应制取金属铬的化学方程式 。
(2)酸化滤液D时,用硫酸而不选用盐酸,可能的原因是 。
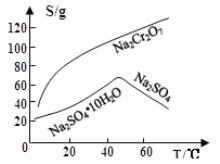
(3)固体E的主要成分是Na2SO4,根据下图分析操作a为 、 。
(4)已知含+6价铬的污水会污染环境。电镀厂产生的镀铜废水中往往含有一定量的Cr2O72-,处理该废水常用还原沉淀法,具体流程如下:

①Cr(OH)3的化学性质与Al(OH)3相似。在上述生产过程中加入NaOH溶液时要控制溶液的pH不能过高,是因为 ;(用离子方程式表示)
②下列溶液中可以代替上述流程中Na2S2O3溶液的是 (填选项序号);
A.FeSO4溶液 B.浓H2SO4 C.酸性KMnO4溶液 D.Na2SO3溶液
③上述流程中,每消耗0.1molNa2S2O3转移0.8mole-,则加入Na2S2O3溶液时发生反应的离子方程式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】金银花有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法正确的是

A.绿原酸的分子式为C16H8O9
B.1mol绿原酸最多与7mol NaOH反应
C.绿原酸是芳香族化合物
D.绿原酸分子中有4种化学环境不同的氢原子
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述不正确的是
A.常温常压下,NA个CO2分子的质量总和为44 g
B.常温常压下,1mol氦气含有的核外电子数为4 NA
C.12.4 g 白磷(P4)中含有的磷原子数为0.4 NA
D.0.1 mol·L-1稀硫酸100 mL中含硫酸根个数为0.1 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实中,能证实一元酸HR是弱电解质的是( )
A.HR溶液和KCl溶液不发生反应
B.能与水以任意比例互溶
C.0.1 mol·L-1 的HR溶液中c(R- ) =0.01 mol·L-1
D.HR属于共价化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com