
科目: 来源: 题型:
【题目】下列实验目的无法实现的是( )
A.用激光笔光束鉴别氯化铁溶液和氢氧化铁胶体
B.用KSCN溶液鉴别Fe3+和Fe2+
C.用NaOH溶液和红色石蕊试纸鉴别溶液是否含NH4+
D.在氢氧化钠溶液中滴入氯化铁饱和溶液可以制得氢氧化铁胶体
查看答案和解析>>
科目: 来源: 题型:
【题目】在标准状况下,将aLHCl(气)溶于1L水中(水的密度为1gcm﹣3),得到的盐酸的密度为bgmL﹣1,质量分数为w,物质的量浓度为cmolL﹣1则下列关系式中不正确的是
A.w=![]()
B.w=![]()
C.C=![]()
D.b=![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是

A.如图可表示水分解过程中的能量变化
B.若2C(s)+O2(g)=2CO(g) △=-221.0kJ/mol,则碳的燃烧热为110.5kJ/mol
C.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应
D.已知I:反应H2(g)+Cl2(g)=2HCl(g) △=-akJ/mol
II: ![]()
且a、b、c均大于零,则断开1mol H—Cl键所需的能量为(-a-b-c)kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。
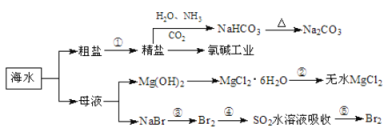
下列有关说法正确的是
A.在第③、④、⑤步骤中,溴元素均被氧化
B.制取NaHCO3的反应是利用其在此反应所涉及物质中溶解度最小
C.用澄清的石灰水可鉴别NaHCO3和Na2CO3
D.工业上通过电解饱和MgCl2溶液制取金属镁
查看答案和解析>>
科目: 来源: 题型:
【题目】

(1)该浓盐酸中HCl的物质的量浓度为__________mol·L-1。
(2)某学生欲用该浓盐酸和蒸馏水配制成1mol·L-1的稀盐酸。现实验室仅需要这种盐酸220mL,试回答下列问题:
①经计算需要______mL浓盐酸,在量取时宜选用下列量筒中的______。
A.5mL |
B.10mL |
C.25mL |
D.50mL |
②在量取浓盐酸后,进行了下列操作:
a等稀释的盐酸的温度与室温一致后,沿玻璃棒注入容量瓶中。
b往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度标线相切。
c在盛盐酸的烧杯中注入蒸馏水,并用玻璃棒搅动,使其混合均匀。
d用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)____________。若量取的是浓硫酸,简述第c步实验的操作过程。
③在上述配制过程中,用量筒量取浓盐酸时仰视观察凹液面,其配制的稀盐酸浓度________(填“偏高”、“偏低”或“无影响”,下同)。若定容后把容量瓶倒置摇匀,发现液面低于刻度线,又加水至刻度线,则配制的稀盐酸浓度________
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下列仪器: ①烧杯 ②蒸馏烧瓶 ③冷凝管 ④普通漏斗 ⑤分液漏斗 ⑥蒸发皿 ⑦玻璃棒 ⑧铁架台(带铁圈、铁夹) ⑨酒精灯 ⑩温度计
①在过滤时需要用到的有 (填序号,下同)。
②在蒸馏时需要用到的有 。
③在萃取时需要用到的有 。
④在蒸发结晶时需要用到的有 。
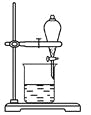
(2)用CCl4萃取碘水中的碘在右图的分液漏斗中,下层液体呈________色;他们打开分液漏斗活塞,却未见液体流下,原因可能是______________________。
(3)某同学用某种粗盐进行提纯实验,步骤见下图。
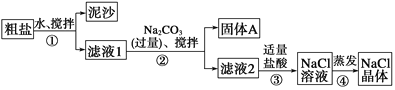
请回答下列问题:
①步骤①和②的操作名称是________。
②步骤③判断加入盐酸“适量”的方法是______________;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止____________,当蒸发皿中有较多量固体出现时,应________,用余热使水分蒸干。
③猜想和验证:
猜想 | 验证的方法 | 现象 | 结论 |
猜想Ⅰ:固体A中含CaCO3、MgCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | _________ | 猜想Ⅰ成立 |
猜想Ⅱ:固体A中含BaCO3 | 取少量固体A于试管中,先滴入__________,再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | ___________ |
猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量NaCl晶体溶于试管中的蒸馏水,____________ | _________ | 猜想Ⅲ成立 |
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式中正确的是( )
A.Cu溶于稀HNO3:Cu+2 H++NO![]() ===Cu2++NO2↑+H2O
===Cu2++NO2↑+H2O
B.用石墨电极电解饱和食盐水:2 Cl-+2 H2O ![]() 2 OH-+H2↑+Cl2↑
2 OH-+H2↑+Cl2↑
C.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-===Fe(OH)2↓
D.向Fe(NO3)3溶液中加入过量的HI溶液:2 Fe3++2 I-===2 Fe2++I2
查看答案和解析>>
科目: 来源: 题型:
【题目】
(1)3.6gH2O物质的量为______mol,约含有_________个原子。
(2)已知1.204×1023个X气体的质量是6.4g。则X气体的摩尔质量是______。
(3)2molNH3与_________L(标准状况)CH4所含氢原子数目相同。
(4)同温同压下,同体积的甲烷(CH4)和CO2分子数之比为________,物质的量之比_______,原子总数之比_________,质量之比为________,密度之比_________。
(5)VLAl2(SO4)溶液中含Al3+amol,溶液的物质的量浓度为__________,取出V/2L再加入水稀释到4VL。则稀释后溶液中SO42-的物质的量浓度是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)在标准状况下15 g CO与CO2的混合气体,体积为11.2 L。则:
①混合气体的平均摩尔质量是___________________。
②混合气体中所含碳原子的物质的量是_____________________。
③CO2和CO的体积之比是_______________________。
(2)标准状况下有①0.112 L水 ②0.5NA个HCl分子③25.6 g SO2气体 ④0.2 mol氨气(NH3) ⑤2 mol He 所含原子个数从大到小的顺序为__________________。
(3)将质量分数为a%,物质的量浓度为c1 mol·L-1的稀H2SO4蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol·L-1,则c1和c2的数值关系是_______________。(用含c1 和c2的代数式表示)
(4)某温度时,一定量的元素A的气态氢化物AH3,在恒温密闭容器中分解为两种气体单质,此时压强增加了75%,则AH3分解反应的化学方程式________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物是药物生产的中间体,其结构简式如图。下列有关叙述正确的是( )

A. 该有机物能与溴水发生加成反应
B. 该有机物与浓硫酸混合加热可发生消去反应
C. 1 mol 该有机物与足量NaOH溶液反应最多消耗3 mol NaOH
D. 该有机物经催化氧化后能发生银镜反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com