
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的ΔH > 0
B.已知2CO(g)+O2(g) = 2CO2(g) ΔH=-566 kJ·mol-1,则CO的燃烧热ΔH=-283 kJ
C.已知H+(aq)+OH-(aq)== H2O(l) ΔH=-57.3 kJ·mol-1,则稀H2SO4溶液和稀Ba(OH)2 溶液反应的反应热ΔH ==2×(-57.3) kJ·mol-1
D.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6 kJ·mol-1
2NH3(g) △H=-38.6 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是
A.稀硫酸和铜粉反应可制备硫酸铜
B.碘化钾与浓硫酸反应可制备碘化氢
C.过氧化钠与二氧化碳反应可制备氧气
D.铝箔在氯气中燃烧可制备无水三氯化铝
查看答案和解析>>
科目: 来源: 题型:
【题目】为探究测定中和热的实验,小明利用50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液,在如图所示的装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热(中和热数值为57.3 kJ/mol)。
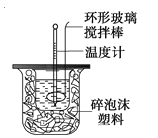
(1)写出实验所进行的中和反应的热化学方程式 。
(2)实验装置中,烧杯间填满碎纸条的作用为 。
(3)该实验中,使用浓度略大于盐酸的NaOH溶液的原因是 ,若改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1,NaOH溶液进行反应,所求中和热的数值_________(填“相等”或“不相等”),理由是 。
(4)小明利用上述装置做实验,测得中和热的数值偏低,请你分析可能的原因是 。
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.做本实验的当天室温较高
C.将量筒中的NaOH(aq)倒入小烧杯时动作迟缓
D.在量取盐酸时仰视读数
E.大烧杯的盖板中间小孔太大
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下列物质中,能导电的是 ,属于电解质的是 (填序号)。
①氨气、②氨水、③NH3·H2O、④硫酸溶液、⑤干冰、⑥BaSO4、⑦金刚石
(2)将等物质的量的①Na、②Na2O、③Na2O2、④NaOH投入相同质量的水中,所得溶液浓度由大到小的顺序为 。如果将等物质的量换成等质量则 。(填序号)
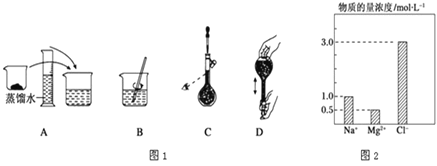
(3)如图表示某同学配制480mL 0.5mol/L 的NaOH溶液的部分操作示意图,其中有错误的是___________,这样操作所配制的溶液比要求的浓度要___________ (填“偏高”、“偏低”、“不影响”)。配制应称取___________gNaOH。
查看答案和解析>>
科目: 来源: 题型:
【题目】A~F六种元素中,除F外其他均为短周期元素,它们的原子结构或性质如下表所示。
元素 | 原子结构或性质 |
A | 其形成的一种同位素原子在考古中可推测化石的年代 |
B | 与A同周期,其最高价氧化物的水化物无论浓、稀溶液均有强氧化性 |
C | 地壳中含量最多的元素 |
D | D原子的内层电子数是最外层电子数的5倍 |
E | 其单质主要存在于火山口附近 |
F | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
请回答下列问题:
(1)A在元素周期表中的位置是_______________;A与C形成的化合物AC2的电子式是__________。
(2) 下列事实能证明C和E的非金属性强弱的是 。(填序号)
①常温下,C的单质呈气态,E的单质呈固态
②C的气态氢化物的稳定性强于E的气态氢化物的稳定性
③C与E形成的化合物中,E呈正价
④E的氢化物的沸点高于C的氢化物的沸点
(3) 由A、B、C和氢元素四种元素所形成的阴、阳离子数目之比为1:1的离子化合物是 (填化学式),它与足量NaOH溶液在加热时反应的离子方程为: 。
(4) FC与足量B的最高价氧化物的水化物的稀溶液反应的离子方程式 。若有标准状况下5.6L的BC生成,则转移的电子数为 。
(5) A的氢化物有多种,1 mol A的某种氢化物分子中含有14 mol电子,已知在25℃、101kPa下,1g该氢化物在足量氧气中完全燃烧生成液态水时放出的热量为40 kJ,写出表示该氢化物燃烧热的热化学方程式: 。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)在常温下,发生下列几种反应:
①16H++10Z-+2XO===2X2++5Z2+8H2O
②2A2++B2===2A3++2B-
③2B-+Z2===B2+2Z-
根据上述反应,XO![]() 、Z2、B2、A3+氧化性从强到弱的顺序为:_________________
、Z2、B2、A3+氧化性从强到弱的顺序为:_________________
(2)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3- + 4H+ + 3e- ═ NO↑ + 2H2O,KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
①写出并配平该氧化还原反应的化学方程式_____________________;
②反应中硝酸体现了______________;
③反应中若产生标准状况下11.2L气体,则转移电子的物质的量是________ mol;
查看答案和解析>>
科目: 来源: 题型:
【题目】物质的量浓度相同的NaNO3、Mg(NO3)2、Al(NO3)3三种溶液的体积比为3:2:1时,三种溶液中c(NO3-)之比为
A.1:1:1 B.1:2:3 C.3:2:1 D.3:4:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com