
科目: 来源: 题型:
【题目】短周期元素X和Y中,X原子的最外层电子数是内层电子总数的一半,Y元素在该元素的前一周期,Y2﹣离子和Ne原子的电子层结构相同,关于X和Y形成的化合物Z的说法正确的是( )
A.Z是一种酸酐
B.Z是一种碱性氧化物
C.Z的分子式一定是X2Y5
D.Z中含有离子键
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
B. 电离能最小的电子能量最高
C. 同是s能级,在不同的电子层中所能容纳的最多电子数是不相同的
D. 核外电子排布完全相同的两种微粒,其化学性质一定相同
查看答案和解析>>
科目: 来源: 题型:
【题目】向浓度相等、体积均为50 mL 的 A、B 两份NaOH 溶液中,分别通入一定量的CO2后,再稀释到100 mL。
(1)在 NaOH 溶液中通入一定量的 CO2 后,溶液中溶质的可能组成是
①_________, ②________, ③________, ④________。
(2)在稀释后的溶液中逐滴加入0.2 mol/L 的盐酸,产生 CO2 的体积(标准状况)与所加盐酸的体积关系如图所示。
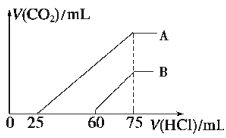
①A 曲线表明,原溶液通入CO2后,所得溶质与盐酸反应产生 CO2 的最大体积是_________mL(标准状况)。
②B 曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为______________。
③原 NaOH 溶液的物质的量浓度为________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】欧盟原定于2012年1月1日起征收航空碳排税以应对冰川融化和全球变暖,使得对如何降低大气中CO2的含量及有效地开发利用碳资源显得更加紧迫。请运用化学反应原理的相关知识研究碳及其化合物的性质。
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯, 请完成该反应的化学方程式
_____C+____ KMnO4+____H2SO4→____CO2↑+_____MnSO4+ ______K2SO4+_____H2O
(2)焦炭可用于制取水煤气,测得12g碳与水蒸气完全反应生成水煤气时,吸收了131.6kJ热量。
反应的热化学方程式为_________________。
(3)工业上在恒容密闭容器中用下列反应合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g) △H=akJ/mol 如表所列数据是反应在不同温度下的化学平衡常数(K)。
CH3OH(g) △H=akJ/mol 如表所列数据是反应在不同温度下的化学平衡常数(K)。

① 判断反应达到平衡状态的依据是___________。(填序号)
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的平均相对分子质量不变
C.混合气体的密度不变
D.CH3OH、CO、H2的浓度都不再发生变化
②某温度下,将2molCO和一定量的H2充入2L的密闭容器中,充分反应l0min后,达到平衡时测得c(CO)=0.2 mol/L,则以H2表示的反应速率v(H2)=________。
(4)CO还可以用做燃料电池的燃料,某熔融盐燃料电池具有高的发电效率,因而受到重视,该电池用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混和气为正极助燃气,制得在650℃下的燃料电池,其正极反应式:O2+2CO2+4e-=2CO32-,则负极反应式为___________________。
(5)向BaSO4沉淀中加入饱和碳酸钠溶液,充分搅拌,弃去上层淸液,如此处理多次,可使BaSO4 全部转化为BaCO3发生反应:BaSO4(s) + CO32-(aq)=BaCO3(s) +SO42-(aq)。己知某温度下该 反应的平衡常数 K=4.0×10-2,BaSO4的Ksp=1.0×10-10,则 BaCO3的溶度积 Ksp=______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图所示的四个容器中分别盛有不同的溶液,除a、b外,其余电极均为石墨电极。甲为铅蓄电池,其工作原理为:Pb + PbO2+2H2SO4![]() 2PbSO4+2H2O,其两个电极的电极材料分别为PbO2和Pb。闭合K,发现g电极附近的溶液先变红,20min后,将K断开,此时c、d两极上产生的气体体积相同:据此回答:
2PbSO4+2H2O,其两个电极的电极材料分别为PbO2和Pb。闭合K,发现g电极附近的溶液先变红,20min后,将K断开,此时c、d两极上产生的气体体积相同:据此回答:
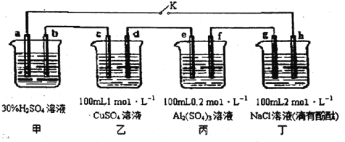
(1) a电极的电极材料是____________________ (填“PbO2”或“Pb”)。
(2)丙装置中发生电解的总反应方程式为_____________________。
(3)电解20min时,停止电解,此时要使乙中溶液恢复到原来的状态,需要加入的物质及其物质的量是________________。
(4)20min后将乙装置与其他装置断开,然后在c、d两极间连接上灵敏电流计,发现电流计指针偏转,则此时c电极为_______极,d电极上发生反应的电极反应式为_____________。
(5)电解后取amL丁装置中的溶液,向其中逐滴加入等物质的量浓度的CH3COOH溶液,当加入 bmLCH3COOH溶液时,混合溶液的pH恰好等于7(体积变化忽略不计)。己知CH3COOH 的电离平衡常数为1.75×10-5,则a/b=________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 原子晶体中的相邻原子都以共价键相结合
B. 金属晶体的熔点都比分子晶体的熔点高
C. 干冰升华时,分子内共价键会发生断裂
D. BaO2(过氧化钡)固体中的阴离子和阳离子个数比为2:1
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下向10mL0.1mol·L-1的HR溶液中逐滴滴入0.1 mol·L-1的NH3·H2O溶液,所得溶液pH及导电性变化如图。下列分析不正确的是
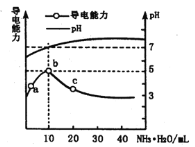
A.ab点导电能力增强,说明HR为弱酸
B.b点溶液pH=7说明NH4R没有发生水解
C.c 点溶液存在 c(NH4+)>c(R-)、c(OH-)>c(H+)
D.b~c任意点溶液均有 c(H+)·c(OH-)=KW=1.0×10-14
查看答案和解析>>
科目: 来源: 题型:
【题目】如下图是课外活动小组的同学设计的 4 个喷泉实验方案。下列有关操作不可能引发喷泉现象的是( )
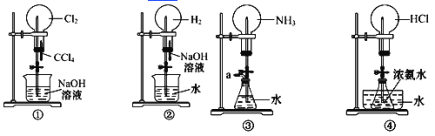
A.挤压装置①的胶头滴管使 CCl4。全部进入烧瓶,片刻后打开止水夹
B.挤压装置②的胶头滴管使 NaOH 溶液全部进入烧瓶,片刻后打开止水夹
C.用鼓气装置从装置③的 a 处不断鼓入空气并打开止水夹
D.向装置④的水槽中慢慢加入足量浓硫酸并打开止水夹
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com