
їЖДїЈє АґФґЈє МвРНЈє
ЎѕМвДїЎїПВБРОпЦКЦРКфУЪјоРФСх»ЇОпµДКЗ(ЎЎЎЎ)
A. MgO B. Mn2O7 C. Na2O2 D. Fe3O4
Ійїґґр°ёєНЅвОц>>
їЖДїЈє АґФґЈє МвРНЈє
ЎѕМвДїЎїПЦУРX(g)+Y(g)2Z(g),Хэ·ґУ¦·ЕИИ,ґУ·ґУ¦їЄКјѕ№эt1єуґпµЅЖЅєвЧґМ¬Ј¬t2К±УЙУЪМхјюёД±дЈ¬ЖЅєвКЬµЅЖЖ»µЈ¬ФЪt3К±УЦґпµЅЖЅєвЈ¬ѕЭИзНј»ШґрЈєґУt2Ўъt3µДЗъПЯ±д»ЇКЗУЙДДЦЦМхјюТэЖрµД( )
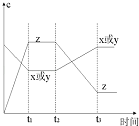
AЈ®ФцґуX»тYµДЕЁ¶И BЈ®ФцґуС№Зї
CЈ®ФцґуZµДЕЁ¶И DЈ®ЙэёЯОВ¶И
Ійїґґр°ёєНЅвОц>>
їЖДїЈє АґФґЈє МвРНЈє
ЎѕМвДїЎїИзНјЛщКѕµДОЮ»ъОпµДЧЄ»Ї№ШПµЦРЈ¬Ії·ЦЙъіЙОпєН·ґУ¦МхјюТСВФИҐЎЈЖдЦРAУлFКЗБЅЦЦЛбКЅСОЈ»іЈОВПВBЎўCЎўYЎўZКЗЖшМеЈ¬ЗТBДЬК№ZµДЛ®ИЬТєНКЙ«Ј»EКЗТ»ЦЦіЈјыµД»Ї·КЈ»XЦРє¬УР20ёцµзЧУЎЈ

ЈЁ1Ј©РґіцXµДµзЧУКЅЈє________________ Ј»EЦРє¬УРµД»ЇС§јьАаРНКЗ________________ЎЈ
ЈЁ2Ј©ZУлCТФОпЦКµДБїЦ®±И31·ґУ¦ТІДЬЙъіЙGЈ¬Н¬К±ЙъіЙБнТ»ЦЦ¶юФЄ»ЇєПОпHЈ¬ТСЦЄёГ·ґУ¦ ЦРЦ»УРТ»ЦЦФЄЛШµД»ЇєПјЫ·ўЙъёД±дЈ¬ФтHµД»ЇС§КЅОЄ________________ЎЈHґуБїУГУЪГж·ЫµДЖЇ°ЧєНПы¶ѕЈ¬ЛьУлЛ®·ґУ¦µД»ЇС§·ЅіМКЅОЄ________________ЎЈ
ЈЁ3Ј©Ѕ«Ме»эѕщОЄ560 mL(±кЧјЧґїц)µДBєНZН¬К±»є»єНЁИлЛ®ЦРЈ¬µГµЅ1.0 LИЬТєЈ¬ФтИЬТєЦРc(H Ј« )ЈЅ________mol/LЎЈ
ЈЁ4Ј©AЎ«GЖЯЦЦОпЦКЦРЈ¬КфУЪµзЅвЦКµДУР________ЦЦЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈє АґФґЈє МвРНЈє
ЎѕМвДїЎїЎ°µНМјС»·Ў±ТэЖрёч№ъµДёЯ¶ИЦШКУЈ¬¶шИзєОЅµµНґуЖшЦРCO2µДє¬Бїј°УРР§µШїЄ·ўАыУГCO2Ј¬ТэЖрБЛИ«КАЅзµДЖХ±йЦШКУЎЈЛщТФЎ°µНМјѕјГЎ±ХэіЙОЄїЖС§јТСРѕїµДЦчТЄїОМвЎЈ
(1)ТСЦЄЈєўЩ CO(g)+H2O(g)![]() H2(g)+CO2(g) ¦¤HЈЅЈ41 kJЎ¤molЈ1
H2(g)+CO2(g) ¦¤HЈЅЈ41 kJЎ¤molЈ1
ўЪ C(s)+2H2(g)![]() CH4(g) ¦¤HЈЅЈ73 kJЎ¤molЈ1
CH4(g) ¦¤HЈЅЈ73 kJЎ¤molЈ1
ўЫ 2CO(g)![]() C(s)+CO2(g) ¦¤HЈЅЈ171 kJЎ¤molЈ1
C(s)+CO2(g) ¦¤HЈЅЈ171 kJЎ¤molЈ1
РґіцCO2УлH2·ґУ¦ЙъіЙCH4єНH2O(g)µДИИ»ЇС§·ЅіМКЅ ЎЈ
(2)Ѕ«ИјГє·ПЖшЦРµДCO2ЧЄ»ЇОЄ¶юјЧГСµД·ґУ¦ФАнОЄЈє
2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)
ТСЦЄТ»¶ЁМхјюПВЈ¬ёГ·ґУ¦ЦРCO2µДЖЅєвЧЄ»ЇВКЛжОВ¶ИЎўН¶БП±И[n(H2)/n(CO2)]µД±д»ЇЗъПЯИзПВЧуНјЈє
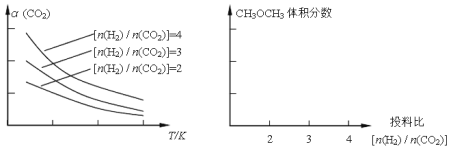
ўЩФЪЖдЛыМхјюІ»±дК±Ј¬ЗлФЪЙПНјЦР»іцЖЅєвК±CH3OCH3µДМе»э·ЦКэЛжН¶БП±И[n(H2)/n(CO2)]±д»ЇµДЗъПЯНјЎЈ
ўЪДіОВ¶ИПВЈ¬Ѕ«2.0 mol CO2(g)єН6.0 mol H2(g)ідИлИЭ»эОЄ2LµДГЬ±ХИЭЖчЦРЈ¬·ґУ¦µЅґпЖЅєвК±Ј¬ёД±дС№ЗїєНОВ¶ИЈ¬ЖЅєвМеПµЦРCH3OCH3(g)µДОпЦКµДБї·ЦКэ±д»ЇЗйїцИзПВНјЛщКѕЈ¬№ШУЪОВ¶ИєНС№ЗїµД№ШПµЕР¶ПХэИ·µДКЗ ЎЈ
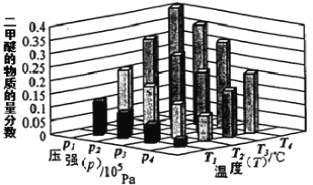
A. P3>P2Ј¬T3>T2 B. P1>P3Ј¬T1>T3
C. P2>P4Ј¬T4>T2 D. P1>P4Ј¬T2>T3
(3)Гє»Ї№¤НЁіЈНЁ№эСРѕїІ»Н¬ОВ¶ИПВЖЅєвіЈКэТФЅвѕцёчЦЦКµјКОКМвЎЈТСЦЄµИМе»эµДCOєНЛ®ХфЖшЅшИл·ґУ¦ЖчК±Ј¬»б·ўЙъИзПВ·ґУ¦ЈєCO(g)+H2O(g)![]() H2(g)+CO2(g)Ј¬ёГ·ґУ¦ЖЅєвіЈКэЛжОВ¶ИµД±д»ЇИзПВ±нЛщКѕЈє
H2(g)+CO2(g)Ј¬ёГ·ґУ¦ЖЅєвіЈКэЛжОВ¶ИµД±д»ЇИзПВ±нЛщКѕЈє
ОВ¶И/Ўж | 400 | 500 | 800 |
ЖЅєвіЈКэK | 9.94 | 9 | 1 |
ёГ·ґУ¦µДЖЅєвіЈКэµД±нґпКЅОЄЈє
ёГ·ґУ¦µДХэ·ґУ¦·ЅПтКЗ ·ґУ¦(МоЎ°ОьИИЎ±»тЎ°·ЕИИЎ±)Ј¬ИфФЪ500ЎжК±ЅшРРЈ¬ЙиЖрКјК±COєНH2OµДЕЁ¶ИѕщОЄ0.020 molЎ¤L-1Ј¬ФЪёГМхјюПВCOµДЖЅєвЧЄ»ЇВКОЄ ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈє АґФґЈє МвРНЈє
ЎѕМвДїЎїТСЦЄAОЄЦРС§»ЇС§ЦРµДТ»ЦЦСОЈ¬BЎўCОЄИХіЈЙъ»оЦРіЈјыµДЅрКф,АлЧУУРПаН¬»ЇєПјЫЎЈНЁіЈМхјюПВDОЄОЮЙ«ОЮО¶ЖшМеЈ¬ОЮЙ«ЖшМеGУцїХЖш±дємЧШЙ«ЎЈТСЦЄУГ¶иРФµзј«µзЅвAИЬТєТ»¶ОК±јдєуЈ¬ІъОпЦ»УРCЎўDєНEµДПЎИЬТєЎЈёчОпЦКЦ®јдµДЧЄ»Ї№ШПµИзПВНјЈЁІї·Ц·ґУ¦ІъОпТСВФИҐЈ©ЎЈ

Зл»ШґрПВБРОКМвЈє
ЈЁ1Ј©AµД»ЇС§КЅОЄ__________ЎЈ
ЈЁ2Ј©AИЬТєУлNa 2 O 2 ·ґУ¦µДЧЬ»ЇС§·ЅіМКЅОЄ__________ЎЈ
ЈЁ3Ј©EµДПЎИЬТєУлFИЬТє·ґУ¦µДАлЧУ·ЅіМКЅОЄ__________ЎЈ
ЈЁ4Ј©ИфПт100mLСОAµДИЬТєЦРјУИл10gЅрКфµҐЦКBµД·ЫД©Ј¬ід·ЦЅБ°иєуЈ¬№эВЛЈ¬єжёЙµГ10.16g№ММеЈ¬ФтВЛТєЦРИЬЦКµДОпЦКµДБїЕЁ¶ИОЄ__________ЎЈЈЁјЩЙиИЬТєМе»эІ»±дЈ©
Ійїґґр°ёєНЅвОц>>
їЖДїЈє АґФґЈє МвРНЈє
ЎѕМвДїЎїјЧНй№г·єґжФЪУЪМмИ»ЖшЎўХУЖшЎўГєїуїУЖшЦ®ЦР,КЗУЕЦКµДЖшМеИјБП,ёьКЗЦЖФмРн¶а»Ї№¤ІъЖ·µДЦШТЄФБПЎЈ
ўсЈ®ЦЖИЎЗвЖш
ТСЦЄЈєCH4ЈЁgЈ©+H2OЈЁgЈ©![]() COЈЁgЈ©+3H2ЈЁgЈ© ЎчH=+206.2kJЎ¤mol-1
COЈЁgЈ©+3H2ЈЁgЈ© ЎчH=+206.2kJЎ¤mol-1
CH4ЈЁgЈ©+CO2ЈЁgЈ©![]() 2COЈЁgЈ©+2H2ЈЁgЈ© ЎчH=+247.4kJЎ¤mol-1
2COЈЁgЈ©+2H2ЈЁgЈ© ЎчH=+247.4kJЎ¤mol-1
ЈЁ1Ј©ЗлРґіцCH4ЈЁgЈ©УлH2OЈЁgЈ©·ґУ¦ЙъіЙCO2ЈЁgЈ©єНH2ЈЁgЈ©µДИИ»ЇС§·ЅіМКЅ___________________
ЈЁ2Ј©ИфЅ«0.1mol CH4єН0.1mol H2OЈЁgЈ©НЁИлМе»эОЄ10LµДГЬ±ХИЭЖчАпЈ¬ФЪТ»¶ЁМхјюПВ·ўЙъ·ґУ¦ЈєCH4ЈЁgЈ©+H2OЈЁgЈ©![]() COЈЁgЈ©+3H2ЈЁgЈ©,CH4µДЖЅєвЧЄ»ЇВКУлОВ¶ИЎўС№ЗїµД№ШПµИзНј
COЈЁgЈ©+3H2ЈЁgЈ©,CH4µДЖЅєвЧЄ»ЇВКУлОВ¶ИЎўС№ЗїµД№ШПµИзНј

ўЩТСЦЄ100ЎжК±ґпµЅЖЅєвЛщРиµДК±јдОЄ5minЈ¬ФтУГH2±нКѕµДЖЅѕщ·ґУ¦ЛЩВК_________Ј»
ўЪёГ·ґУ¦µД»ЇС§ЖЅєвіЈКэ___________________Ј»
ўЫНјЦРµДp1 p2ЈЁМоЎ°ЈјЎ±ЎўЎ°ЈѕЎ±»тЎ°=Ў±Ј©Ј»
ўтЈ®ЦЖ±ёјЧґј
ЈЁ3Ј©ФЪС№ЗїОЄ0.1MPaМхјюПВЈ¬Ѕ«a mol COУл3amol H2µД»мєПЖшМеФЪґЯ»ЇјБЧчУГПВДЬЧФ·ў·ґУ¦ЙъіЙјЧґјЈєCOЈЁgЈ©+2H2ЈЁgЈ©![]() CH3OHЈЁgЈ© ЎчHЈј0ЎЈИфИЭЖчИЭ»эІ»±дЈ¬ПВБРґлК©їЙФцјУјЧґјІъВКµДКЗ________Ј»
CH3OHЈЁgЈ© ЎчHЈј0ЎЈИфИЭЖчИЭ»эІ»±дЈ¬ПВБРґлК©їЙФцјУјЧґјІъВКµДКЗ________Ј»
AЈ®ЙэёЯОВ¶И
BЈ®ФЩідИл1mol COєН3mol H2
CЈ®Ѕ«CH3OHЈЁgЈ©ґУМеПµЦР·ЦАл
DЈ®ідИлHeЈ¬К№МеПµЧЬС№ЗїФцґу
EЈ®К№УГёьёЯР§µДґЯ»ЇјБ
ўуЈ®єПіЙТТЛб
ЈЁ4Ј©јЧНйЦ±ЅУєПіЙТТЛбѕЯУРЦШТЄµДАнВЫТвТеєНУ¦УГјЫЦµЎЈ№вґЯ»Ї·ґУ¦јјКхК№УГCH4єН ЈЁМо»ЇС§КЅЈ©Ц±ЅУєПіЙТТЛбЈ¬ЗТ·ыєПЎ°ВМЙ«»ЇС§Ў±µДТЄЗуЈЁФЧУАыУГВК100ЁGЈ©ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈє АґФґЈє МвРНЈє
ЎѕМвДїЎїДіС§П°РЎЧйЅшРРЕЁБтЛб¶ФХбМЗµДНСЛ®КµСйЈ¬Ў°ФЪ200 mLЙХ±ЦР·ЕИл20 gХбМЗ(C12 H22 O11 )Ј¬јУИлККБїЛ®Ј¬ЅБ°иѕщФИЈ¬И»єуФЩјУИл15 mLЦКБї·ЦКэОЄ98%µДЕЁБтЛбЈ¬СёЛЩЅБ°иЎ±ЅшРРИзПВМЅѕїЎЈ
ЈЁ1Ј©№ЫІмПЦПуЈєХбМЗПИ±д»ЖЈ¬ФЩЦ𽥱дєЪЈ¬Ме»эЕтХНЈ¬РОіЙКиЛЙ¶аїЧµДєЈГаЧґєЪЙ«ОпЦКЈ¬Н¬К±ОЕµЅґМј¤РФЖшО¶ЎЈ°ґС№ґЛєЪЙ«ОпЦКК±Ј¬ёРѕхЅПУІЈ¬·ЕФЪЛ®ЦРіКЖЇёЎЧґМ¬ЎЈ
Н¬С§ГЗУЙЙПКцПЦПуНЖІвіцПВБРЅбВЫЈєўЩЕЁБтЛбѕЯУРЗїСх»ЇРФЈ»ўЪЕЁБтЛбѕЯУРОьЛ®РФЈ»ўЫЕЁБтЛбѕЯУРНСЛ®РФЈ»ўЬЕЁБтЛбѕЯУРЛбРФЈ»ўЭєЪЙ«ОпЦКѕЯУРЗїОьёЅРФЈ¬ЖдЦРТАѕЭІ»ід·ЦµДКЗ (МоРтєЕ)ЎЈ
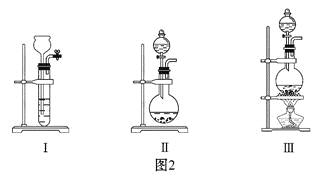
ЈЁ2Ј©ОЄБЛСйЦ¤ХбМЗУлЕЁБтЛб·ґУ¦ЙъіЙµДЖшМ¬ІъОпЈ¬Н¬С§ГЗЙијЖБЛИзПВЧ°ЦГЈє
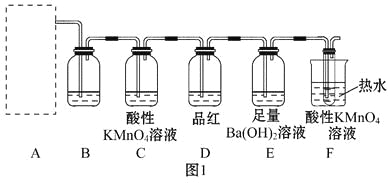
КФ»ШґрПВБРОКМвЈє
ўЪ Нј1µДAЦРЧоєГСЎУГНј2ЦРµДЧ°ЦГ (Мо±аєЕ)ЎЈ
ўЪНј1µДBЧ°ЦГЛщЧ°КФјБКЗ Ј»DЧ°ЦГЦРКФјБµДЧчУГКЗ Ј»
EЧ°ЦГЦР·ўЙъµДПЦПуКЗ ЎЈ
ўЫ Нј1µДAЧ°ЦГЦРК№ХбМЗПИ±дєЪµД»ЇС§·ґУ¦·ЅіМКЅОЄ Ј»єуМе»эЕтХНµД»ЇС§·ЅіМКЅОЄ ЎЈ
ўЬ ДіС§ЙъЅшРРКµСйК±Ј¬·ўПЦDЖїЖ·ємІ»НКЙ«Ј¬EЧ°ЦГЦРУРЖшМеТЭіцЈ¬FЧ°ЦГЦРЛбРФёЯГМЛбјШИЬТєСХЙ«±дЗіЈ¬НЖІвFЧ°ЦГЦРЛбРФёЯГМЛбјШИЬТєСХЙ«±дЗіµДФТт ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈє АґФґЈє МвРНЈє
ЎѕМвДїЎїУР№ШДЬФґµДЛµ·ЁІ»ХэИ·µДКЗ(ЎЎЎЎ)
A. ЗвДЬЎўєЛДЬѕщКЗОЮОЫИѕµДёЯР§ДЬФґ B. №«№ІЖыіµґуІї·ЦІЙУГМмИ»ЖшЧчОЄИјБПїЙјхЙЩ¶ФґуЖшµДОЫИѕ
C. °СГєЧЄ»ЇОЄТєМ¬ИјБПїЙМбёЯГєµДИјЙХР§ВК D. »ЇКЇДЬФґКЗ·ЗФЩЙъДЬФґ
Ійїґґр°ёєНЅвОц>>
їЖДїЈє АґФґЈє МвРНЈє
ЎѕМвДїЎїФЪјоРФИЬТєЦРДЬґуБї№ІґжЗТИЬТєОЄОЮЙ«НёГчµДАлЧУЧйКЗЈЁ Ј©
A.K+ЎўMnO4©ЃЎўNa+ЎўCl©Ѓ
B.K+ЎўNa+ЎўNO3©ЃЎўCO32©Ѓ
C.Na+ЎўH+ЎўNO3©ЃЎўSO42©Ѓ
D.Fe3+ЎўNa+ЎўCl©ЃЎўSO42©Ѓ
Ійїґґр°ёєНЅвОц>>
їЖДїЈє АґФґЈє МвРНЈє
ЎѕМвДїЎїПВБРіэФУКФјБєН·Ѕ·ЁІ»ХэИ·µДКЗ
±аєЕ | ±»МбґїОпЦКЈЁФУЦКЈ© | іэФУКФјБ | ·ЦАл·Ѕ·Ё |
A | јЧНйЈЁТТП©Ј© | ЛбРФёЯГМЛбјШИЬТє | ПґЖш |
B | ТТП©ЈЁ¶юСх»ЇБтЈ© | ЗвСх»ЇДЖИЬТє | ПґЖш |
C | де±ЅЈЁдеЈ© | ЗвСх»ЇДЖИЬТє | ·ЦТє |
D | ±ЅЈЁ±Ѕ·УЈ© | ЗвСх»ЇДЖИЬТє | ·ЦТє |
A. A B. B C. C D. D
Ійїґґр°ёєНЅвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com