
科目: 来源: 题型:
【题目】A,B均为原子序数1﹣20的元素,已知A的原子序数为n,A2+离子比B2﹣离子少8个电子,则B的原子序数是( )
A.n+4
B.n+6
C.n+8
D.n+10
查看答案和解析>>
科目: 来源: 题型:
【题目】氨对地球上的生物相当重要,它是许多食物和肥料的重要成分。氨也是制造硝酸、化肥、炸药 的重要原料。氨在国民经济中占有重要地位。回答下列问题:
(1)合成氨工业中,合成塔中每产生2 mol NH3,放出92.2 kJ热量。
①工业合成氨的热化学方程式是_______________。
②若起始时向容器内放入1 mol N2和3 mol H2,达平衡后N2的转化率为20%,则反应放出的热量为Q1 kJ,则Q1的数值为____________;若在同体积的容器中充人2 mol N2和6 molH2,达平衡后放出的热量为Q2 kJ,则Q2__________(填“>”、“<”或“=”)2Q1。
③已知:

1 mol N-H键断裂吸收的能量约等于__________kJ。
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行合成氨反应:N2 (g)+3H2 (g)![]() 2NH3 (g),其平衡常数K与温度T的关系如下表:
2NH3 (g),其平衡常数K与温度T的关系如下表:
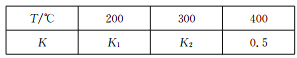
①平衡常数表达式K=_________,K1___________(填“>”、“<”或“一”)K2。
②一定温度下,下列各项能作为判断该反应达到化学平衡状态的依据是__________(填字母)。
a.容器内N2、H2、NH3的浓度之比为1: 3:2
b.浓度商Q=平衡常数K
c.容器内压强保持不变
d.混合气体的密度保持不变
③在400℃时,当测得N2、H2和NH3的物质的量分别为2 mol、1 mol、2 mol时,则此时该反应_________(填“处于”或“不处于”)平衡状态。
查看答案和解析>>
科目: 来源: 题型:
【题目】Fe(OH)3可用来制颜料、药物,作净水剂。现设计实验研究制备Fe(OH)3的方法。
资料:新制Fe(OH)3在溶液中存在两种电离:Fe3++3OH-![]() Fe(OH)3
Fe(OH)3![]() H++FeO2-+H2O
H++FeO2-+H2O
(1)向3支盛有1 mL 1.0 mol·L-1 FeCl3溶液的试管中,分别加入3 mL不同浓度的NaOH溶液,都产生红褐色沉淀。充分反应后,过滤,取滤液分成两等份,分别进行实验,实验记录如下:
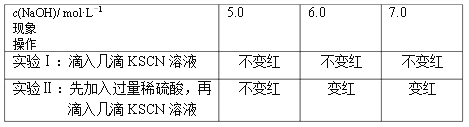
① 产生红褐色沉淀的离子方程式是________。
② 当c(NaOH)≥6.0 mol·L-1时,实验Ⅱ中溶液变红的原因是________、________(用离子方程式表示)。
(2)有同学提出可用某些盐与FeCl3反应制备Fe(OH)3。
① 向1 mL 1.0 mol·L-1 FeCl3溶液中滴加1.0 mol·L-1 Na2CO3溶液,立即有大量气泡并有红褐色沉淀产生。有同学提出沉淀中可能含有碳酸盐。将沉淀过滤、洗涤后取样,________,证明沉淀中含有碳酸盐。
② 向1 mL 1.0 mol·L-1 FeCl3溶液中滴加1.0 mol·L-1 Na2SO3溶液,溶液由黄色变为红色,无丁达尔效应,继续滴加Na2SO3溶液,最终得到红褐色沉淀。经检验沉淀中除Fe(OH)3外还含有FeSO3。产生FeSO3的原因是_________________。
(3)比较(1)和(2),制备Fe(OH)3的合理方法是___________(注明试剂和用量)。
(4)FeSO4溶液仅与一种试剂反应也可制Fe(OH)3,该试剂的化学式是________(写出一种即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.有的共价化合物在液态时也能导电
B.含有离子键的化合物中,也可能还含有共价键
C.形成离子键的微粒必须是金属阳离子与阴离子
D.非金属元素形成的化合物一定不存在离子键
查看答案和解析>>
科目: 来源: 题型:
【题目】检验氯化氢气体中是否混有Cl2,可采用的方法是( )
A. 用干燥的蓝色石蕊试纸
B. 用干燥有色布条
C. 将气体通入硝酸银溶液
D. 用湿润的淀粉碘化钾试纸
查看答案和解析>>
科目: 来源: 题型:
【题目】2015年末,在巴黎召开的全球气候变化大会讨论了“全球气温升高过快”的议题。该议题的实质是如何减少排放下列气体中的
A. H2 B. CO2 C. N2 D. O2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质中既含有离子键又含有共价键的是( )
A. NaOH、H2O、NH4Cl B. KOH、Na2O2、(NH4)2S
C. H2O2 、MgO、Na2SO4 D. CaBr2 、HCl、 MgCl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com