
科目: 来源: 题型:
【题目】现有甲、乙两种易溶于水的化合物,已知甲的水溶液不导电,乙的水溶液能导电,下列有关说法正确的是( )
A.甲一定是共价化合物,乙一定是离子化合物
B.甲一定是共价化合物,乙可能是共价化合物
C.甲可能是离子化合物,乙可能是共价化合物
D.甲一定是离子化合物,乙可能是共价化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】用已知浓度的NaOH溶液滴定未知浓度的醋酸溶液,下列操作会使测定结果偏低的有
A. 以酚酞作指示剂
B. 锥形瓶中有少量水
C. 滴定前,滴定管尖嘴部分有气泡,滴定后气泡消失
D. 滴定前仰视滴定管读数,滴定后平视读数
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于铜锌稀H2SO4构成的原电池的有关叙述错误的是( )
A. 锌为负极,锌发生氧化反应
B. 铜为正极,但铜不发生反应
C. 负极发生还原反应,正极发生氧化反应
D. 外电路电子流入的一极为正极,电子流出的一极为负极
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 纳米泡沫碳与金刚石互为同位素 B. H2O与D2O互为同分异构体
C. CH3CH2COOH与CH3COOH互为同系物 D. C3H8的一氯取代物有3种,其沸点各不相同
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验能获得成功的是( )
A.制备溴苯时,将苯与溴水混合,剧烈振荡
B.除去甲烷中混有的二氧化碳时,依次通过烧碱溶液和浓硫酸
C.在酸性高锰酸钾溶液中滴加几滴苯,用力振荡,紫红色褪去
D.在苯中铜氢气制备环己烷
查看答案和解析>>
科目: 来源: 题型:
【题目】格林太太镶有两颗假牙:第一个是黄金的,第二颗是不锈钢的.令人百思不解的是,自从镶上假牙后,格林太太经常头疼、夜间失眠、心情烦躁某同学提出以下几种方案来治疗格林太太的“疾病”,理论上可行的是( )
A.把不锈钢牙都换成铝质假牙
B.把金质假牙换成铝质假牙
C.把不锈钢假牙换成金质假牙
D.在不锈钢假牙表面镀上一层金
查看答案和解析>>
科目: 来源: 题型:
【题目】某种胃药的止酸剂为碳酸钙,测定每片中碳酸钙含量的方法有以下几步操作(设药片中的其他成分不与盐酸或氢氧化钠反应):
①配制0.100 mol·L-1稀盐酸和0.100 mol·L-1氢氧化钠溶液,
②取一粒药片(药片质量相同,均为0.100 g),研碎后加入20.0 mL蒸馏水
③以酚酞为指示剂,用0.100 mol·L-1氢氧化钠溶液滴定,用去体积为V时达到终点
④加入25.00 mL 0.100 mol·L-1稀盐酸。
请回答下列问题
(1)测定过程的正确操作顺序为:________________(填序号)。
(2)测定过程中发生反应的离子方程式为:__________________、___________________。
(3)若某次实验需重复测定4次。实验室现有50 mL、100 mL、250 mL、500 mL四种规格的容量瓶,则配制稀盐酸应选用的容量瓶规格最好为________________,理由是__________________。
(4)某同学四次测定的V数据如下:
测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
V/mL | 12.9 | 15.4 | 13.1 | 13.0 |
请根据这位同学的实验数据,计算药片中碳酸钙的质量分数________________。
(5)下列实验操作会引起测量结果偏低的是 。
①用天平称量NaOH固体,将小烧杯放在右盘,砝码放在左盘,并移动游码,使之平衡②滴定前滴定管尖嘴有气泡,滴定后尖嘴气泡消失 ③中和滴定时,锥形瓶内有少量蒸馏水④滴定管用蒸馏水洗后,未用标准液洗⑤读取滴定管终点读数时,仰视刻度线。
查看答案和解析>>
科目: 来源: 题型:
【题目】【加试题】乳酸亚铁:{[CH3CH(OH)COO]2Fe·3H2O,M=288.0g/mol}是一中新型的优良补铁剂,绿白色晶体,溶于水,几乎不溶于乙醇。某研究性学习小组欲从硫铁矿烧渣(主要成分为Fe2O3、SiO2、Al2O3)出发,先制备绿矾,再合成乳酸亚铁。
已知:
①几种金属离子生成氢氧化物沉淀的PH(开始沉淀的PH按金属离子浓度为1.0mol/L计算)。
金属离子 | 开始沉淀的PH | 沉淀完全的PH |
Fe3+ | 1.1 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 5.8 | 8.8 |
②研究性学习小组设计的由烧渣制备绿矾晶体的操作流程如下:
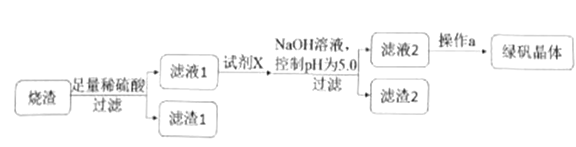
③由绿矾(FeSO4·7H2O)制备乳酸亚铁涉及下列反应:
FeSO4+Na2CO3=FeCO3↓+Na2SO4
2CH3CH(OH)COOH+FeCO3+2H2O![]() [CH3CH(OH)COO]2Fe·3H2O+CO2↑。
[CH3CH(OH)COO]2Fe·3H2O+CO2↑。
请回答:
(1)滤渣2的成分为__________(写化学式)。
(2)操作a为蒸发浓缩、冷却结晶、抽滤、洗涤、干燥。洗涤绿矾粗产品的具体操作为_______。
(3)据题干信息,欲制备较纯净的FeCO3时,某同学设计的实验装置示意图如图所示(夹持装置省略)。仪器A 中存放的试剂为________,装置C的作用为___________。
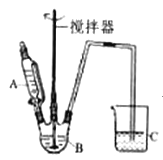
(4)在室温下,将所得的乳酸亚铁成品用无水乙醇进行浸泡2次,从而得到精制产品。选择用无水乙醇进行浸泡的优点是___________(写出两点)。
(5)该学习小组同学用KMnO4滴定法测定样品中Fe2+的量进而计算产品中乳酸亚铁的纯度,发现结果总是大于100%,其原因可能是___________。
经查阅文献后,小组同学改用Ce(SO4)2标准溶液滴定进行测定。反应中Ce4+离子的还原产物为Ce3+。测定时,先称取0.576g样品,溶解后进行必要处理,用0.1000mol/L Ce(SO4)2标准溶液滴定至终点,记录数据如下表。
滴定次数 | 0.1000mol/L Ce(SO4)2标准溶液体积/mL | |
滴定前读数 | 滴定后读数 | |
1 | 0.10 | 19.85 |
2 | 0.12 | 21.32 |
3 | 1.05 | 20.70 |
则产品中乳酸亚铁的纯度为________(以质量分数表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】【加试题】药物K可用于治疗哮喘、系统性红斑狼疮等。其合成路线如下图所示。
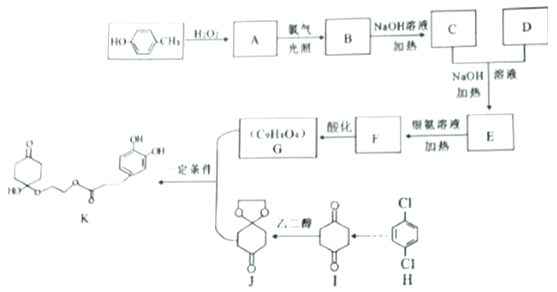
已知:
①通常在同一个碳原子上连有两个烃基不稳定,易脱水形成羰基
②醛能发生烃醛缩合反应,再脱水生成不饱和醛:
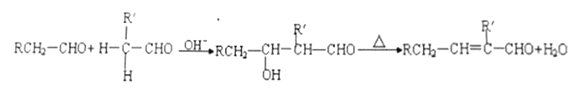
③
请回答:
(1)下列说法不正确的是_______
A.化合物A能与FeCl3发生显色反应
B.化合物C能够发生银镜反应
C.I转化为J属于加成反应
D.K与足量NaOH溶液反应时,1molK最多可消耗3molNaOH
(2)化合物D的结构简式为_______。
(3)E![]() F的化学方程式为___________。
F的化学方程式为___________。
(4)写成符合下列条件的A的所有同分异构体的结构简式_______。
①能与氯化铁溶液发生显色反应
②1H-NMR谱显示分子中苯环上有两种不同化学环境的氢原子
(5)通常采用有机物H为原料合成有机物I,请设计该合成路线_______(用流程图表示,无机试剂任选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com