
科目: 来源: 题型:
【题目】W、X、Y、Z是短周期元素,其部分性质如下表:
W | 单质是淡黄色固体 |
X | 在地壳中的含量居第二位 |
Y | 原子最外层电子数是电子总数的 |
Z | 第三周期原子半径最小的金属元素 |
下列说法正确的是
A. 气态氢化物的热稳定性:X>W B. Z的氧化物中含有非极性共价键
C. 离子半径:Z>W D. 最高价氧化物对应水化物的酸性:Y>X
查看答案和解析>>
科目: 来源: 题型:
【题目】下列烷烃含量越高,汽油品质越好的是( )
A. CH3(CH2)6CH3
B. CH3CH(CH3)CH2CH2CH3
C. (CH3)2CHCH2C(CH3)3
D. CH3(CH2)14CH3
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:SO32-+I2+H2O= SO42-+2I-+2H+。某无色溶液中可能含有I-、NH4+、Cu2+、SO32-,向该溶液中加入少量溴水,溶液仍呈无色,下列关于溶液组成的判断正确的是
①肯定不含I- ②肯定不含Cu2+ ③肯定含有SO32 - ④可能含有I-
A. ①③ B. ①②③ C. ①② D. ②③④
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示装置中,电流表G指针发生偏转,同时X极放出气体,Y极逐渐变细。下列判断正确的是

A.X是Zn,Y是Cu,Z为稀HCl溶液
B.X是Cu,Y是Zn,Z为稀H2SO4溶液
C.X是Cu,Y是石墨,Z为稀AgNO3溶液
D.X是石墨,Y是Fe,Z为稀AgNO3溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]俗称莫尔盐,是浅绿色晶体,可溶于水,在100℃~110℃时分解,常用作定量分析中的标准试剂。某化学小组以废铁屑为原料在实验室中进行实验探究——制备硫酸亚铁铵并检验其纯度,过程如下:
I.制备硫酸亚铁铵
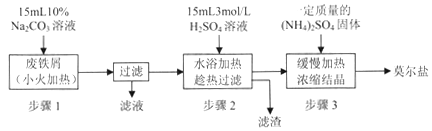
请回答下列问题:
(1)步骤l的作用是_________。(用离子方程式及必要的文字说明);
(2)步骤2中所加硫酸需过量,且不宜等到铁屑完全反应后才过滤,其中蕴含的道理是_______________;
II.测定硫酸亚铁铵的纯度
称取mg实验室制备的硫酸亚铁铵样品,配成500ml溶液,取25. 00mL硫酸亚铁按溶液,用0 . 1mol/L的酸性KMnO4溶液进行滴定,再重复滴定两次。
(3)配制(NH4)2SO4·FeSO4溶液所用的蒸馏水,通常需加热煮沸一段时间后,冷却至室温再使用,这样操作的好处是___________________;
(4)滴定时发生反应的离子方程式为___________________;
(5)滴定终点时的现象为 ___________________;
(6)三次滴定测得酸性KMnO4溶液的用量平均值为VmL,则硫酸亚铁铵样品的纯度为__________;
(7)化学小组分析发现这种检测纯度的方法不够准确,目前处理氮氧化物污染的方法有多种,请你帮助他们设计一种检测方案________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】纳米ZnO的颗粒直径介于1~100nm之间,具有许多特殊的性能,可用于制造变阻器、图像记录材料、磁性材料和塑料薄膜等。一种利用粗ZnO(含FeO、Fe2O3、CuO)制备纳米ZnO的生产工艺流程如下图所示:

已知:① 生成氢氧化物沉淀时溶液的pH如下表:
物质 | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
开始沉淀时pH | 6.34 | 1.48 | 6.2 | 5.2 |
完全沉淀时pH | 9.7 | 3.2 | 8.0 | 6.4 |
② 25℃时,Fe(OH)3的溶度积常数Ksp=4.0×10-38。
请回答以以下问题:
(1)酸浸时,为了提高浸出率,可采取的措施有________(填写两种);
(2)反应1中发生反应的离子方程式为______________,一种双氧水的质量分数为34.0 % (密度为1.13g/cm3) ,其浓度为_______mol/L;
(3)反应2中加适量氨水的目的是_________,此时所需pH的范围为_________,当调节溶液pH=5时,溶液中的c(Fe3+)=__________;
(4)反应3的离子方程式为__________,反应类型为__________;
(5)从滤液B中可回收的主要物质是__________;
(6)经检验分析,反应4 所得固体组成为Zna(OH)bCO3,称取该固体22.4g,焙烧后得固体16.2g,则a=_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】电解硫酸钠溶液生产硫酸和烧碱的装置如图所示,其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为1∶2,下列有关说法正确的是

(说明:阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)
A. a电极反应式为2H++2e-===H2↑
B. 产物丙为硫酸
C. d为阴离子交换膜
D. Na2SO4溶液浓度增大
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F、G七种短周期元素,原子序数依次增大。由A、B形成的单质在一定条件下可生成气体X且X的水溶液呈碱性;D原子K层电子数是其M层电子数的2倍;E的简单阳离子与X具有相同电子数,且E的简单阳离子是同周期中简单离子半径最小的元素;F元素的原子最外层比次外层少两个电子,C和G的最外层电子数之和为13 。则
(1)C在周期表中的位置为 _________________ ;
(2)写出:D在C单质中燃烧所生成淡黄色的固体的电子式_______________
(3)A、B、D、E四种元素的原子,半径由大到小的顺序为________________。(用元素符号表示 )
(4)G的单质在反应中常作氧化剂,该单质的水溶液与F的低价氧化物反应的化学方程式为______________________。
(5)写出由A、C、D、F这四种元素共同组成的2种化合物在水溶液中发生反应的离子方程式:__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,试预测实验结果: _______与盐酸反应最快。
Ⅱ.利用下图装置可以验证非金属性的变化规律。

(2)仪器A的名称为________,干燥管D的作用是____________________________。
(3)若要证明非金属性:S>C>Si,则A中加 ____________、B中加NaHCO3溶液、C中加___________,观察到C中溶液的现象为________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】液化石油气作为燃料,已普遍进入城市家庭,它是含有下列物质的混合物,在常压下,这些物质的沸点如下表所示:
物质名称 | 乙烷 | 丙烷 | 丁烷 | 戊烷 | 己烷 |
沸点/℃ | -88.6 | -42.1 | -0.5 | 36.1 | 69.2 |
在常温下使用至无气体放出时,钢瓶中常剩余一些液态物质,这些物质最有可能是( )
A. 乙烷、丙烷和丁烷 B. 乙烷和丙烷
C. 只有乙烷 D. 戊烷和己烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com