
科目: 来源: 题型:
【题目】氯化铁溶液与氢氧化铁胶体具有的共同性质是
A.都能产生丁达尔效应 B.有相同的颜色
C.分散质颗粒直径都在1-100nm之间 D.加入浓氢氧化钠溶液都产生红褐色沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,下列离子组在给定条件下一定能大量共存的是
A. pH=1的溶液中:K+、Na+、NO3-、CH3COO-
B. Na2S溶液中:K+、Na+、NO3-、Ag+
C. KCl溶液中:Na+、Fe3+、SO42-、SCN-
D. c(OH-)=1×10-13mol·L-1的溶液中:K+、Mg2+、Cl-、NO3-
查看答案和解析>>
科目: 来源: 题型:
【题目】鉴别两种溶液食盐水和蔗糖水的方法有
①在两种溶液中分别加入少量稀硫酸,加热,再加入碱中和硫酸,再加入银氨溶液,微热;②测量溶液的导电性;③将溶液与溴水混合、振荡;④用舌头尝味道。
其中在实验室进行鉴别的正确方法是
A. ①② B. ①③ C. ②③ D. ③④
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关化学计量的叙述,正确的是( )
A.H2SO4的摩尔质量为98g
B.1molH2SO4的质量为98g/mol
C.标准状况下2molO2的体积约为44.8L
D.室温常压下气体摩尔体积约为22.4L/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z是一种短周期元索,原子半径的大小为:r(Y)>r(X)>r(Z),三种元素的原子序数之和为15;X、Y、Z三种元素的常见单质在适当条件下可发生右下图转化关系.其中R为10电子分子,是一种常见的无机溶剂。下列说法中不正确的是
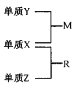
A. X元素位于周期表中第16列
B. X、Y、Z元素两两之间均能形成原子个数比为l:1的化合物
C. X、Y、Z元素形成的单质均具有强还原性
D. R的沸点高于M的沸点
查看答案和解析>>
科目: 来源: 题型:
【题目】用萃取剂将溴水中的溴萃取出来,这种萃取剂应具备的性质是( )
A.难溶于水,且必须比水的密度大
B.难溶于水,且比水溶解溴的能力强
C.易溶于水,且比水溶解溴的能力弱
D.难溶于水,且必须与溴单质发生化学反应
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向20.00 mL 0.1000 mol·L-1 CH3COONa 溶液中逐滴加入 0.100 0 mol L-1盐酸,溶液的pH与所加盐酸体积的关系如下图所示(不考虑挥发)。下列说法正确的是
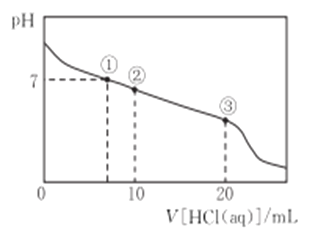
A. CH3COONa溶液中:c(H+) +c(CH3COOH)=c(OH-)+c(Na+)
B. 点①所示溶液中:c(CH3COOH) =c(Cl-)>c(OH-)=c(H+)
C. 点②所示溶液中:c(Cl-)>c(CH3COO-)>c(CH3COOH)>c(H+) >c(OH-)
D. 点③所示溶液中:c(Na+)= c(Cl-)>c(CH3COOH) >c(H+)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2做原料的燃料电池,负极材料采用Pt/C.正极材料采用MnO2,可用做空军通信卫星电源,其工作原理如图所示。下列说法中不正确的是
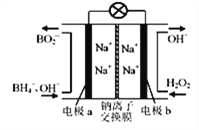
A. 电池放电时Na+从a极区移向b极区
B. 燃料电池是一类能量转化效率高、环境友好的发电装置
C. 该电池的负极反应为BH4-+ 8OH-一8e-═BO2-+ 6H2O
D. 在电池反应中,每消耗3molH2O2,转移电子数为3NA
查看答案和解析>>
科目: 来源: 题型:
【题目】铜及其化合物在工农业生产及日常生活中应用非常广泛。回答下列问题:
(1)纳米级Cu2O由于具有优良的催化性能而受到关注,制取Cu2O的两种方法如下表所示。
方法I | 用炭粉在高温条件下还原CuO生成Cu2O和CO2 |
方法II | 用肼(N2H4)还原新制Cu(OH)2 |
① 方法I中还原剂与氧化剂的物质的量之比为________。
② 方法II发生反应的化学方程式为______________。
(2)氢化亚铜是一种红色同体,可由下列反应制备:
4CuSO4+3H3PO2+6H2O=4CuH↓+4H2SO4+3H3PO4
该反应中每转移3 mol电子,生成CuH的物质的量为___________mol。
(3)氯化铜溶液中各种含铜微粒的分布分数(平衡时某微粒的浓度占各微粒浓度之和的分数)与c(C1-)之间的关系如图所示。

① 当c(C1-)= 9 mol/L时,溶液中3种主要含铜微粒浓度的大小关系为__________。
② 在c(C1-)= l mol /L的氯化铜溶液中,加人AgNO3溶液,CuCl+转化为Cu2+的离子方程式为____________。
(4)已知:Cu(OH)2是二元弱碱,25℃时Ksp[Cu(OH)2]=2.0×10-20。则此温度下在铜盐溶液中Cu2+发生水解反应的平衡常数为______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,用浓度均为0.1mol·L-1的Na0H 溶液和盐酸分别滴定体积均为20mL、浓度均为0.1mol·L-1的HA溶液与BOH溶液。滴定过程中溶液的pH随滴加溶液的体积变化关系如图所示。下列说法中正确的是

A. HA为弱酸,BOH为强碱
B. a点时,溶液中粒子浓度存在关系:c(B+)>c(Cl-)>c(OH-)>c(BOH)
C. b点时两种协液中水的电离程度相同.且V=20
D. c、d两点溶液混合后微粒之间存在关系:c(H+)= c(OH-)+c(BOH)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com