
科目: 来源: 题型:
【题目】亚硝酸钠是一种工业盐,外观与食盐非常相似,毒性较强。某化学兴趣小组对食盐与亚硝酸钠进行探究:
Ⅰ. 鉴别NaCl和NaNO2
甲同学用沉淀分析法
经查:常温下Ksp(AgNO2)=2×10-8,Ksp(AgCl)=1.8×10-10.分别向盛有5mL0.0001mol/L两种盐溶液的试管中同时逐滴滴加0.0001mol/L硝酸银溶液,先生成沉淀的是装有_____________溶液的试管。
乙同学测定溶液pH
用pH试纸分别测定0.1mol/L两种盐溶液的pH,测得NaNO2溶液呈碱性。该溶液呈碱性的原因是__________(用离子方程式解释)。
Ⅱ. 如图是在实验室进行二氧化硫制备与性质实验的组合装置,部分固定装置未画出。
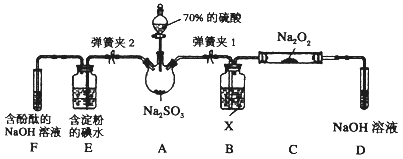
(1)装置B中试剂X是_______,装置D中盛放NaOH溶液的作用是_______________________。
(2)关闭弹簧夹2,打开弹簧夹1,注入硫酸至浸没三颈烧瓶中固体,检验SO2与Na2O2反应是否有氧气生成的方法是_____________________________________。
(3)关闭弹簧夹1后,打开弹簧夹2,残余气体进入E、F中,能说明I-还原性弱于SO2的现象为______________;发生反应的离子方程式是_____________________。
Ⅲ. 用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入右图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能:
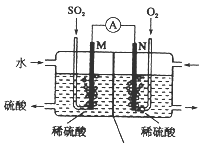
(1)M极发生的电极反应式为____________________________。
(2)若使该装置的电流强度达到2.0 A,理论上每分钟应向负极通入标准状况下气体的体积为_____L(已知:1个e所带电量为1.6×10-19C)。(保留两位有效数字)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:A、D、E、H的焰色反应均呈黄色;G能使带火星的木条复燃;溶 液B中加入AgN03溶液产生浅黄色沉淀;溶液H中加AgN03溶液产生白色沉淀。在一定条件下,各物质可发生如下图所示的变化:
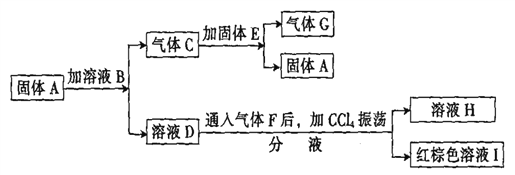
(1)写出A、B的化学式:A __________、 B _________。
(2)写出C和E反应的化学方程式:_________。
(3)写出F通人D溶液反应的离子方程式:_________。
(4)溶液H中加AgN03溶液反应的离子方程式为:_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,下列有关电解质溶液的说法正确的是( )
A. 将Na2CO3溶液用水稀释后,pH变大,Kw不变
B. 向有AgCl固体的饱和溶液中加少许水,c(Ag+)和Ksp(AgCl)都不变
C. pH=4.75浓度均为0.1mol/L的CH3COOH、CH3COONa的混合溶液中:c(CH3COO-)+c(OH-)
<c(H+)+c(CH3COOH)
D. 分别用pH=2和pH=3 的 CH3COOH溶液中和等物质的量的NaOH,消耗CH3COOH溶液的体积分别为Va和Vb,则10Va=Vb
查看答案和解析>>
科目: 来源: 题型:
【题目】根据我省中心气象台报道,近年每到春季,我省很多城市多次出现大雾天气。根据物质的分类,雾属于下列分散系中的
A. 胶体 B. 悬浊液 C. 乳浊液 D. 溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)接触法制硫酸工艺中,其主反应是在恒容、温度为450℃并有催化剂存在的条件下进行:
2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-190Kj/mol
2SO3(g) ΔH=-190Kj/mol
①下列描述中能说明上述反应已达平衡的是____________。
a. ![]() (O2)正=2
(O2)正=2![]() (SO3)逆 b.容器中气体的密度不随时间而变化
(SO3)逆 b.容器中气体的密度不随时间而变化
c.容器中气体的平均相对分子质量不随时间而变化 d.容器中气体的分子总数不随时间而变化
②在一个固定容积为5L的密闭容器中充入0.20molSO2和0.10molO2,半分钟后达到平衡,测得容器中含SO30.18mol,则![]() (O2)=__________mol·L-1·min-1,若继续通入0.40 mol SO2和0.20molO2则平
(O2)=__________mol·L-1·min-1,若继续通入0.40 mol SO2和0.20molO2则平
衡______移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,________mol3) <_____mol。
(2)工业生成尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为2NH3 (g)+ CO2(g) ![]() CO(NH2)2(1)+H2O(1),该反应的平衡常数和温度关系如下:
CO(NH2)2(1)+H2O(1),该反应的平衡常数和温度关系如下:
T/℃ | 165 | 175 | 185 | 195 |
K | 111.9 | 74.1 | 50.6 | 34.8 |
①ΔH_______0(填“>”、“<”或“=”)
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)![]() =x,下图是氨碳比(x)与CO2平衡转化率(α)的关系,α随着x增大而增大的原因是___________。
=x,下图是氨碳比(x)与CO2平衡转化率(α)的关系,α随着x增大而增大的原因是___________。

③右图中的B点对应的NH3的平衡转化率为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 乙二醇和丙三醇互为同系物
B. 甲烷、乙烯和苯在工业上都可通过石油分馏得到
C. 可通过酸性高锰酸钾溶液来区别烯烃和炔烃
D. 苯酚对皮肤有腐蚀性,如果不慎粘到手上,应该立即用酒精清洗
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)工业上可利用CO2和H2生成甲醇,热化学方程式如下:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=Q1kJ·mol-1
CH3OH(g)+H2O(g) △H=Q1kJ·mol-1
又查资料得知:①CH3OH(l)+1/2O2(g)![]() CO2(g)+H2(g) △H=Q2kJ·mol-1
CO2(g)+H2(g) △H=Q2kJ·mol-1
②H2O(g)= H2O(I) △H=Q3kJ·mol-1
则表示甲醇的燃烧热的热化学方程式为________________。
某同学设计了一个甲醇燃料电池,并用该电池电解200mL一定浓度的NaCl与CuSO4混合溶液,其装置如图:
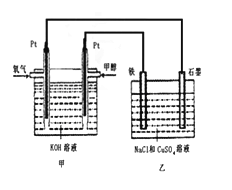
(2)写出甲中通入甲醇这一极的电极反应式_______________________。
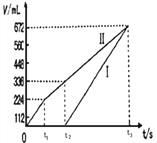
(3)理论上乙中两极所得气体的体积随时间变化的关系如图所示(已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式___________,原混合溶液中NaCl的物质的量浓度为_______mol/L。(设溶液体积不变)
(4)当向上述甲装置中通入标况下的氧气336mL时,理论上在铁电极上可析出铜的质量为_________g。
(5)已知草酸H2C2O4为弱酸。
①常温下,下列事实能说明草酸是弱电解质的是____________。
A.向草酸钠溶液加酚酞,溶液变红
B.取一定量草酸溶液加水稀释至10倍,PH变化小于1
C.草酸能使酸性KMnO4溶液褪色
D.取相同PH的草酸溶液和盐酸,分别加入足量的大小、形状相同的镁条,草酸溶液反应速度快
②常温下,0.1mol·L-1的草酸溶液与pH=13的NaOH溶液等体积混合,所得溶液的pH为6,则c(HC2O4-)+2c(C2O42-)=________________。(用准确的数学表达式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com