
科目: 来源: 题型:
【题目】化学与生产、生活密切相关,下列有关说法正确的是
A. 淀粉与纤维素互为同分异构体
B. 煤的气化、液化与石油的裂化、裂解均为化学变化
C. 被称为“黑金”的新型纳米材料石墨烯属于有机化合物
D. 糖类、油脂和蛋白质都属于营养物质,都能发生水解反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子在溶液中能大量共存的是
A. Ba2+、 HCO3-、 OH—、 K+ B. Fe2+、 H +、 MnO4—、 SO42-
C. Fe3+、 Na+、 SO42-、 SCN— D. H+、 SO42-、 Cl—、 K+
查看答案和解析>>
科目: 来源: 题型:
【题目】(15分)重铬酸钠在制革工业、印刷工业、电镀工业等有重要用途,铬铁矿的主要成分可表示为FeOCr2O3,还含有Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钠(Na2Cr2O7)的流程图:

(1)煅烧前应将铬铁矿充分粉碎,其目的是_________。灼烧是中学化学中常用的操作方法,如在实验室中将铬铁矿和碳酸钠固体混合物灼烧,以下各实验仪器中不需要的是_____。
a.陶瓷坩埚 b.铁坩埚 c.三脚架 d.泥三角
(2)转窑中发生的主要反应为:
①Na2CO3+Al2O3![]() 2NaAlO2+CO2↑;
2NaAlO2+CO2↑;
②__FeOCr2O3+__Na2CO3+__O2![]() __Na2CrO4+__Fe2O3+__ 。
__Na2CrO4+__Fe2O3+__ 。
请配平反应②的化学方程式。
(3)生成固体Y的离子方程式为_______________。
(4)向母液中加入浓硫酸,把铬酸钠转化为重铬酸钠,经两次蒸发,主要是除去___(填化学式),冷却至30~40℃得到产品晶体。洗涤该晶体的溶剂最好是__________(填序号)。
a.蒸馏水 b.无水乙醇 c.75%乙醇溶液
(5)为了测定实验制得的产品中Na2Cr2O7的含量,称取样品0.140g置于锥形瓶中,加50mL水;再加入2gKI(过量)及稍过量的稀硫酸溶液,摇匀,暗处放置10min;然后加150mL蒸馏水并加入3mL 0.5%淀粉溶液;用0.1000mol/L Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液30.00mL。(假定杂质不参加反应,已知:Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,I2+2S2O32-=2I-+S4O62-)
①终点实验现象是________。
②该产品中Na2Cr2O7的纯度为____ 。(以质量分数表示)
③若滴定管在滴定前俯视读数,滴定结束后仰视读数,测得样品的纯度将 (填“偏高”、或“偏低”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】铝热反应是铝的一个重要性质。


(1)按如图装置进行实验,可观察到反应剧烈,火星四射,漏斗下方有红热熔融物“铁块”流出。
该反应的化学方程式为_____,其能量变化为如图中的______(填“A”或“B”)所示。

(2)某校化学兴趣小组同学,为了测定铝热反应后得到“铁块”混合物中铝的含量。取“铁块”样品研碎称得质量为x g,加入如图装置,再滴入足量NaOH溶液充分反应,测量生成气体体积为a ml(标况)。
①仪器A的名称为_______。
②写出样品中Al与NaOH反应的化学方程式_______。
③该小组同学改进实验,用恒压漏斗(如图)代替仪器A,其优点有________(写2点)。
④该样品中铝的含量为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为元素周期表的一部分。

利用表中元素回答下列问题:
(1)X元素在周期表中的位置为__________。
(2)气态氢化物水溶液呈碱性的元素是_____________,此氢化物的电子式__________。
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是__________。
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1mol硫得电子多
c.Y和硫两元素的简单氢化物受热分解,前者的分解温度高
(4)![]() 和
和![]() 是元素R的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为w g,则
是元素R的两种稳定的天然同位素,它们的原子质量分别为a g和b g,在自然界中所占的原子百分比分别为m%和n%,已知12C原子的质量为w g,则![]() 的相对原子质量的表达式为___________,元素R的相对原子质量的表达式为___________________。
的相对原子质量的表达式为___________,元素R的相对原子质量的表达式为___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有以下几种有机物:
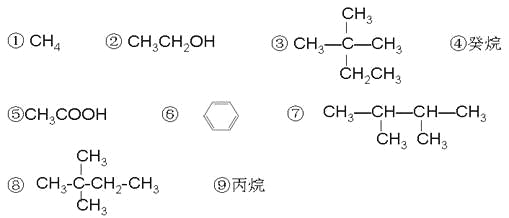
请利用上述给出的物质按要求回答下列问题:
(1)相对分子质量为44的烷烃的结构简式为 ;
(2)分子中含有14个氢原子的烷烃的分子式是 ;
(3)与③互为同分异构体的是 (填序号);
(4)具有特殊气味,常作萃取剂的有机物在铁作催化剂的条件下与液溴发生一取代反应的化学方程式 ;
(5)用“>”表示①③④⑨熔沸点高低顺序: (填序号);
(6)有机物②在加热条件下和CuO反应的化学方程式 ;
(7)在120℃,1.01×105Pa条件下,某种气态烃与足量的O2完全反应后,测得反应前后气体的体积没有发生改变,则该烃是 (填序号);它与⑧互为 关系;
(8)有机物⑤和②在一定条件下发生反应的化学方程式是 ;
查看答案和解析>>
科目: 来源: 题型:
【题目】为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是
选项 | 混合物 | 除杂试剂 | 分离方法 |
A | 己烷(己烯) | 溴的CCl4溶液 | 分液 |
B | 溴乙烷(乙醇) | 水 | 分液 |
C | 淀粉溶液(NaCl) | 水 | 过滤 |
D | 皂化液(甘油) | NaCl | 盐析,分液 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】分子式为C4H8O2的有机物能与金属钠反应放出氢气,且与新制氢氧化铜反应生成砖红色沉淀,符合条件的有机物有(不含立体异构)
A. 4种 B. 5种 C. 6种 D. 7种
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.常温常压下,断裂1mol(理想)气体分子化学键所吸收的能量或形成1mol(理想)气体分子化学键所放出的能量称为键能(单位为KJ.mol-1)下表是一些键能数据(KJ·mol-1)
化学键 | 键能 | 化学键 | 键能 | 化学键 | 键能 |
C-F | 427 | C-Cl | 330 | C-I | 218 |
H-H | 436 | S=S | 255 | H-S | 339 |
回答下列问题:
写出H2(g)与S2(g)反应生成H2S(g)的热化学方程式____________________________。
Ⅱ.某温度时,在2 L密闭容器中,三种气态物质X、Y、Z的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析可得:

(1)该反应的化学方程式为___________________。
(2)反应开始至2 min,用Y表示的平均反应速率为_____________,X的转化率为_________。
(3)在一定温度下,下列情况可作为上述反应达到反应限度的标志的是________。
A.X、Y、Z的浓度相等
B.X、Y、Z的分子数比为3︰1︰2
C.Z的生成速率是Y的生成速率的二倍
D.单位时间内生成n mol Y,同时生成3n mol X
Ⅲ.如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是________(填“a”或“b”)电极,该极的电极反应式为: ________________。
②电池工作一段时间后电解质溶液的pH__________(填“增大”“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com