
科目: 来源: 题型:
【题目】已知一个碳原子上连有两个羟基时,易发生下列转化:![]() 。请根据下图回答:
。请根据下图回答:
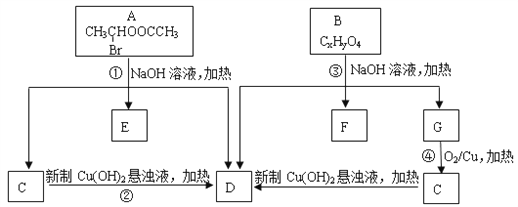
(1)A中所含官能团的名称为________________。
(2)质谱分析发现B的相对分子质量为208;红外光谱显示B分子中含有苯环结构和两个酯基;核磁共振氢谱中有五个吸收峰,其峰值比为2︰2︰2︰3︰3,其中苯环上的一氯代物只有两种。则B的结构简式为___________________。
(3)写出下列反应方程式:
①____________________________;
④_____________________________。
(4)符合下列条件的B的同分异构体共有________________种。
①属于芳香族化合物;
②含有三个取代基,其中只有一个烃基,另两个取代基相同且处于相间的位置;③能发生水解反应和银镜反应。
查看答案和解析>>
科目: 来源: 题型:
【题目】a、b、c、d、e、f是H、C、N、Na、Si、Cu六种元素中的其中一种,已知:图1表示的是这六种元素单质的熔点高低顺序,其中c、d均是热和电的良导体,f形成的某种单质硬度最大。

回答下列问题:
(1)a、b、f三种元素的电负性从小到大的顺序为______(用元素符号表示)。
(2)元素b的单质的一个分子中含有____个σ键和______个π键。
(3)元素c的单质的晶体堆积方式类型是_______;若c单质分别与氟气和氯气形成化合物甲和乙,则甲的晶格能______乙的晶格能(填“>”、“<”或“=”)。
(4)元素d的单质基态原子的价电子排布式为______(用NA表示阿伏加德罗常数的值)。
(5)元素e和f可形成化合物丙(丙的晶胞结构如图2所示),则丙的化学式为_____;丙的晶体类型为_______,在丙中,每个e原子周围最近的e原子数目为______,若晶胞的边长为a pm,则丙的密度为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2的转换在生产、生活中具有重要的应用。
(1)CO2的低碳转型对抵御气候变化具有重要意义,海洋是地球上碳元素最大的“吸收池”。

①溶于海水中的CO2主要以四种无机碳形式存在,除CO2、H2CO3两种分子外,还有两种离子的化学式为_________、___________________。
②在海洋碳循环中,可通过上图所示的途径固碳。写出钙化作用的离子方程式:____________。
(2)将CO2与金属钠组合设计成Na-CO2电池,很容易实现可逆的充、放电反应,该电池反应为4Na+3CO2 ![]() 2Na2CO3+C。放电时,在正极得电子的物质为___________;充电时,阳极的反应式为___________。
2Na2CO3+C。放电时,在正极得电子的物质为___________;充电时,阳极的反应式为___________。
(3)目前工业上有一种方法是用CO2和H2在230℃并有催化剂条件下转化生成甲醇蒸汽和水蒸气。下图表示恒压容器中0.5molCO2和1.5 mol H2转化率达80%时的能量变化示意图。能判断该反应达到化学平衡状态的依据_______(填字母)。

a.容器中压强不变 b.H2的体积分数不变
c.c(H2 =3c(CH3OH) d.容器中密度不变
e.2个C = O断裂的同时有6个H - H断裂
(4)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)![]() CO2(g) +H2(g),得到如下三组数据:
CO2(g) +H2(g),得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
3 | 900 | a | b | c | d | t |
①实验2条件下平衡常数K=____________。
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b的值_________(填具体值或取值范围)。
③实验4,若900℃时,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时v(正____v(逆)(填“ <”、“ >”或“=")。
(5)已知在常温常压下:
①2CH3OH(I)+3O2(g)=2CO2(g)+4H2O(g) △H=-1275.6kJmol-1
②2CO(g)+O2(g)=2CO2(g) △H=-566.0kJ·mol-1
③H2O(g)=H2O(I) △H=-44.0kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是
A.大力实施矿物燃料“脱硫、脱硝”技术,可减少酸雨的发生
B.SiO2 具有较高的熔点,可用于制成耐高温的坩埚对氢氧化钠固体加热
C.节日燃放的烟花,是钠、钾、锶、铂、铁等金属化合物焰色反应所呈现的色彩
D.CO、NO、NO2都是大气污染气体,在空气中都能稳定存在
查看答案和解析>>
科目: 来源: 题型:
【题目】Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定,在酸性环境下易分解生成S和SO2。某小组设计了如下实验装置制备Na2S2O3(夹持及加热仪器略),总反应为2Na2S+Na2CO3+4SO2 ![]() 3Na2S2O3+CO2。回答下列问题:
3Na2S2O3+CO2。回答下列问题:

(1)装置A的作用是制备______________,反应的化学方程式为______________。
(2)完成下表实验过程:
操作步骤 | 装置C的实验现象 | 解释原因 |
检查装置气密性后,添加药品 | pH计读数约为13 | 用离子方程式表示(以S2-为例): ① |
打开K2,关闭K3,调节K1使硫酸缓慢匀速滴下 | ⅰ.导管口有气泡冒出, ② ⅱ.pH计读数逐渐 ③ | 反应分步进行: Na2CO3+SO2 2Na2S+3SO2 Na2SO3+S |
当pH计读数接近7时,立即停止通SO2,操作是 ④ | 必须立即停止通SO2的原因是: ⑤ |
(3)Na2S2O3有还原性,可作脱氯剂。向Na2S2O3溶液中通入少量Cl2,某同学预测S2O32-转变为SO42-,设计实验验证该预测:取少量反应后的溶液于试管中,______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】1.76克铜镁合金完全溶解于50mL密度为1.40g/cm3质量分数为63%的浓硝酸中,得到NO2 气体1792mL (标准状况),向反应后的溶液中加入适量的1.0mol/LNaOH溶液,恰使溶液中的金属离子全部沉淀下列说法不正确的是( )
A. 该浓硝酸中HNO3的物质的量浓度是14.0mol/L
B. 加入NaOH溶液的体积是50mL
C. 浓硝酸在与合金反应中起了酸性和氧化性的双重作用
D. 得到的金属氢氧化物的沉淀为3.12克
查看答案和解析>>
科目: 来源: 题型:
【题目】镁铝合金质优体轻,又不易锈蚀,被大量用于航空工业、造船工业、日用化工等领域。下列关于镁铝合金性质的叙述中,正确的是
A. 此合金的熔点比镁和铝的熔点都高
B. 此合金能全部溶解于稀盐酸中
C. 此合金能全部溶解于氢氧化钠溶液中
D. 此合金的硬度比镁和铝的硬度都小
查看答案和解析>>
科目: 来源: 题型:
【题目】碱性电池有容量大,放电电流大的特点,被广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn + 2MnO2 + H2O=Zn(OH)2 + Mn2O3。下列说法错误的是
A. 电池工作时,锌失去电子
B. 电池正极的电极反应式为2 MnO2 + H2O +2e-== Mn2O3 + 2OH-
C. 电池工作时,电子由负极通过外电路流向正极
D. 外电路中每通过0.2mol电子,锌的质量理论上减少13g
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、R、M是原子序数依次增大的五种元素,基态X原子的s电子数比P电子数多3个,Y、Z均位于第二周期且两元素原子的最外层电子数之和为11,Z、R同主族,M核外电子有26种运动状态,请回答下列问题:
(1)元素M的基态原子的核外电子排布式为_________________。
(2)第一电离能:Y_____(填“ > ”或“<”)Z。
(3)化合物XCl3中心原子的杂化轨道类型为________;RC12的立体构型为_______。
(4)H2Z、H2R的沸点分別为100℃、-60.4℃,试解释其原因:_____________________________。
(5)R、M形成的一种化合物晶胞如图所示。

①该化合物的化学式为_____________。
②若晶胞参数为a pm。列式计算该晶胞的密度ρ=______g·㎝-3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com