
科目: 来源: 题型:
【题目】铁屑和氯气在500~600 ℃ 下可制取无水FeCl3 ,实验装置如下图。下列说法正确的是( )

A. 分液漏斗中盛放的试剂是稀盐酸
B. 实验时应先点燃I 中酒精灯,再点燃Ⅲ中酒精灯
C. 洗气瓶中盛放的试剂是饱和食盐水
D. 烧杯中盛放的试剂是澄清石灰水,目的是吸收尾气
查看答案和解析>>
科目: 来源: 题型:
【题目】下列溶液与100 mL 0.5 mol·L-1 NaCl溶液中所含Cl-的物质的量浓度相同的是( )
A. 100 mL0.5molL-1 MgCl2溶液 B. 200 mL0.25molL-1 AlCl3溶液
C. 50mL1molL-1 NaCl溶液 D. 25mL 0.5molL-1 HCl溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】金属晶体的堆积密度大,原子配位数高,能充分利用空间的原因是( )
A. 金属原子的价电子数少
B. 金属晶体中有自由电子
C. 金属原子的原子半径大
D. 金属键没有饱和性和方向性
查看答案和解析>>
科目: 来源: 题型:
【题目】[化学——选修5:有机化学基础]乙基香兰素是最重要的合成香料之一,常作为婴幼儿奶粉的添加剂。制备乙基香兰素的一种合成路线(部分反应条件略去)如下图所示:

已知:① R—ONa + R’—Br —→ R—O—R’ + NaBr
② Ⅲ中生成的Cu2O经氧化后可以循环利用
回答下列问题:
(1)A的核磁共振氢谱有3组峰。A的结构简式为 。
(2)Ⅰ中可能生成的一种烃是 (填名称);催化剂PEG可看作乙二醇脱水缩聚的产物,PEG的结构简式为 。若PEG的平均相对分子质量为17618,则其平均聚合度约为 。
(3)Ⅱ中,发生的反应属于 (填反应类型)。
(4)Ⅲ中,反应的化学方程式为 。
(5)Ⅳ中,有机物脱去的官能团是 (填名称)。
(6)D是乙基香兰素的同分异构体,其分子结构中不含乙基。由A制备D的一种合成路线(中间产物及部分反应条件略去)如下图所示:
C和D的结构简式分别为 、 。
查看答案和解析>>
科目: 来源: 题型:
【题目】电讯器材元件材料MnCO3在空气中加热易转化为不同价态锰的氧化物,其固体残留率随温度变化如下图。下列说法不正确的是( )
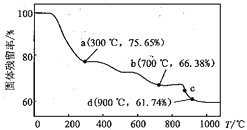
A. a 点剩余固体中n(Mn) : n(O) = 1 : 2
B. b 点对应固体的成分为Mn3O4
C. c 点发生的反应为2MnO2 △ 2MnO+O2↑
D. d 点对应固体的成分为MnO
查看答案和解析>>
科目: 来源: 题型:
【题目】已知链烃A 的分子式为C6Hx,它与足量的溴水反应生成C6HxBr2,该生成物中含有两个甲基,则满足上述条件(不考虑立体异构)的链烃A的结构有
A. 5种 B. 6种 C. 7种 D. 9种
查看答案和解析>>
科目: 来源: 题型:
【题目】乙酸正丁酯是医药合成的重要中间体,某同学在实验室中用乙酸和正丁醇来制取,实验操作如下:
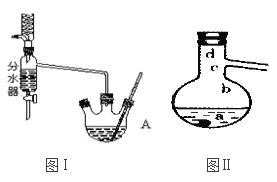
Ⅰ.将混合液(18.5 mL正丁醇和13.4 mL乙酸(过量),0.4 mL浓硫酸)置于仪器A中并放入适量沸石(见图I,沸石及加热装置等略去),然后加热回流约20分钟。
Ⅱ.将反应后的溶液进行如下处理:①用水洗涤,②用试剂X干燥,③用10% Na2CO3溶液洗涤。
Ⅲ.将所得到的乙酸正丁酯粗品转入蒸馏烧瓶中进行蒸馏,最后得到17.1 g乙酸正丁酯。
部分实验数据如下表所示:
化合物 | 相对分子质量 | 密度/(g·mL-1) | 沸点/℃ | 溶解度(g)/(100 g水) |
正丁醇 | 74 | 0.80 | 118.0 | 9 |
乙酸 | 60 | 1.045 | 118.1 | 互溶 |
乙酸正丁酯 | 1 1 6 | 0.882 | 126.1 | 0.7 |
(1)仪器A的名称是_________,使用分水器(实验中可分离出水)能提高酯的产率,其原因是______________________.
(2)步骤Ⅱ中的操作顺序为____________(填序号),用Na2CO3溶液洗涤的目的是____________,试剂X不能选用下列物质中的______________(填字母序号)。
a.无水硫酸镁 b.新制生石灰 c.无水硫酸钠
(3)步骤Ⅲ(部分装置如图Ⅱ所示)。
①蒸馏过程中需要使用_________形冷凝管,当仪器连接好后,a.向相应的冷凝管中通冷凝水;b.加热蒸馏烧瓶的先后顺序是___________。(填“先a后b"或“先b后a”)
②温度计水银球所处的位置不同,会影响馏出物的组成,当温度计水银球分别位于图Ⅱ中的________(填“a”“b”“c”或“d”)点时会导致收集到的产品中混有较多的低沸点杂质。
(4)该实验乙酸正丁酯的产率是_____________。(计算结果保留2位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
【题目】Al(NO3)3 常用于![]() 的萃取。测量Al(NO3)3 纯度的实验步骤如下图所示。下列说法正确的是( )
的萃取。测量Al(NO3)3 纯度的实验步骤如下图所示。下列说法正确的是( )

A. 配置Al(NO3)3 溶液需要的玻璃仪器只有250 mL容量瓶,玻璃棒
B. 加入试剂a发生反应的离子方程式为Al3++3OH—=Al(OH)3↓
C. 操作“b ”需要在蒸发皿中进行
D. Al(OH)3的纯度为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】如表是元素周期表的一部分,参照元素在表中的位置,请用化学用语回答下列问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
4 |
(1)这些元素中,化学性质最不活泼原子的原子结构示意图为__________;气态氢化物中,最稳定的是___________;最高价氧化物对应水化物中,酸性最强的是______________。
(2)①和④两种元素的原子按1:1组成的常见化合物的电子式为___________________。
(3)②、③的单质中更容易与①的单质反应的是___________________(用化学式表示)。
(4)④、⑦、⑧、⑨的简单离子半径由大到小的顺序为___________________ (用离子符号和“>”表示)。
(5)⑥和⑧的最高价氧化物对应水化物之间发生反应的离子方程式____________________。
(6)⑤⑨三种元素的单质沸点由高到低的顺序是________________(用化学式和“>”表示)。
(7)⑦⑧两元素相比较,金属性较强的是_____________ (填名称),可以验证该结论的实验是____________________(填字母)。
A.将在空气中放置已久的这两种元素的块状单质分别放入热水中
B.将形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应
C.将形状、大小相同这两种元素的单质分别和热水作用,并滴入酚酞溶液
D.比较这两种元素的气态氢化物的稳定性
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关含硅物质的说法正确的是
A. 二氧化碳通入水玻璃可以制得硅酸 B. 二氧化硅可以用作太阳能光电池板
C. 高纯度的硅单质广泛用于制作光导纤维 D. 二氧化硅是酸性氧化物,它不溶于任何酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com