
科目: 来源: 题型:
【题目】熔触的金属锡在300℃左右能直接与氯气作用生成四氯化锡。四氯化锡的熔点-33℃,沸点114℃,遇潮湿空气水解。某学习小组用以下装置制取少量四氯化锡。回答下列问题:
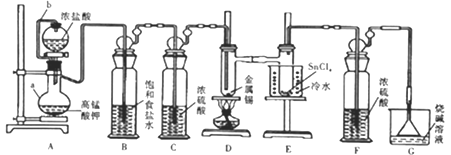
(1)仪器组装完毕,为检查装置的气密性,将装置G中漏斗改为导管且管口浸没于水中,后续操作是__________,说明气密性良好。
(2)仪器a的名称是__________;设计连接管b的目的是_______________。
(3)装置B、F的作用分別是______________、____________。
(4)装置A中反应的离子方程式为______________,排尽装置中的空气后才能点燃D处的酒精灯,判断装置中的空气已排尽的现象是_____________;D中加热的作用之一是加快氯气与金属锡反应,另一作用是__________。
(5)四氯化锡遇潮湿空气时有白色烟雾产生,同时生成白色固体(SnO2·xH2O),该反应的化学方程式为_____________。
(6)实验结束后,若制得SnCl4的质量为2.61g,Cl2的转化率为80%,则消耗KmnO4的质量为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有几种有机物之间的转化关系如图所示(部分产物和条件省略),已知A为氯代醇。

请根据上述信息,回答下列问题:
(1)A的结构简式 _________________________ ,G的结构简式 _______________________ ,
H中官能团的电子式 ____________________ 。
(2)上述流程中,有机反应类型相同的是 ________ 。
A.①② B.③④ C.⑤⑨ D.⑦⑧
(3)下列有关E的说法正确的是 ________ 。
A.E属于二元醇
B.E能与钠反应产生气体
C.E能使溴的四氯化碳溶液褪色
D.E能发生银镜反应
(4)I有多种同分异构体,写出同时满足下列条件的I的所有同分异构体的结构简式: ____________________________________________________________ 。
①能水解且能与新制氢氧化铜反应生成砖红色固体; ②能与钠反应放出气体。
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸是植物(特别是草本植物)常具有的成分,具有广泛的用途。草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数K1=5.4×10-2,K2=5.4×10-5。回答下列问题:
(1)拟用下列装置分解草酸制备少量纯净的CO,其合理的连接顺序为___________(填字母序号)。
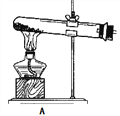

![]()

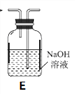
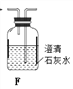
(2)相同温度条件下,分别用3支试管按下列要求完成实验:
试管 | A | B | C |
加入试剂 | 4mL 0.01mol/L KMnO4 1ml 0.1moL/L H2SO4 2mL 0.1mol/L H2C2O4 | 4mL 0.02mol/L KMnO4 1ml 0.1moL/L H2SO4 2mL 0.1mol/L H2C2O4 | 4mL 0.03mol/L KMnO4 1ml 0.1moL/L H2SO4 2mL 0.1mol/L H2C2O4 |
褪色时间 | 28秒 | 30秒 | 不褪色 |
写出试管B的离子方程式_____________________________________;上述实验能否说明“相同条件下,反应物浓度越大,反应速率越快”?____________(选填“能”或“不能”);简述你的理由:__________________________________。
(3)设计实验证明草酸为弱酸的方案及其现象均正确的有_____________(填序号)。
A.室温下,取0.010mol/L的H2C2O4溶液,测其pH=2;
B.室温下,取0.010mol/L的NaHC2O4溶液,测其pH >7;
C.室温下,取pH=a(a<3)的H2C2O4溶液稀释100倍后,测其pH< a+2;
D.标况下,取0.10mol/L的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL;
(4)为测定某H2C2O4溶液的浓度,取20.00mL H2C2O4溶液于锥形瓶中,滴入2-3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.00mL。
①所用指示剂为_______________;滴定终点时的现象为_________________________;
②H2C2O4溶液物质的量浓度为_______________;
③下列操作会引起测定结果偏高的是__________(填序号)。
A. 滴定管在盛装NaOH溶液前未润洗
B. 滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C. 滴定前读数正确,滴定终点时俯视读数
D. 滴定前读数正确,滴定终点时仰视读数
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上,以钛铁矿为原料制备二氧化钛的工艺流程如下图所示。钛铁矿主要成分为钛酸亚铁(FeTiO3),其中一部分Fe2+在风化过程中会转化为+3价。

已知:TiO(OH)2(即H2TiO3)为两性氢氧化物
(1)步骤②中,发生反应的主要离子方程式为______________。
(2)步骤③中,实现混合物的分离是利用物质的____________(填字母序号)。
A.熔沸点差异 B.溶解性差异 C.氧化性、还原性差异
(3)步骤②、③、④中,均需用到的操作是____________(填操作名称)。
(4)请结合化学用语用化学平衡理论解释步骤④中将TiO2+转化为H2TiO3的原理:__________________________。
(5)上述工艺流程中可以循环利用的物质是____________。
(6)研究发现,可以用石墨作阳极、铁网作阴极、熔触CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。

①写出阳极所发生反应的电极反应式_________________________。
②在制备金属Ti前后,CaO的质量将______(填“增大”、“不变”或“减小”)
查看答案和解析>>
科目: 来源: 题型:
【题目】将4.74gK2SO4·Al2(SO4)3·nH2O的样品溶于水,配制成250ml溶液,取出20ml溶液,与浓度为0.064mol/L的氯化钡溶液25ml恰好完全反应生成沉淀.则K+的物质的量浓度为多少? n值为多少?
__________________、____________________
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)蛋白质主要是由_____、_____、_____、_____四种元素组成,它们的一级结构是多个不同的氨基酸通过_________结合而成的。已知某蛋白质含氮的质量分数为15%,若成人每天排出尿素[化学式为CO(NH2)2]23克,则每天从食物中摄取的蛋白质的质量平均值为______克。
(2)用5.0千克含淀粉80%(质量分数)的玉米制取葡萄糖,反应的方程式为________________,若转化率为90%,可以制得葡萄糖的质量是______千克。
查看答案和解析>>
科目: 来源: 题型:
【题目】某烃的结构简式CH3CH2CH=C(C2H5)C≡CH,分子中含有四面体结构的碳原子数为a,在同一直线上的碳原子数最多为b,一定在同一平面内的碳原子数为c,则a、b、c分别为( )
A. 4、3、5B. 4、3、6C. 2、5、4D. 4、6、4
查看答案和解析>>
科目: 来源: 题型:
【题目】下列变化过程中,属于放热反应的是( )
① 煅烧石灰石制生石灰 ② 木炭取暖③ 固体 NaOH溶于水 ④ 酸与碱的中和反应⑤ 铝热反应⑥ NH4Cl晶体与Ba(OH)2·8H2O混合搅拌
A. ① ③ ⑥B. ② ④ ⑤C. ② ③ ④D. ② ④ ⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是
A. 标准状况下,2.24LCCl4含有的共价键数为0.42NA
B. 氢原子数为0.4NA的甲醇分子中含有的键数为0.4NA
C. 1![]() Fe溶于过量硝酸,电子转移数为2NA
Fe溶于过量硝酸,电子转移数为2NA
D. 14![]() 乙烯和丙烯混合气体中的氢原子数为2NA
乙烯和丙烯混合气体中的氢原子数为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com