
【题目】熔触的金属锡在300℃左右能直接与氯气作用生成四氯化锡。四氯化锡的熔点-33℃,沸点114℃,遇潮湿空气水解。某学习小组用以下装置制取少量四氯化锡。回答下列问题:
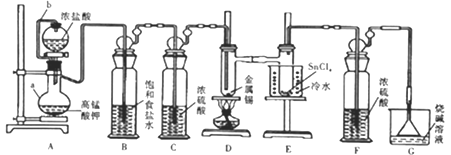
(1)仪器组装完毕,为检查装置的气密性,将装置G中漏斗改为导管且管口浸没于水中,后续操作是__________,说明气密性良好。
(2)仪器a的名称是__________;设计连接管b的目的是_______________。
(3)装置B、F的作用分別是______________、____________。
(4)装置A中反应的离子方程式为______________,排尽装置中的空气后才能点燃D处的酒精灯,判断装置中的空气已排尽的现象是_____________;D中加热的作用之一是加快氯气与金属锡反应,另一作用是__________。
(5)四氯化锡遇潮湿空气时有白色烟雾产生,同时生成白色固体(SnO2·xH2O),该反应的化学方程式为_____________。
(6)实验结束后,若制得SnCl4的质量为2.61g,Cl2的转化率为80%,则消耗KmnO4的质量为__________。
【答案】 用热毛巾捂住烧瓶,导管口有气泡逸出,停止加热后,导管口水回流,形成一段水柱 蒸馏烧瓶 避免加料时需打开分液漏斗上口玻璃塞,浓盐酸挥导致成污染 除去氯气中的氯化氢 防止水蒸气由G进入E,使产品水解 2MnO4-+16H++10Cl- = 2Mn2++5Cl2 ↑+8H2O 装置中充满黄绿色气体 促进SnCl4气化,从反应混合物中分离 SnCl4 +(x+2)H2O =SnO2·xH2O↓+ 4HCl↑ 1.58 g
【解析】试题分析:(1)根据气密性检验的方法回答。
(2)仪器a的名称是蒸馏烧瓶;连接管b能平衡烧瓶和漏斗中的压强。
(3)饱和食盐水除去氯气中的氯化氢、浓硫酸可以干燥氯气。
(4)装置A中高锰酸钾与浓盐酸反应生成氯气,根据氯气的颜色,判断装置中的空气已排尽的现象;根据金属锡在300℃左右能直接与氯气作用生成四氯化锡。四氯化锡的熔点-33℃,沸点114℃,分析D中加热的作用。
(5)四氯化锡遇潮湿空气时生成白色固体(SnO2·xH2O)和氯化氢。
(6)根据化学方程式计算。
解析:(1)仪器组装完毕,为检查装置的气密性,将装置G中漏斗改为导管且管口浸没于水中,用热毛巾捂住烧瓶,导管口有气泡逸出,停止加热后,导管口水回流,形成一段水柱,说明气密性良好。
(2)仪器a的名称是蒸馏烧瓶;连接管b能平衡烧瓶和漏斗中的压强,避免加料时需打开分液漏斗上口玻璃塞,浓盐酸挥导致成污染。
(3) 饱和食盐水除去氯气中的氯化氢、浓硫酸可以干燥氯气,装置B、F的作用分別是除去氯气中的氯化氢、干燥氯气防止水蒸气由G进入E,使产品水解。
(4) 装置A中高锰酸钾与浓盐酸反应生成氯气,反应的离子方程式为2MnO4-+16H++10Cl- = 2Mn2++5Cl2 ↑+8H2O ,氯气是黄绿色气体,判断装置中的空气已排尽的现象是装置中充满黄绿色气体;金属锡在300℃左右能直接与氯气作用生成四氯化锡。四氯化锡的熔点-33℃,沸点114℃,D中加热的作用之一是加快氯气与金属锡反应,另一作用是促进SnCl4气化,从反应混合物中分离。
(5) 四氯化锡遇潮湿空气时生成白色固体(SnO2·xH2O)和氯化氢,该反应的化学方程式为SnCl4 +(x+2)H2O =SnO2·xH2O↓+ 4HCl↑。
(6) 若制得SnCl4的质量为2.61g,Cl2的转化率为80%,则需要制备氯气的质量![]() 1.775g,则消耗KmnO4的质量为__________。
1.775g,则消耗KmnO4的质量为__________。

所以x=1.58 g


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
【题目】如图所示的装置中,金属片紧贴着滤纸,下列判断错误的是( )
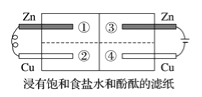
A. 左侧锌片是负极,右侧锌片是阳极 B. 左侧铜片上的电极反应为2H++2e-=H2↑
C. 阴离子移动方向分别由②→①、③→④ D. 左侧变红色的区域是②、右侧变红色的区域是④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向饱和澄清石灰水中加入一定量的生石灰,充分反应后恢复到原温度,下列有关说法中,正确的是
A. 溶液中Ca2+数目增加 B. 溶液中Ca2+数目减少
C. 溶液中OH-浓度减少 D. 溶液中OH-浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫元素有多种化合价,可形成多种化合物。 H2S和SO2在工农业生产中具有重要应用。
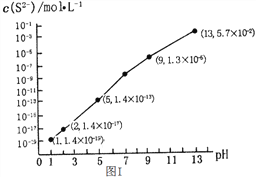
(1)H2S气体溶于水形成的氢硫酸是一种二元弱酸,25℃时,在0.10 mol/L H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图I所示(忽略溶液体积的变化、H2S的挥发)。
①pH=13时,溶液中的c(H2S)+c(HS-)=____________mol/L;
②某溶液含0.01 mol/LFe2+、未知浓度的Mn2+和0.10 mol/L H2S,当溶液pH=________时,Fe2+开始沉淀;当Mn2+开始沉淀时,溶液中![]() =____________。
=____________。
【已知:KSP(FeS)=1.4×10-19,KSP(MnS)=2.8×10-13】
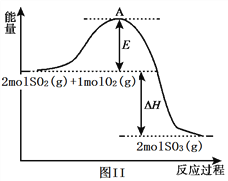
(2) 利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。已知:SO2(g)+1/2O2(g)![]() SO3(g) △H=-99kJ/mol。某温度下该反应的平衡常数K=3.33。反应过程的能量变化如图II所示。
SO3(g) △H=-99kJ/mol。某温度下该反应的平衡常数K=3.33。反应过程的能量变化如图II所示。
①图II中ΔH=____________ kJ/mol;该反应通常用V2O5作催化剂,加V2O5会使图中A点降低,原因是_____________________________________________________ 。
②该温度下,向100 L的恒容密闭容器中,充入3.0 mol SO2(g)、16.0 mol O2(g)和3.0 mol SO3(g),则反应开始时v(正)______ v(逆)(填“<”、“>”或“=”)。
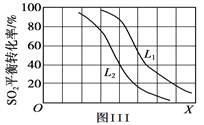
③L(L1、L2)、X可分别代表压强或温度。图III表示L一定时,SO2(g)的平衡转化率随X的变化关系。则X代表的物理量是____________;L1、L2的大小关系为L1_________L2(填“<”、“>”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4.74gK2SO4·Al2(SO4)3·nH2O的样品溶于水,配制成250ml溶液,取出20ml溶液,与浓度为0.064mol/L的氯化钡溶液25ml恰好完全反应生成沉淀.则K+的物质的量浓度为多少? n值为多少?
__________________、____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物的鉴别方法(必要时可以加热),不能达到目的的是( )
A. 用银氨溶液鉴别葡萄糖、甲酸、乙酸和乙醇溶液
B. 用碘水鉴别淀粉和纤维素
C. 用浓硝酸鉴别蚕丝和人造丝
D. 用氢氧化钠溶液鉴别植物油、汽油和甘油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】进行化学实验必须注意安全,下列说法中正确的组合是
①点燃氢气前要检验氢气的纯度,以免发生爆炸
②CO气体有毒,处理CO气体时可将其点燃,转化为无毒的CO2
③在盛O2的集气瓶中进行铁丝燃烧实验时,事先在集气瓶底部铺上一层沙子
④用氢气还原氧化铜时,先加热再通入氢气,以免浪费氢气
⑤稀释浓硫酸的操作如下图所示

A.①②③④ B.①②③ C.①②④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对气体或溶液中的离子鉴定方案正确的是
A.向溶液中加入硫酸酸化的NaCl溶液,生成白色沉淀,证明原溶液中含Ag+
B.向溶液中加入稀盐酸,生成能使澄清石灰水变浑浊的无色无味气体,证明原溶液中含![]()
C.向溶液中加入硝酸酸化的BaCl2溶液,生成白色沉淀,证明原溶液中含![]()
D.向溶液中加入浓NaOH溶液,加热后产生使湿润的红色石蕊试纸变蓝的气体,证明原溶液中含![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】主族元素在周期表中的位置取决于该元素原子的
A. 相对原子质量和核外电子数 B. 相对原子质量和最外层电子数
C. 电了层数和最外层电子数 D. 电子层数和次外层电子数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com