
科目: 来源: 题型:
【题目】有下列几种有机化合物的结构简式:(选填序号,下同)
①CH3CH═CH﹣CH2CH3 ② ③CH3CH2﹣CH2﹣CH2OH ④CH3﹣C≡C﹣CH3 ⑤CH3﹣CH2﹣C≡CH ⑥
③CH3CH2﹣CH2﹣CH2OH ④CH3﹣C≡C﹣CH3 ⑤CH3﹣CH2﹣C≡CH ⑥![]()
⑦CH3CH2CH2OCH3 ⑧![]() ⑨CH2═CH﹣CH═CH2 ⑩CH2═CH﹣CH2CH2CH3
⑨CH2═CH﹣CH═CH2 ⑩CH2═CH﹣CH2CH2CH3
(1)互为同分异构体的是______________ (2)互为同系物的是___________
(3)官能团位置不同的同分异构体是_______ (4)官能团类型不同的同分异构体是__
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是
A. 投入足量漂白粉后的溶液中:Fe2+、H+、Cl-、SO42-
B. 0.1mol/LFeCl3溶液中:Na+、Ba2+、NO3-、SCN-
C. ![]() 的溶液中:NH4+、Ca2+、Cl-、NO3-
的溶液中:NH4+、Ca2+、Cl-、NO3-
D. 水电离的c(OH-)=1×10-13mol/L的溶液中:K+、Na+、AlO2-、CO32-
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.将适量的蔗糖放入烧杯中,加入少量水,搅拌均匀。然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。
(1)生成的黑色物质是_____(填化学式)。
(2)“体积膨胀,并放出有刺激性气味的气体”,写出对应的化学反应方程式:__________。
(3)上述实验表明,浓硫酸具有____(填序号)。
①酸性 ②吸水性 ③脱水性 ④强氧化性
Ⅱ.向80 mL浓硫酸中加入56 g铜片,并加热一段时间。当反应停止后,测得反应中共有13.44 L标准状况下的SO2生成,反应中转移的电子为_________ mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 反应2H2(g)+O2(g)=2H2O(l) 在室温下可自发进行,则该反应的△H<0
B. 常温常压下,7.8gNa2O2与水完全反应,产生1.12L气体
C. 煤的干馏是物理变化,石油的裂化是化学变化
D. 气体分子总数不再改变时,反应H2(g)+I2(g)![]() 2HI(g))达到平衡
2HI(g))达到平衡
查看答案和解析>>
科目: 来源: 题型:
【题目】功能高分子P的结构简式为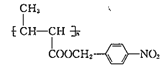 ,它的合成路线如下:
,它的合成路线如下:
![]()
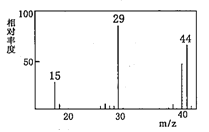
已知:① A是一种烃的含氧衍生物,它的质谱图如图。
②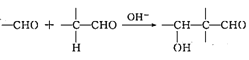
③ 醇容易被硝酸氧化。
(1)A的结构简式为_________。
(2)C中官能团的名称为_________。要检验C中的含氧官能团,下列可选用的试剂有________(填选项的字母)。
A.新制的氢氧化铜 B.溴水 C.酸性高锰酸钾溶液 D.浓硫酸
(3)E→F 的化学方程式为_________。
(4)① H物质的结构简式为_________。
② 以甲苯为原料,选用必要的无机试剂合成H,设计合成路线。(合成路线常用的表示方式为:![]() )__________
)__________
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | Z |
以下说法不正确的是
A. 非金属性:Y>硫
B. 离子半径:Y2->S2->Z-
C. 单质氧化性:Z单质>硫单质
D. Z元素在周期表中位于第三周期第ⅦA族
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室欲配制1mol/L NaOH溶液240ml,请回答:
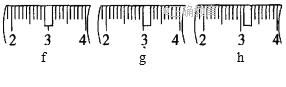
(1)需称取NaOH固体____________g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小___________(填字母),并在下图中选出能正确表示游码位置的选项____________(填字母)。
附表砝码规格
a | b | c | d | e | |
砝码大小/g | 100 | 50 | 20 | 10 | 5 |
(2)选用的主要玻璃仪器除烧杯、玻璃棒外还有_____________________________。
(3)下列操作的顺序是(用序号表示)_________________。
A、用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B、用天平准确称取所需的NaOH的质量,加入少量水,用玻璃棒慢慢搅动,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(4)下列情况对所配制的NaOH溶液浓度有何影响?(用“偏大”“偏小”“无影响”填写)
①容量瓶用蒸馏洗涤后残留有少量的水________________
②将热的溶液直接移入了容量瓶________________
③定容时,仰视容量瓶的刻度线________________
④转移溶液时,玻璃棒的下端在容量瓶的刻度线以上________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com