
科目: 来源: 题型:
【题目】下列说法正确的是
A. CH3CH2OH是由-C2H5和-OH两种官能团组成的
B. CHFCl2分子结构只有一种
C. H2与D2互为同位素
D. 13C表示核内有6个质子,核外有7个电子的一种核素
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用 KMnO4 与密度为 1.19 g·cm-3,溶质质量分数为 36.5%的 HCl 溶液反应制取氯气,反应方程式为:
2KMnO4 + 16HCl = 2KCl + 2MnCl 2 + 5Cl 2↑ + 8H2O
(1)用双桥线法分析电子转移的方向和数目____________(直接在上述方程式中表示);
(2)氧化剂_____________ 氧化产物________________
(3)若反应中有 0.5 mol 电子转移,被氧化的 HCl 的物质的量是__________ mol;
(4)c(HCl)=_________________________________ ;
查看答案和解析>>
科目: 来源: 题型:
【题目】将14.2g Na2SO4完全溶于水中,配成500 mL溶液,其物质的量浓度为__________;若从中取出50 mL,Na+物质的量浓度为___________;若将这50 mL溶液用水稀释至100 mL,所得溶液中SO42-的物质的量浓度为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)AgNO3的水溶液呈________(填“酸”、“中”或“碱”)性,原因是(用离子方程式表示):______________;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于_______中,然后再用蒸馏水稀释到所需的浓度,以________(填“促进”或“抑制”)其水解。
(2)明矾可用于净水,原因是(用离子方程式表示)______________。把FeCl3溶液蒸干、灼烧,最后得到的主要固体产物是________。
(3)用热的纯碱溶液洗涤餐具,原因是(用离子方程式表示)_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化亚砜用于医药、农药、染料工业,常作氯化剂,制锂氯化亚砜(Li/SOCl2)电池.用SO2、SCl2与Cl2反应合成SO2(g)+Cl2(g)+SCl2(g)2SOCl2(g).
(1)在373K时,向2L的密闭容器中通入SO2、SCl2与Cl2均为0.04mol,发生上述反应.测得其压强(p)随时间(t)的变化为表中数据I(反应达到平衡时的温度与起始温度相同).
t/min | 0 | 1 | 2 | 3 | 4 | 5 | |
I | p | 6.0p0 | 6.7p0 | 6.1p0 | 5.4p0 | 5.0p0 | 5.0p0 |
II | p | 6.0p0 | 7.0p0 | 5.3p0 | 5.0p0 | 5.0p0 | 5.0p0 |
请回答下列问题:
①反应开始至达到平衡时,v(SOCl2)=____________。
②若只改变某一条件,其他条件相同时,测得其压强随时间的变化为表中数据II,则改变的条件是_____。
(2)如图是某同学测定上述反应平衡常数的对数值(lgK)与温度的变化关系点.

A点的数值为_____。(已知:lg4=0.6)
(3)已知反应S4(g)+4Cl2(g)═4SCl2(g) 的△H=﹣4kJmol﹣1,1molS4(g)、1molSCl2(g)分子中化学键断裂时分别需要吸收1064kJ、510kJ的能量,则1molCl2(g)分子中化学键断裂时需吸收的能量为_____kJ。
(4)某种锂电池的负极由金属锂构成,正极由二氯亚砜(SOCl2)和碳材料构成.总反应为:4Li+2SOCl2═4LiCl+S+SO2↑,此种锂电池是一次电池,在放电时有气体产生.此电池工作时正极的电极反应式为________________,电解质中锂离子定向移向_____极(填“正极”或“负极”).
查看答案和解析>>
科目: 来源: 题型:
【题目】碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型髙效絮凝剂,在医药上也可于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的流程如下:
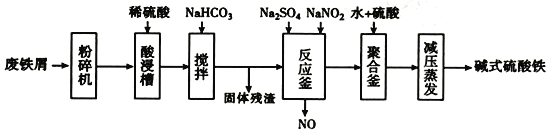
已知:
部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
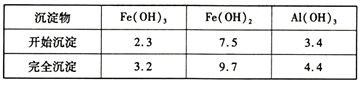
回答下列问题:
(1)粉碎过筛的目的是____________________。
(2)加入少量NaHCO3的目的是________。
(3)反应釜中发生反应的离子方程式为_______________________。在实际生产中,常同时通入02以减少NaNO2的用量,若参与反应的O2有11.2L(标准状况),则相当于约NaNO2的物质的量为________。
(4)聚合釜中溶液的PH必须控制在一定的范围内。PH偏小时Fe3+水解程度弱,PH偏大时则_____________________________________。
(5)采取减压蒸发的原因是___________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物YX2、ZX2中,X、Y、Z的核电荷数小于18;X原子最外能层的p能级中有一个轨道充填了2个电子,Y原子的最外层中p能级的电子数等于前一能层电子总数,且X和Y具有相同的电子层;Z与X在周期表中位于同一主族。回答下列问题:
(1)X的电子排布式为________,Y的轨道表示式为________;
(2)ZX2的分子式是________,YX2电子式是________ ;
(3)Y与Z形成的化合物的结构式是________,该化合物中化学键的种类是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com