
科目: 来源: 题型:
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是 ( )

A. 该硫酸的物质的量浓度为9.2mol/L
B. 1molCu与足量该硫酸反应产生2g氢气
C. 配制200mL4.6mol/L的稀硫酸需取该硫酸50mL
D. 该硫酸与等质量的水混合后所得溶液的浓度大于9.2mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. FeCl3溶液腐蚀印刷电路铜板:Cu+Fe3+=Cu2++Fe2+
B. 醋酸溶解鸡蛋壳:2H++CaCO3=Ca2++CO2↑+H2O
C. 在NaHSO4溶液中滴入Ba(OH)2溶液至溶液呈中性:Ba2++2OH-+2H++SO![]() =BaSO4↓+2H2O
=BaSO4↓+2H2O
D. 在NaHCO3溶液中滴入少量澄清石灰水:HCO![]() +Ca2++OH-=CaCO3↓+H2O
+Ca2++OH-=CaCO3↓+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g) ![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。

回答下列问题:
(1)反应的△H___________0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。在0~60s时段,反应速率v(N2O4)为_____________molL-1s-1,反应的平衡常数K1为______________。
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 molL-1s-1的平均速率降低,经10 s又达到平衡。
① T __________100℃(填“大于”“小于”),判断理由是______________________________________;
② 温度T时反应的平衡常数K2 为 ___________________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向______________(填“正反应”或“逆反应”)方向移动。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是( )
A. 1 mol Cl2中含有的原子数为NA
B. 标准状况下,a L氧气和氮气的混合物含有的分子数约为![]() ×6.02×1023个
×6.02×1023个
C. 标准状况下,22.4 L水中所含的分子数约为6.02×1023个
D. 从1 L0.5 mol·L-1NaCl溶液中取出100 mL,剩余溶液中NaCl物质的量浓度为0.45 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2,电解液为硫酸。工作时该电池总反应式为Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O。根据上述情况判断:
2PbSO4+2H2O。根据上述情况判断:
(1) 蓄电池的负极材料是________;工作时,正极反应为________________________________;
(2) 工作时,电解质溶液的pH________(填“增大”、“减小”或“不变”);
(3) 工作时,电解质溶液中的阴离子移向_______极;电流方向从______极流向______极;
(4) 充电时,铅蓄电池的负极与电源的_______极相连。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯碱厂电解精制的饱和食盐水,利用电解产品可制取漂白粉等。
(1)如果粗盐中含有SO42﹣,精制时须添加试剂除去SO42﹣,该试剂不能选用______。
A.Ba(OH)2 B.Ba(NO3)2 C.BaCl2
(2)电解饱和食盐水发生的化学方程式_________________。
(3)利用氯气和氢氧化钠溶液制取“84”消毒液的化学方程式____________。
(4)漂白粉在空气中久置后会变质的化学方程式_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】“漂粉精”Ca(ClO)2与密度为1.19g·cm-3质量分数为36.5%的HCl溶液反应生成Cl2,该化学方程式为:Ca(ClO)2 + 4HCl(浓)= CaCl2 + 2Cl2↑ + 2H2O
(1)浓盐酸在反应中显示出来的性质是____________ (填写字母)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)用双线桥法表示该氧化还原反应中电子转移情况_________________。
(3)标准状况下若产生4.48L Cl2,则反应过程中被氧化的HCl的物质的量是___。
(4)某同学欲用该浓盐酸配制100mL1mol·L﹣1HCl溶液.回答下列问题:
①需取用该浓盐酸体积为________。
②配制1mol·L﹣1HCl溶液时需用的主要仪器有烧杯、量筒、玻璃棒、胶头滴管、___。
③不规范的实验操作会导致实验结果的误差.分析下列操作对实验结果的影响偏小的是__。(请填序号)
A.容量瓶中原有少量蒸馏水 B.定容时俯视刻度线
C.玻璃棒在刻度线上方引流溶剂水 D.颠倒摇匀后发现凹液面低于刻度线但没加水
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生产、生活、社会密切相关。下列有关说法正确的是 ( )
A.沾附在试管内壁上的油脂,用热碱液洗涤
B.“春蚕到死丝方尽”里“丝”的主要成分是纤维素
C.尼龙绳、宣纸 、羊绒衫主要由合成纤维制造
D.丝织品可以用弱碱性洗涤剂或肥皂洗涤
查看答案和解析>>
科目: 来源: 题型:
【题目】下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的KI溶液、足量的CuSO4溶液和K2SO4溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加32 g。据此回答问题: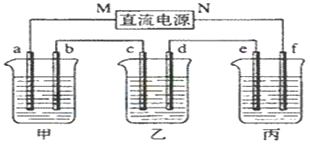
(1) 电源的N端为_________极;
(2) 电极b上发生的电极反应为____________________________________________;
(3) 电极f上生成的气体在标准状况下的体积_________________________________;
(4) 电解开始时,在甲烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是______________;
(5) 电解前后溶液的pH变化情况,(填增大、减小或不变)甲溶液___________;乙溶液_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】SO42-中存在一种特殊的π键,它是由配位氧原子p轨道上的孤对电子与中心硫原子的空3d轨道发生肩并肩重叠而形成,称为d-pπ键。下列微粒可能含有d-pπ键的是( )
A.NO3-B.PO43-C.CCl4D.SiH4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com