
科目: 来源: 题型:
【题目】化学与社会、生产、生活紧切相关。下列说法正确的是
A.石英只能用于生产光导纤维
B.从海水提取物质都必须通过化学反应才能实现
C.为了增加食物的营养成分,可以大量使用食品添加剂
D.“地沟油”禁止食用,但可以用来制肥皂
查看答案和解析>>
科目: 来源: 题型:
【题目】亚氯酸钠( NaCl02)是一种高效氧化剂和漂白剂,主要用于棉纺、纸张漂白、食品消毒、水处理等。已知:NaClO2饱和溶液在温度低于38 ℃时析出的晶体是NaClO2![]() 3H2O,高于38 ℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。纯ClO2易分解爆炸。一种制备亚氯酸钠粗产品的工艺流程如下:
3H2O,高于38 ℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。纯ClO2易分解爆炸。一种制备亚氯酸钠粗产品的工艺流程如下:
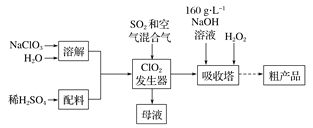
(1) ClO2发生器中的离子方程式为 ,发生器中鼓人空气的作用可能是__________(选填序号)。
a.将SO2氧化成SO3,增强酸性
b.稀释ClO2以防止爆炸
c.将NaClO3还原为ClO2
(2)吸收塔内反应的化学方程式为 ,吸收塔的温度不能超过20℃,其原因是_____________。
(3)从“母液”中可回收的主要物质是 。
(4)从吸收塔中可获得NaCl02溶液,从NaCl02溶液到粗产品(NaClO2)经过的操作步骤依次为:①减压,55℃蒸发结晶;② ;③ ;④低于60℃干燥,得到成品。
(5)为测定粗品中NaCl02的质量分数,做如下实验:
准确称取所得亚氯酸钠样品10.00 g于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴人适量的稀硫酸,充分反应(ClO2-+ 4I-+ 4H+= 2H2O+ 2I2+ Cl-)。将所得混合液配成250mL待测溶液,取25.00 mL待测液,用2.000 mol.L-lNa2S203标准液滴定(I2+2S2O32-= 2I-+S4O62-),测得消耗Na2SO3溶液平均值为16.40mL。该样品中NaClO2的质量分数为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于苯的说法中,不正确的是( )
A. 苯不溶于水,可以作为萃取剂将溴从水中分离出来
B. 苯有毒,故不能作为有机溶剂
C. 苯是煤加工的产品之一
D. 苯是一种重要的化工原料
查看答案和解析>>
科目: 来源: 题型:
【题目】将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO![]() 两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是( )
两种离子的物质的量(n)与反应时间(t)的变化示意图如图所示。下列说法不正确的是( )

A. 反应中转移电子的物质的量是0.21 mol
B. ClO![]() 的生成可能是由于温度升高引起的
的生成可能是由于温度升高引起的
C. 苛性钾溶液中KOH的质量是16.8 g
D. 一定有3.36 L氯气参加反应
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物Bilirubin在一定波长的光照射下发生分解反应,反应物浓度随反应时间变化如图所示,计算反应8~12 min间的平均反应速率和推测反应20 min时反应物的浓度,结果应是( )

A. 1.25 μmol·L-1·min-1和1.25 μmol·L-1
B. 2.5 μmol·L-1·min-1和2.5 μmol·L-1
C. 3.0 μmol·L-1·min-1和3.0 μmol·L-1
D. 5.0 μmol·L-1·min-1和3.0 μmol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,在密闭容器中发生如下反应:CO(g)+2H2(g)![]() CH3OH(g),若开始时只充入a mol CH3OH蒸气,达到平衡时,混合物的压强比起始时增大了70%;若开始时充入a mol CO和2a mol H2的混合气体,达到平衡时H2的转化率为( )
CH3OH(g),若开始时只充入a mol CH3OH蒸气,达到平衡时,混合物的压强比起始时增大了70%;若开始时充入a mol CO和2a mol H2的混合气体,达到平衡时H2的转化率为( )
A. 30% B. 35% C. 65% D. 70%
查看答案和解析>>
科目: 来源: 题型:
【题目】金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。

(1)在通常状况下,金刚石和石墨相比较,____________(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为________________。
(2)12 g石墨在一定量的空气中燃烧,生成气体36 g,该过程放出的热量为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应属于氧化还原反应,且生成物的总能量高于反应物的总能量的是
A. 铝热反应 B. 铝与盐酸反应
C. Ba(OH)2·8H2O晶体和NH4Cl晶体反应 D. 灼热的炭与CO2反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com