
科目: 来源: 题型:
【题目】甲~辛等元素在周期表中的相对位置如下表.甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( ) 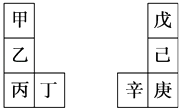
A.丙与庚的原子核外电子数相差3
B.原子半径:辛>己>戊
C.金属性:甲>乙>丁
D.乙的单质在空气中燃烧生成只含离子键的化合物
查看答案和解析>>
科目: 来源: 题型:
【题目】PETG是一种新型材料,可回收利用,对环境不构成任何威胁,其结构简式如下: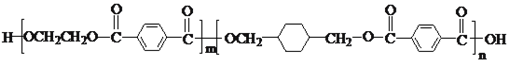 ,已知:RCOOR1+R2OH―→RCOOR2+R1OH(R、R1、R2表示烃基)。采用如下图所示的合成路线可合成PETG:
,已知:RCOOR1+R2OH―→RCOOR2+R1OH(R、R1、R2表示烃基)。采用如下图所示的合成路线可合成PETG:

试回答下列问题:
(1)试剂X为______________;反应⑦的反应类型为_______________。
(2)写出物质H的名称________________________。
(3)写出结构简式: I_____________________________。
(4)写出反应⑤的化学方程式:_________________________________________。
(5)合成时应控制的单体的物质的量n (D)∶n (F)∶n (H)=__________(用m、n表示)。
(6)同时符合下列要求的物质H的同分异构体共有__________种。
①遇FeCl3溶液显紫色;②能与NaHCO3溶液反应,并有气体放出;③能发生银镜反应。
(7)已知:![]() 请写出由D及其它必要物质可合成
请写出由D及其它必要物质可合成![]() 的反应历程。________________
的反应历程。________________
查看答案和解析>>
科目: 来源: 题型:
【题目】W,X,Y,Z均为短周期元素,W的最外层电子数与核外电子总数之比为7:17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色.下列判断正确的是( )
A.金属性:Y>Z
B.氢化物的沸点:X>W
C.离子的还原性:X>W
D.原子及离子半径:Z>Y>X
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液中除Na+外,还含有SO42—、HCO3—、SO32—和Br—等离子,通入足量Cl2,溶液中离子浓度增大的是
A. SO42— B. HCO3— C. SO32— D. Br—
查看答案和解析>>
科目: 来源: 题型:
【题目】第二、三周期元素X,Y,Z,W与第四周期元素砷(33As)在周期表中的位置关系如图所示,则下列说法中正确的是( ) 
A.W的氧化物对应的水化物必是强酸
B.X的原子半径比As原子半径小,两者原子序数之差为29
C.Z的氧化物可与Y的氢化物水溶液不会发生化学反应
D.图中五种元素均是非金属元素,并且Y的非金属性最强
查看答案和解析>>
科目: 来源: 题型:
【题目】工业品氢氧化钾溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。下列说法不正确的是
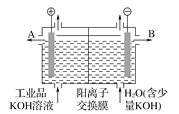
A. 阴极材料可以是Fe,含氧酸根杂质不参与电极上放电
B. 该电解槽的阳极反应式为:4OH―― 4e-= 2H2O+O2↑
C. 通电后,该电解槽阴极附近溶液pH会减小
D. 除去杂质后氢氧化钾溶液从出口B导出
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:①2H2(g)+O2(g)=2H2O(l) ΔH1=-571.6 kJ·mol-1
②2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH2=-1452 kJ·mol-1
③H+(aq)+OH-(aq)=H2O(l) ΔH3=-57.3 kJ·mol-1
下列说法正确的是( )
A. H2(g)的燃烧热为571.6 kJ·mol-1
B. 同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多
C. ![]() H2SO4(aq)+
H2SO4(aq)+![]() Ba(OH)2(aq)=
Ba(OH)2(aq)=![]() BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1
D. 3H2(g)+CO2(g)=CH3OH(l)+H2O(l) ΔH=+131.4 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】如图中,a、b、c、d、e为元素周期表中前四周期的一部分元素,下列有关叙述正确的是( ) 
A.元素c和d的最高价氧化物对应水化物的酸性:c>d
B.五种元素中,元素e的性质最稳定
C.元素b位于ⅥA族,有+6、﹣2两种常见化合价
D.元素c和e的气态氢化物的稳定性:c>e
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com