
科目: 来源: 题型:
【题目】燃烧是人类最早利用的化学反应之一,与人类的生产、生活有密切的联系:
(1)如图是探究燃烧条件的实验,铜片上的白磷燃烧而水中的白磷不燃烧,说明燃烧需要;铜片上的白磷燃烧而红磷不燃烧,说明白磷的着火点比红磷的(填“高”或“低”).
(2)加油站、仓库等地方要张贴“禁止烟火”的标志,是因为这些地方存在着大量的 , 当遇火或温度较高时,会发生燃烧甚至爆炸.
(3)实验室用灯帽盖灭酒精灯火焰,其灭火的原理是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】近日,《中国航空报》透露了一条重大消息,中国在先进高温合金领域不断获得重大成果。可以说,没有高温合金,就没有今天先进的航空发动机。下列物质中不属于合金的是
A. 硬铝 B. 玻璃钢
C. 不锈钢 D. 黄铜
查看答案和解析>>
科目: 来源: 题型:
【题目】据《本草纲目》记载:“生熟铜皆有青,即是铜之精华,大者即空绿,以次空青也。铜青则是铜器上绿色者,淘洗用之。”这里的”铜青”是指
A. CuO B. Cu2O C. Cu D. Cu2(OH)2CO3
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中进行如下反应:X2(g)+Y2(g) ![]() 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol·Lˉ1、0.3 mol·Lˉ1、0.2 mol·Lˉ1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是(mol·Lˉ1)( )
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol·Lˉ1、0.3 mol·Lˉ1、0.2 mol·Lˉ1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是(mol·Lˉ1)( )
A. Z为0.3 B. Y2为0.4 C. X2为0.2 D. Z为0.4
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物A、B、C、D、E之间的转化关系如图所示。

已知:
回答下列问题:
(l)A中含有的官能团名称为_________。
(2)由C 生成D 的反应类型为________。
(3)X 的结构简式为_________。
(4)由D 生成E 的化学方程式为_________。
(5)F是D的同分异构体,符合下列条件的F 的结构共有________种(不考虑立体异构)。
①能与NaHCO3溶液发生反应 ②能与FeCl3溶液发生显色反应 ③苯环上只有2个取代基
(6)写出以环戊烷和2-丁烯为原料(其他无机试剂任选)制备化合物![]() 的合成路线_______。
的合成路线_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2800 kJ/mol,则下列热化学方程式正确的是( )
A. C(s)+![]() O2(g)=CO(g) ΔH =-393.5 kJ/mol
O2(g)=CO(g) ΔH =-393.5 kJ/mol
B. 2H2(g)+O2(g)=2H2O(l) ΔH = +571.6 kJ/mol
C. CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH =-890.3 kJ/mol
D. C6H12O6(s) +6O2(g)=6CO2(g)+6H2O(l) ΔH =-2800 kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】金属的冶炼一般用热分解法、热还原法和电解法,选用冶炼方法的依据主要是
A. 金属在自然界里存在的形式B. 金属元素在地壳中的含量
C. 金属阳离子得电子的能力D. 金属熔点的高低
查看答案和解析>>
科目: 来源: 题型:
【题目】以软锰矿(主要成分为MnO2)和硫锰矿(主要成分为MnS)为原料(已知两种原料中均不含有单质杂质)制备高纯度硫酸锰的工艺流程如图所示。
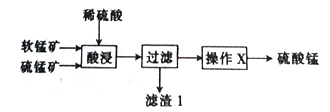
(1)已知滤渣1中含有一种非金属单质,该非金属单质的化学式为_____________________。
(2)已知二氧化锰与硫化锰的物质的量之比对酸浸时的浸出率有影响,相关实验数据如下表所示。当二氧化锰与硫化锰的物质的量之比为______________时,为最优反应配比。
号 | 二氧化锰与硫化锰的物质的量之比 | 浸出液的pH | 浸出率% |
1 | 1.25:1 | 2.5 | 95.30 |
2 | 1.75:1 | 2.5 | 97.11 |
3 | 2.25:1 | 2.5 | 99.00 |
4 | 2.5:1 | 2.5 | 98.40 |
(3)操作X为蒸发浓缩、______________、过滤,洗涤、烘干,在洗涤操作中,常用酒精洗涤MnSO4·H2O晶体,其主要目的是_________。
(4)现有10t锰矿,其中MnO2和MnS的含量均为29%,若流程中Mn的损耗率为10%,则最终制得硫酸锰(MnSO4·H2O)_________t。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com