
科目: 来源: 题型:
【题目】A、B、C、D、E是位于短周期的主族元素.已知:
①热稳定性:HmD>HmC;
②Cm﹣、E(m﹣1)﹣具有相同的电子层结构;
③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;
④A与B质子数之和是D质子数的3倍.
依据上述信息用相应的化学用语回答下列问题:
(1)HmDm的电子式 .
(2)Cm﹣、E(m﹣1)﹣的还原性强弱顺序为: , (用离子符号表示)能证明其还原性强弱的离子方程式为 .
(3)写出B单质与A元素的最高价氧化物对应水化物的溶液反应的离子方程式: .
查看答案和解析>>
科目: 来源: 题型:
【题目】铍及其化合物的应用正日益被重视。
(l)最重要的含铍矿物是绿柱石,含2%铬(Cr)的绿柱石即为祖母绿。基态Cr原子价电子排布图为__________。
(2)铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的有_____(填标号)。
A.铍属于s区主族元素 B.电负性都比镁大
C.铝的第一电离能比镁小 D.氯化物的水溶液pH均大于7
(3)铍、铝晶体都是由金属原子密置层在三维空间堆积而成(最密堆积)。铍的熔点(155lK)比铝的熔点(930K)高,原因是_______________________________________________________。
(4)氯化铍在气态时存在BeC12分子(a)和二聚分子(BeCl2)2(b),固态时则具有如下图所示的链状结构(c)。

①a属于__________(填“极性”或“非极性”)分子。
②b中Be原子的杂化方式相同,且所有原子都在同一平面上。b 的结构式为____________________ (标出配位键)。
③c中Be原子的杂化方式为__________。
④氯化铍晶体(c)中存在的作用力有__________(填标号)。
A.配位键 B. σ键 C.极性键 D.非极性键 E.离子键
(5)BeO立方晶胞如下图所示。

① BeO晶体中,O2-的配位数为___________。
② 若BeO晶体的密度为dg/cm3,则晶胞参数
a =___________________________nm (列出计算式即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知25℃时Ksp[Al(OH)3]=1.0×10-33,Ksp[Fe(OH)3]=4.0×10-38。向Fe(NO3)3和Al(NO3)3的混合溶液中逐滴加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积的关系如下图所示。计算表明当Fe3+完全沉淀时,Al3+恰好开始沉淀。下列说法正确的是 ( )

A. 原混合溶液中c(Fe3+):c(Al3+)=1:1
B. Fe(NO3)3溶液中混有杂质Al(NO3)3可以加入过量的NaOH溶液除去
C. B点两种沉淀共存,此时上层溶液中c(Al3+):c(Fe3+)=2.5×104
D. C点溶液中的溶质只有NaAlO2
查看答案和解析>>
科目: 来源: 题型:
【题目】某物质A在一定条件下加热完全分解,产物都是气体。分解方程式为 4A=B+2C+2D,测得生成的混合气体对氢气的相对密度为2 d,则A的相对分子质量为( )
A. 7d B. 5d C. 2.5d D. 2d
查看答案和解析>>
科目: 来源: 题型:
【题目】W是由A、B两种元素组成的AB2型化合物.
(1)若W是最常见的温室气体则其结构式为;
(2)若W和焦炭在高温下发生反应,所制得的半导体材料应用广泛.该反应的化学方程式为 .
(3)若W是离子化合物,其阴、阳离子均含18个电子,
①当阴、阳离子个数比为2:1时W的电子式为;
②当阴、阳离子个数比为1:1时阴离子的电子式为
(4)若A、B是同主族元素,W溶于水生成一种二元弱酸.
①如A、B为相邻周期时B在元素周期表中的位置为 . W的水溶液被双氧水氧化的化学方程式为 .
②如果A元素的周期序数是B元素的两倍,A的最高价氧化物对应水化物的分子式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于金属的叙述中正确的是( )
A. 常温下所有的金属都是固态
B. 金属具有导电、导热和延展性
C. 金属都具有较高的硬度和密度
D. 金属都具有较高的熔点和沸点
查看答案和解析>>
科目: 来源: 题型:
【题目】还原沉淀法是处理含铬(含Cr2O72-和CrO42-)工业废水的常用方法,过程如下,已知转化过程中的反应为2CrO42﹣(aq)+2H+(aq)![]() Cr2O72﹣(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是 ( )
Cr2O72﹣(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO42-有10/11转化为Cr2O72-,下列说法不正确的是 ( )
![]()
A. 溶液颜色保持不变,说明上述可逆反应达到平衡状态
B. 若用绿矾(FeSO4·7H2O)作还原剂,处理1L废水,至少需要917.4 g
C. 常温下转化反应的平衡常数K=l×1014.则转化后所得溶液的pH=6
D. 常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5mol/L,应调溶液的pH=5
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中,正确的是( )
A.NH3的空间构型是正四面体结构
B.向豆浆中加入石膏,无现象发生
C.只用淀粉溶液能检验出食盐中是否加碘
D.用双氧水清洗伤口,可以杀菌消毒
查看答案和解析>>
科目: 来源: 题型:
【题目】铬是人体必需元素,如含量不足会影响糖类和脂类的代谢,过高则会引起急性中毒。工业上往往采取下列循环工艺防止铬的污染:
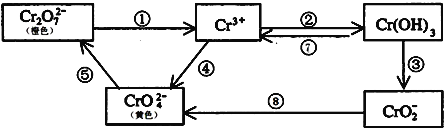
完成下列填空:
(1)含Cr2O72-离子的废水在酸性条件下用Fe3O4处理,反应的离子方程式如下,配平该离子反应方程式:
_____Cr2O72-+Fe3O4+H+→Cr3++Fe3++H2O
(2)工业上处理含Cr2O72-的废水时,一般将剧毒的Cr2O72-转化为Cr3+,以碳为阴极,铁作阳极,电解处理含NaCl、Cr2O72-的酸性废水。写出电极反应:阳极_____________________ 阴极_______________________;用铁做阳极的目的是:_____________________
(3)反应⑤是可逆反应,在Na2CrO4溶液中加入稀硫酸,溶液由黄色逐渐变成橙色,写出该反应的离子方程式:______________________
(4)已知Ag2CrO4和AgCl的Ksp分别为9.0×10-12、1.56×10-10,向含有相同浓度的Na2CrO4和NaCl的混合溶液中逐滴加入硝酸银溶液,首先生成的沉淀是__________
(5)向上述反应后的溶液中加入碱溶液,让废水的pH升至8~10,控制适当的温度,使产物中的金属阳离子全部转变为沉淀。回收所得的Cr(OH)3,经处理后又可转变成K2Cr2O7。纯净的K2Cr2O7常用于准确测定Na2S2O3溶液的物质的量浓度,方法如下:① Cr2O72- +6I- + 14H+ →3I2 + 2Cr3+ + 7H2O ② 2S2O32- + I2→S4O62- + 2I- ,准确称取纯净的K2Cr2O7 0.294g ,配成溶液,用Na2S2O3溶液滴定,消耗Na2S2O3溶液25.00mL。则Na2S2O3溶液的物质的量浓度为_____________________(保留四位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com