
科目: 来源: 题型:
【题目】化学反应原理对学习化学有重要的指导作用。某学习小组特邀你参与下列探究:
(1)影响化学平衡移动因素的探究:在NH4Cl 溶液中存在如下平衡:NH4Cl + H2O ![]() NH3.H2O + HCl,某同学以此为例探究外界条件对化学平衡的影响,实验结果记录如下:
NH3.H2O + HCl,某同学以此为例探究外界条件对化学平衡的影响,实验结果记录如下:
改变条件 | 适当升高温度 | 加水稀释 | 通入HCl(g) | 加少量NaOH固体 |
平衡移动方向 | 无需填写 | 正向 | 逆向 | 正向 |
①写出该反应的平衡常数表达式:____________________________。
②有同学认为,上表中在“条件改变”一栏除列举的4种之外,还添加一种就更为完美,你认为最好添加哪一种“改变条件”?_____________;
③“学习之道在于悟”,结合NH4Cl与水反应的方程式和影响平衡移动的因素分析:加水稀释对上述平衡的影响类似于_____________。
A.使用催化剂对化学平衡的影响; B.减小生成物浓度对化学平衡的影响;
C.升高温度对化学平衡的影响; D.减小压强对化学平衡的影响
(2)复分解反应进行的方向的探究
【提出问题】为什么只要有难溶物质、弱电解质、易挥发的物质生成复分解反应型离子反应就可以发生?
【分析解决问题】小组同学进一步深入思考,发现上述问题其实质是化学反应进行的方向问题。请你结合化学反应原理的相关知识对上述问题作出合理解释:生成难溶物质、弱电解质、易挥发的物质时将会导致体系的_______________或者__________________。
(3)反应条件(介质环境)的探究
已知I- 能被O2氧化生成I2,为探究反应条件(介质环境)设计了如下方案:
操作 | 现象 | |
第一组 | 向2mL1mol/LKI溶液中滴加几滴淀粉溶液 | 未出现蓝色 |
第二组 | 向2mL1mol/LKI溶液中滴加2mL1mol/LNaOH溶液再滴加几滴淀粉溶液 | 未出现蓝色 |
第三组 | 向2mL1mol/LKI溶液中滴加2mL1mol/LH2SO4溶液再滴加几滴淀粉溶液 | 溶液变蓝 |
①上述实验证明,该实验不能选择在中性或者碱性条件下进行,为什么?_____________;
②写出第三组实验中发生反应的离子方程式_____________;
查看答案和解析>>
科目: 来源: 题型:
【题目】回答下列问题
(1)反应mA(g)+nB(g)![]() pC(g)在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表所示:
pC(g)在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如下表所示:
压强/Pa | 2×105 | 4×105 | 8×105 |
c(A)/mol·L-1 | 0.10 | 0.20 | 0.44 |
分析表中数据可知:m、n、p的关系是:m+n______p(填>、=或<)。当压强从4×105 Pa增加到8×105Pa时,该反应的化学平衡________(填“向左”“向右”或“不”)移动,可能的原因是_____________________________________________。
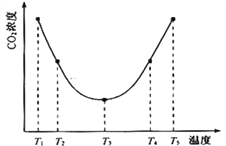
(2)利用反应:(NH4)2CO3(aq)+H2O(l)+ CO2(g)![]() 2NH4HCO3(aq) △H = akJ/mol 可以用(NH4)2CO3溶液捕获CO2以减小温室效应。为研究温度对(NH4)2CO3捕获CO2效率的影响,在某温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体(用氮气作为稀释剂),测定容器中CO2气体的浓度。在其它实验条件不变、时间间隔相同时,测得容器中CO2气体浓度随温度的变化趋势图如下:则△H______0(填>、=或<)。在T3前后容器内CO2气体浓度呈现如图变化趋势的原因是___________________________。
2NH4HCO3(aq) △H = akJ/mol 可以用(NH4)2CO3溶液捕获CO2以减小温室效应。为研究温度对(NH4)2CO3捕获CO2效率的影响,在某温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体(用氮气作为稀释剂),测定容器中CO2气体的浓度。在其它实验条件不变、时间间隔相同时,测得容器中CO2气体浓度随温度的变化趋势图如下:则△H______0(填>、=或<)。在T3前后容器内CO2气体浓度呈现如图变化趋势的原因是___________________________。
(3)某温度下,水的离子积KW = 1.0×10-12,现将100体积pH=a的H2SO4溶液和1体积pH=b的NaOH溶液混合使之呈中性,则a + b = __________。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,将某一元酸HA和NaOH溶液等体积混合,实验信息如下:
实验编号 | c(HA)/mo1·L-1 | c(NaOH)/mo1·L-1 | 反应后溶液pH |
甲 | 0.1 | 0.1 | pH=9 |
乙 | c1 | 0.2 | pH=7 |
下列判断不正确的是
A. 0.1 mo1·L-1的HA溶液中由水电离出的c(H+)=1×l0-13mo1/L
B. c1一定大于0.2 mo1·L-1
C. 甲反应后的溶液中:HA占含A微粒总数的0.02%
D. 乙反应后的溶液中:c(Na+)<c(HA)+c(A一)
查看答案和解析>>
科目: 来源: 题型:
【题目】具有抗菌作用的白头翁素衍生物H的合成路线如下图所示: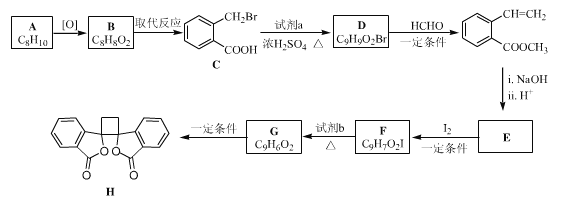
已知:
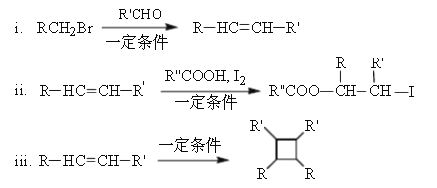
(以上R、R’、R’’代表氢、或烃基等)
(1)a属于芳香烃,名称是______________,B生成C的反应类型是__________。
(2)试剂a是(写结构简式)____________,HCHO的电子式是________________。
(3)E的结构简式是____________。
(4)由F生成G的化学方程式是 _________。
(5)二取代芳香化合物W是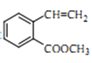 的同分异构体,能使溴的四氯化碳溶液褪色,能犮生银镜反应,能发生水解反应,W共有_______种(不含顺反异构和其他立体异构)。其中核磁共振氢谱为五组峰的结构简式为___________。
的同分异构体,能使溴的四氯化碳溶液褪色,能犮生银镜反应,能发生水解反应,W共有_______种(不含顺反异构和其他立体异构)。其中核磁共振氢谱为五组峰的结构简式为___________。
(6)以乙醇为起始原料,结合己知信息选用必要的无机试剂合成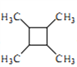 ,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。________________
,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。________________
查看答案和解析>>
科目: 来源: 题型:
【题目】配制一定物质的量浓度的KOH溶液时,导致浓度偏低的原因可能是( )
A.容量瓶中原有少量的蒸馏水
B.移液时,不慎将液体流到瓶外
C.容量瓶盛过KOH溶液,使用前未洗涤
D.定容时俯视刻度线和液面
查看答案和解析>>
科目: 来源: 题型:
【题目】温家宝总理在2010年政府工作报告中提出:“要大力开发低碳技术,推广高效节能技术,积极发展新能源和可再生能源。”下列有关做法与此不相符的是
A.大力开发丰富的煤炭资源,减少对石油的依赖
B.回收废弃饮料包装纸,制作成公园内的休闲长椅
C.在西部和沿海地区兴建风力发电站,解决能源问题
D.鼓励购买小排量汽车,推广与发展电动、混合动力汽车
查看答案和解析>>
科目: 来源: 题型:
【题目】我国的科技发展改变着人们的生活、生产方式。下列说法中错误的是
A. “甲醇制取低碳烯烃”技术可获得聚乙烯原料
B. “嫦娥四号”使用的SiC―Al材料属于复合材料
C. 5G芯片“巴龙5000”的主要材料是SiO2
D. “东方超环(人造太阳)”使用的氘、氚与氕互为同位素
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生产、生活、社会密切相关。下列有关说法中正确的是( )
A.服用铬含量超标的药用胶囊会对人体健康造成危害
B.酒精可以使蛋白质变性,酒精纯度越高杀菌消毒效果越好
C.食品袋中放置的CaO可直接防止食品氧化变质
D.“酸雨”是由大气中的碳、氮、硫的氧化物溶于雨水造成的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com